Kategorien
neuer Blog
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
- Hauptursachen für Undichtigkeiten an der Zellversiegelung von Beuteln
- Formation und Grading in der Lithium-Ionen-Batterieherstellung
Tags
Entwicklung einer Quasi-Festkörper-Na-Ionen-Batterie auf Basis einer wasserarmen Preußisch-Blau-Kathode
1. State Key Lab of Fine Chemicals, School of Chemical Engineering, Dalian University of Technology, Dalian 116024, China
2. Zweigstelle der Entwicklung neuer Materialien, Valiant Co., Ltd., Yantai 265503, China
Zusammenfassung
Im Vergleich zu Li-Ionen-Batterien bieten Na-Ionen-Batterien die Vorteile niedriger Kosten, guter Leistung bei niedrigen Temperaturen und Sicherheit und ziehen bei kosten- und zuverlässigkeitskritischen Anwendungen große Aufmerksamkeit auf sich. Mit hoher Kapazität und geringen Kosten gelten preußisch-blaue Materialien (PBAs) als vielversprechende Kathodenmaterialien für Na-Ionen-Batterien. Das Vorhandensein von kristallinem Wasser in ihrer Struktur führt jedoch zu einem schnellen Leistungsabfall der Batterie und stellt einen kritischen Engpass dar, der ihre Anwendung einschränkt. Diese Arbeit berichtet über eine einfache thermische Behandlungsstrategie zur effektiven Entfernung von kristallinem Wasser aus PBA-Kathodenmaterialien, wodurch die Kapazitätserhaltung nach 340 Zyklen von 73 % auf 88 % verbessert wird. Die In-situ-Analyse zeigt, dass der anfängliche Verlust der Coulomb-Effizienz der PBA-Kathode auf ihre irreversible Umwandlung von einer trigonalen Form in eine kubische Phase während des Lade- und Entladevorgangs zurückzuführen ist. Dieses Problem kann durch die Einführung von Na2C2O4 behoben werden, um den irreversiblen Na-Verlust in der Kathode zu kompensieren. Auf dieser Grundlage wird eine leistungsstarke Quasi-Festkörper-Na-Ionen-Batterie gebaut, indem eine PBA-Kathode mit niedrigem Wassergehalt und Na2C2O4-Zusatz und eine Anode aus hartem Kohlenstoff (HC) in einem Polyethylenglykoldiacrylat (PEGDA) kombiniert werden )-basierter Quasi-Festkörperelektrolyt mit hoher Ionenleitfähigkeit und elektrochemischer Stabilität. Diese Batterie weist spezifische Kapazitäten im Bereich von 58 bis 105 mAh·g-1 bei Stromdichten von 20 bis 500 mA·g-1 auf und ist in der Lage, stabile Zyklen über mehr als 200 Zyklen aufrechtzuerhalten. Diese Studie unterstreicht die signifikante Verbesserung der Stabilität und Kapazität von PBA-Kathodenmaterialien durch die effiziente Entfernung von kristallinem Wasser in ihnen.
Schlüsselwörter: Na-Ionen-Batterie; Quasi-Festkörperbatterie; Preußischblaue Kathode; In-situ-Analyse
Die Entwicklung leistungsstarker Batterietechnologie ist eine wichtige strategische Notwendigkeit für China, um seine Energiestruktur umzuwandeln und zu verbessern, eine kohlenstoffarme, saubere Wirtschaft zu fördern und das Ziel der „Kohlenstoffneutralität und Kohlenstoffspitze“ zu erreichen. Lithium-Ionen-Batterien gehören zu den am weitesten verbreiteten hocheffizienten Batteriesystemen. Allerdings beträgt der Lithiumvorkommen in der Erdkruste nur 0,0065 %, Chinas Lithiumressourcenreserven machen nur 7 % der weltweiten Gesamtreserven aus und fast 70 % des Lithiumcarbonats werden importiert. Es wird in Zukunft schwierig sein, den großen Bedarf im Bereich Energiespeicher und Power-Batterien zu decken. Die Häufigkeit von Natrium in der Erdkruste ist mehr als 400-mal höher als die von Lithium. Chinas Natriumreserven machen etwa 22 % der gesamten weltweiten Reserven aus. Aus Sicht der Rohstoffkosten können die Kosten für Natrium-Ionen-Batterien im Vergleich zu Lithium-Ionen-Batterien um 30 bis 40 % gesenkt werden. Darüber hinaus weisen Natrium-Ionen-Batterien im Vergleich zu Lithium-Ionen-Batterien eine bessere Leistung bei niedrigen Temperaturen, einen größeren Betriebstemperaturbereich und eine höhere Sicherheit auf. Diese einzigartigen Vorteile haben sie zu einem Schwerpunkt der Aufmerksamkeit in kostensensiblen und sicherheitskritischen Energiespeicheranwendungen gemacht [1].
Angetrieben durch das „Dual-Carbon“-Ziel erreichte Chinas Nachfrage nach Energiespeicher- und Leistungsbatterien im Jahr 2020 158,5 GWh, und es wird erwartet, dass die weltweite Nachfrage nach Batterien im Jahr 2025 in die TWh-Ära eintreten wird. Mit der Weiterentwicklung der Batterietechnologie steigt die Energiedichte von Die Zahl der Batterien hat rapide zugenommen und die Anforderungen an die Batteriesicherheit sind immer wichtiger geworden. Herkömmliche Lithium-/Natriumionenbatterien verwenden flüssige organische Elektrolyte, die zum Auslaufen neigen, was die Zuverlässigkeit der Batterie verringert [2-3]. Die Verwendung von Festkörperbatterien mit hoher thermoelektrischer Stabilität, hoher mechanischer Festigkeit und ohne Leckagerisiko ist eine mögliche Richtung zur Lösung des Zuverlässigkeitsproblems [4-5], weist jedoch Probleme wie eine hohe Dichte fester Elektrolyte und eine niedrige Ionenleitfähigkeit auf und schlechter Kontakt mit der „fest-fest“-Grenzfläche der Elektroden [6]. Quasi-feste Elektrolyte zwischen Flüssigkeit und Feststoff weisen eine bessere Stabilität und Sicherheit als flüssige Elektrolyte auf und sind Festelektrolyten in Bezug auf Ionenleitfähigkeit, Flexibilität und Grenzflächenkompatibilität überlegen [7–9]. Diese Vorteile machen darauf basierende Quasi-Festkörperbatterien zu einer der praktikableren Schwerpunktrichtungen im Bereich der fortschrittlichen Batterietechnologie.
Preußischblaue Verbindungen (PBAs) sind derzeit die beliebtesten Kathodenmaterialien für Natrium-Ionen-Batterien. Ihre offene Skelettstruktur und reichlich vorhandene Natriumspeicherplätze verleihen ihnen eine hohe theoretische spezifische Kapazität (170 mAh g-1) und eine gute Ionentransportleistung [10–11]. In Festkörperbatterien können PBAs nicht nur als Kathodenmaterialien, sondern auch als Festelektrolyte verwendet werden [12–13]. Allerdings werden PBAs im Allgemeinen durch Lösungsfällung hergestellt, wodurch Fe(CN)64--Fehlstellendefekte und eine große Menge Kristallwasser in ihrer Struktur entstehen, was die Einbettung von Na+ in das PBA-Gitter behindert und ihre Natriumspeicherkapazität begrenzt. Darüber hinaus wird das Kristallwasser in PBAs während der Batteriereaktion allmählich in den Elektrolyten freigesetzt, was zu einem schnellen Leistungsabfall der Batterie, Nebenreaktionen, Blähungen und anderen Problemen führt [11,14]. Diese Probleme schränken die Anwendung von PBAs in Festkörperbatterien ein und machen es schwierig, sie mit den meisten wasserempfindlichen anorganischen Festelektrolyten zu kombinieren. Die Bildung von Leerstellendefekten und kristallinem Wasser in PBAs kann durch Strategien wie hydrothermale Behandlung[15], langsame Kopräzipitation[16], Hemmung der Fe2+-Oxidation[17], chemisches Ätzen[18] und Elementdotierung[19-] wirksam gehemmt werden. 20]. Allerdings sind die entsprechenden technischen Prozesse komplex und schwer genau zu steuern, und auch die Leistung der gewonnenen PBA-Kathoden muss verbessert werden. Angesichts der oben genannten Probleme schlägt diese Studie eine einfache und effiziente Wärmebehandlungsmethode vor, um den Gehalt an kristallinem Wasser in PBAs zu reduzieren und ihre Natriumlagerstabilität zu verbessern. Durch In-situ-Polymerisationstechnologie wurde ein Benchmark-Festelektrolyt aus Polyethylenglykoldiacrylat (PEGDA) mit hoher Ionenleitfähigkeit und hoher elektrochemischer Stabilität entwickelt. Auf dieser Grundlage wurden die PBA-Kathode mit niedrigem Wassergehalt und die Hartkohlenstoff-Anode (HC) im PEGDA-Benchmark-Festelektrolyten aufeinander abgestimmt und der Kathode Na2C2O4 als selbstaufopfernder Natriumkompensator zugesetzt, um ein leistungsstarkes Quasi-Elektrolyt zu konstruieren. Festkörper-Natriumionenbatterie. Der dynamische Natriumspeichermechanismus der PBA-Kathode und HC-Anode wurde durch In-situ-Analysetechnologie aufgedeckt.
1 Experimentelle Methode
1.1 Vorbereitung der PBA-Kathode mit niedrigem Wassergehalt
116 mmol Natriumcitrat und 24 mmol FeSO4·7H2O wurden in 400 ml sauerstofffreiem, entionisiertem Wasser gelöst. 116 mmol Natriumcitrat und 26 mmol Na4Fe(CN)6 wurden in 400 ml sauerstofffreiem, entionisiertem Wasser gelöst. Die FeSO4-haltige Lösung wurde langsam zu der Na4Fe(CN)6-haltigen Lösung gegeben und die Reaktion 6 Stunden lang bei konstanter Temperatur gerührt. Das Produkt wurde dreimal durch Zentrifugation mit Ethanol und sauerstofffreiem entionisiertem Wasser gewaschen und 24 Stunden lang im Vakuum bei 120 °C getrocknet, um PBAs mit hohem Kristallwassergehalt (Hw-PBAs) zu erhalten. Es wurde in einen mit Argon geschützten Röhrenofen gegeben und 2 Stunden lang bei 270 °C kalziniert, um PBAs mit niedrigem Wassergehalt (Lw-PBAs) mit einer Heizrate von 0,5 °C·min-1 zu erhalten.
1.2 Probencharakterisierung
Die Morphologie und Struktur der Probe wurde mit einem Feldemissions-Rasterelektronenmikroskop analysiert. Die chemische Zusammensetzung der Probe wurde mit einem Röntgenphotoelektronenspektrometer und einem induktiv gekoppelten Plasmaemissionsspektrometer analysiert. Die Batterie wurde in situ mit einem Pulver-Röntgendiffraktometer und Laser-Raman-Spektroskopie analysiert. Der Kristallwassergehalt der Probe wurde mit einem thermogravimetrischen Analysegerät in einer Argonatmosphäre bei einer Heizrate von 10 â·min-1 analysiert.
1.3 Batteriemontage und elektrochemische Leistungsprüfung
1.3.1 Halbbatteriebaugruppe mit flüssigen Natriumionen
Zum Testen wurden CR2016-Knopfzellen zusammengebaut. Preußischblaues Kathodenmaterial (Hw-PBAs oder Lw-PBAs), Ketjen-Schwarz (KB) und Polyvinylidenfluorid (PVDF)-Binder wurden gleichmäßig in einem Massenverhältnis von 8:1:1 gemischt, N-Methylpyrrolidon (NMP) wurde als Zugabe hinzugefügt Lösungsmittel und Dispergiermittel, und die resultierende Aufschlämmung wurde gleichmäßig auf eine kohlenstoffbeschichtete Aluminiumfolie als Kathode mit einer Beladung mit aktivem Material aufgetragen 3~4 mg·cm-2. Als Gegenelektroden und Referenzelektroden wurden Natriummetallbleche verwendet. Der Elektrolyt war eine DMC/EC-Lösung (DMC: Dimethylcarbonat, EC: Ethylencarbonat, Volumenverhältnis 1:1) aus 1,0 mol·L-1 NaClO4 und 5,0 % Fluorethylencarbonat (FEC). Die Batterie wurde in einer mit Argon gefüllten Handschuhbox (Wassergehalt <10-7, Sauerstoffgehalt <10-7) zusammengebaut.
1.3.2 Flüssignatrium-Ionen-Vollbatterie-Baugruppe
Die positive Elektrode wurde mit der oben genannten Methode hergestellt, HC wurde als negative Elektrode verwendet und das N/P-Verhältnis der positiven und negativen Elektroden wurde auf 1,1–1,2 eingestellt. Die Batterie wurde in einer mit Argon gefüllten Handschuhbox (Wassergehalt <10-7, Sauerstoffgehalt <10-7) unter Verwendung des oben genannten Elektrolyten zusammengebaut.
1.3.3 Herstellung eines quasifesten Elektrolyten
PEGDA wurde mit dem oben genannten flüssigen Elektrolyten in einem Massenverhältnis von 7:93 gemischt. 5,0 % Azobisisobutyronitril (AIBN) wurden als Polymerisationsinitiator zugesetzt, um eine Vorläuferlösung eines quasi-festen Elektrolyten zu bilden. Diese Lösung wurde 10 Stunden lang auf 60 °C erhitzt, um einen quasi-festen Elektrolyten zu bilden.
1.3.4 Zusammenbau einer Quasi-Festkörper-Natriumionen-Vollbatterie
Das positive Elektrodenmaterial, Na2C2O4-Natriumzusatz, KB-Leitmittel und PVDF-Bindemittel wurden gleichmäßig in einem Massenverhältnis von 6,4:1,6:1,0:1,0 gemischt, NMP wurde als Lösungsmittel und Dispergiermittel zugegeben und die erhaltene Aufschlämmung wurde gleichmäßig auf einen Kohlenstoff aufgetragen -beschichtete Aluminiumfolie als positive Elektrode, mit einer aktiven Materialbeladung von 3~4 mg·cm-2. Als negative Elektrode wurde HC verwendet und das N/P-Verhältnis der positiven und negativen Elektrode wurde auf 1,1–1,2 eingestellt. Die Vorläuferlösung des Quasi-Festkörperelektrolyten wurde der Batterie zugesetzt, und nachdem die Batterie eingekapselt war, wurde sie 10 Stunden lang auf 60 °C erhitzt, um eine Quasi-Festkörperbatterie zu erhalten. Die Batterie wurde in einer mit Argon gefüllten Handschuhbox (Wassergehalt <10-7, Sauerstoffgehalt <10-7) zusammengebaut.
1.3.5 Batterieleistungstest
Die Ionenleitfähigkeit des Quasi-Festelektrolyten wurde durch elektrochemische Impedanzspektroskopie (EIS) an einer elektrochemischen Workstation getestet. Der Testfrequenzbereich betrug 1 Hz bis 1000 kHz und die Störungsspannungsamplitude betrug 5,0 mV. Das elektrochemische Stabilitätsfenster des quasi-festen Elektrolyten wurde durch lineare Sweep-Voltammetrie (LSV) mit einer Sweep-Rate von 5 mV·s-1 getestet. Das Material und die Batterieleistung wurden mit einem Konstantstrom-Lade- und Entladeverfahren unter Verwendung eines Land CT2001A-Batterietesters untersucht. Das Halbzellen-Spannungsfenster betrug 2,0–3,8 V (gegenüber Na/Na+), das Gesamtzellen-Spannungsfenster betrug 1,5–3,8 V und die Stromdichte betrug 10–500 mA·g-1. Beim Testen der Zyklenstabilität wurde die Batterie zunächst fünfmal bei einer Stromdichte von 50 mA·g-1 zyklisch zyklisch betrieben und anschließend wurde der Zyklenstabilitätstest bei unterschiedlichen Stromdichten durchgeführt.
2 Ergebnisse und Diskussion
2.1 Morphologie- und Zusammensetzungsanalyse
Die TGA-Kurve von Hw-PBAs in Abbildung 1(a) zeigt zwei Bereiche mit schnellem Gewichtsverlust: 1) Raumtemperatur bis 270 °C, 2) 440 bis 580 °C. Im ersteren Bereich wird der Gewichtsverlust von Raumtemperatur auf 120 °C (Massenanteil 3,1 %) durch die Entfernung von adsorbiertem Wasser verursacht; Der Gewichtsverlust von 120 auf 200 °C (Massenanteil 6,10 %) wird durch die Entfernung von interstitiellem Wasser in der PBA-Gerüststruktur verursacht; Der Gewichtsverlust von 200 auf 270 °C (Massenanteil 6,89 %) entspricht der Entfernung von Kristallwasser in PBAs. Daher wurde eine Wärmebehandlung bei 270 °C gewählt, um Wasser aus Hw-PBAs zu entfernen. Nach der Wärmebehandlung bei dieser Temperatur verloren die erhaltenen Lw-PBAs bei Raumtemperatur ~270 °C nur etwa 1,18 % ihres Gewichts, was 92,67 % weniger als das von Hw-PBAs war; und verloren etwa 0,74 % ihres Gewichts bei 200–270 °C, was 89,26 % weniger als das von Hw-PBAs war. Die obigen Ergebnisse zeigen, dass durch Wärmebehandlung verschiedene Arten von Wasser in PBAs wirksam entfernt werden können und dass die erhaltenen PBAs mit niedrigem Wassergehalt eine gute thermische Stabilität aufweisen.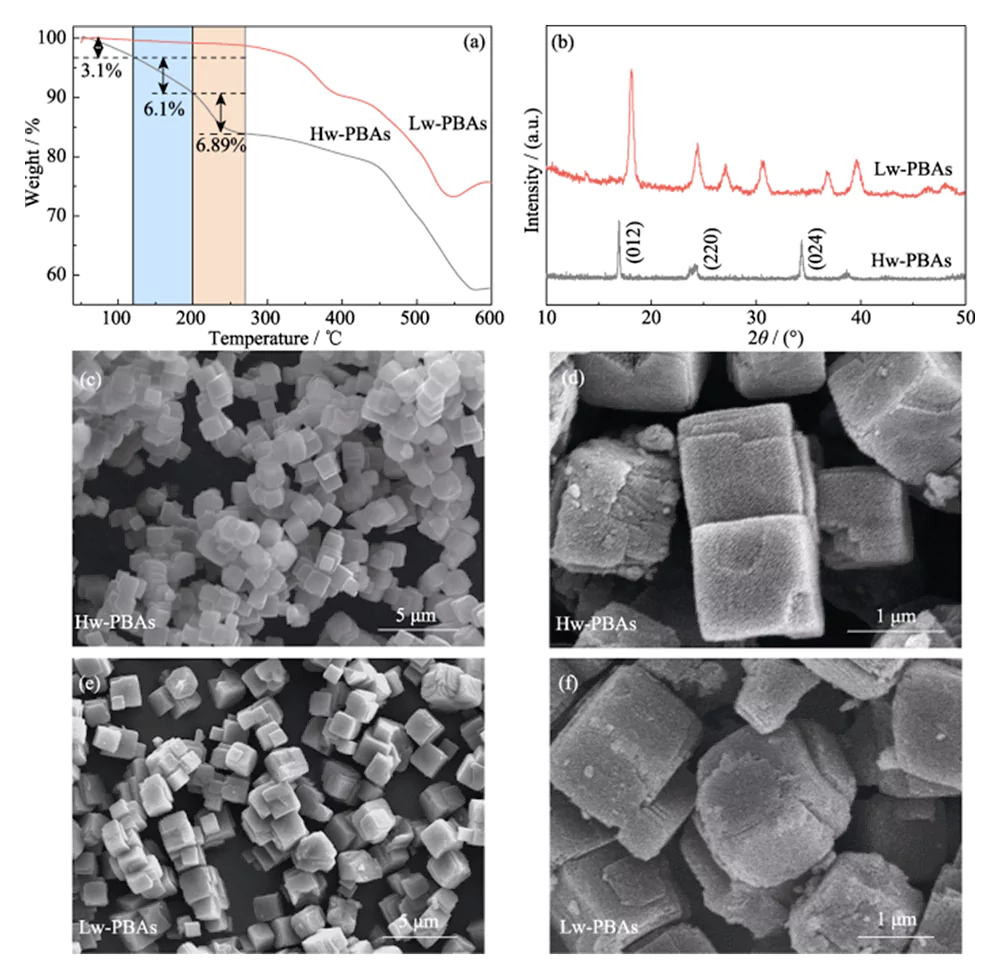
Abbildung 1(b) zeigt die XRD-Spektren von Hw-PBAs und Lw-PBAs. Die Beugungspeaks von Hw-PBAs bei 2θ=17,0°, 24,0° und 34,4° entsprechen den Kristallebenen (012), (220) bzw. (024). Nach der Wärmebehandlung verschwindet der Beugungspeak, der der (024)-Kristallebene entspricht, was darauf hinweist, dass das Kristallwasser erfolgreich entfernt wurde, und die Beugungspeakpositionen, die den (012)- und (220)-Kristallebenen entsprechen, bewegen sich in größere Winkel, was darauf hinweist Das Elementarzellenvolumen nimmt ab, nachdem das Kristallwasser entfernt wurde. Darüber hinaus erscheinen neue Beugungspeaks bei 2θ=27,1°, 30,7° und 36,9°, was darauf hindeutet, dass sich nach der Wärmebehandlung eine trigonale Kristallstruktur gebildet hat. Die SEM-Analyse (Abbildung 1(c~e)) zeigt, dass Hw-PBAs und Lw-PBAs ähnliche kubische Morphologien mit einer durchschnittlichen Größe von 2~3 µm aufweisen. Die Oberfläche der nach der Wärmebehandlung erhaltenen Lw-PBAs-Partikel ist leicht rau (Abbildung 1(f)), aber aufgrund der niedrigen Wärmebehandlungstemperatur kam es zu keinem offensichtlichen Schmelzen und Agglomerieren. Die Zusammensetzung von Lw-PBAs wurde auf Na1,91Fe-[Fe(CN)6]·3,2H2O geschätzt, indem der Metallelementgehalt mittels ICP-OES analysiert und der Wassergehalt mittels TGA gemessen wurde.
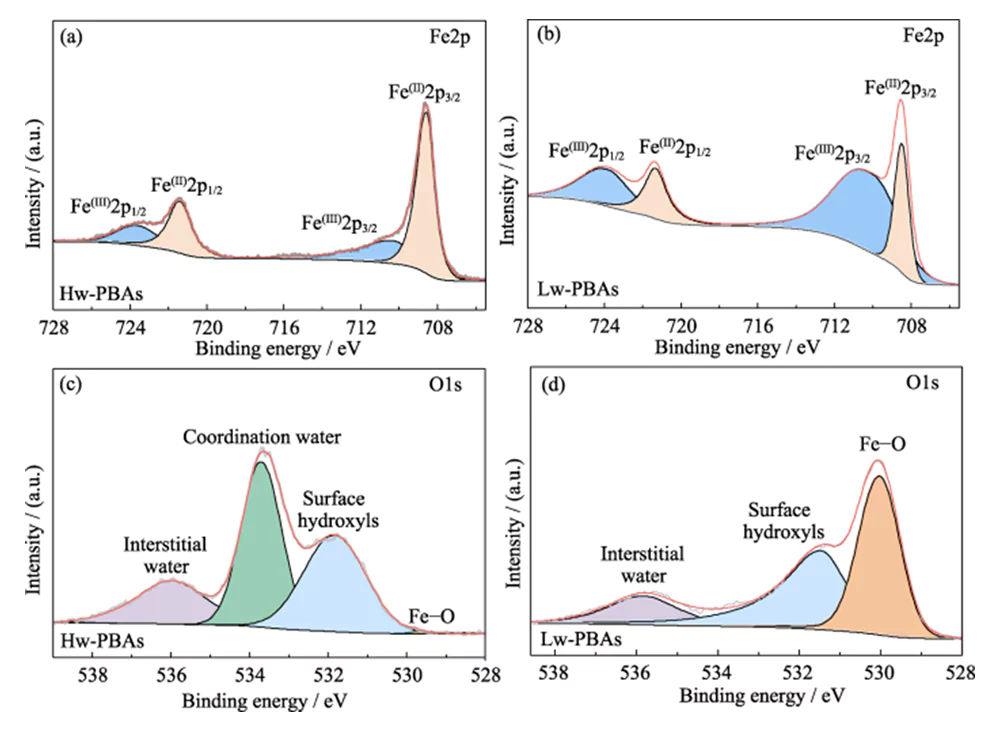
Um die chemische Zusammensetzung und Struktur von Hw-PBAs und Lw-PBAs weiter zu untersuchen, wurde eine XPS-Analyse durchgeführt. Im hochauflösenden Fe2p-XPS-Spektrum von Hw-PBAs entsprechen die beiden charakteristischen Peaks bei Bindungsenergien von 708,6 und 721,4 eV Fe(II) bzw. Fe(III) (Abbildung 2(a)). Fe(II) und Fe(III) kommen auch in Lw-PBAs vor, der Anteil an Fe(III) steigt jedoch deutlich an (Abbildung 2(b)). Dies liegt daran, dass [NaH2O]+ während des Wärmebehandlungsprozesses aus der PBA-Struktur entfernt wird und Fe(II) in Lw-PBAs teilweise oxidiert wird, um das Valenzgleichgewicht aufrechtzuerhalten. Im hochauflösenden O1s XPS-Spektrum von Hw-PBAs entsprechen die charakteristischen Peaks bei Bindungsenergien von 536,0, 533,7, 531,9 und 529,7 eV interstitiellem Wasser, koordiniertem Wasser, Oberflächenhydroxylgruppen bzw. Sauerstoffspezies im PBAs-Gitter (Abbildung). 2(c)). Nach der Wärmebehandlung verschwindet der charakteristische Peak, der koordiniertem Wasser entspricht, was darauf hindeutet, dass dieser Prozess koordiniertes Wasser effektiv aus Lw-PBAs entfernen kann (Abbildung 2(d)). Während dieses Prozesses reagiert Fe auf der Oberfläche von PBAs mit Hydroxylgruppen unter Bildung von Eisenoxiden, wodurch der charakteristische Fe-O-Peak bei der Bindungsenergie von 530,0 eV stark verstärkt wird.
2.2 Elektrochemische Leistung
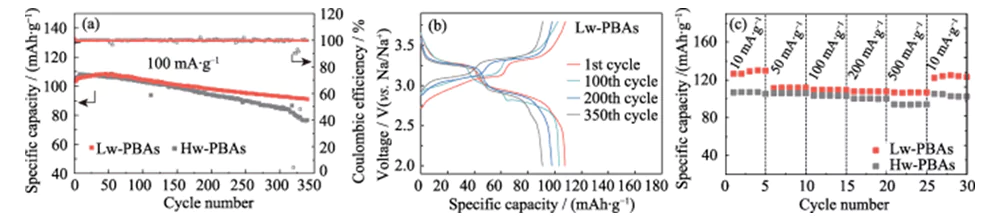
Abbildung 3(a) zeigt die Konstantstrom-Lade-Entlade-Zykluskurven von Natriumionen-Halbzellen mit Hw-PBAs und Lw-PBAs als positive Elektroden bei einer Stromdichte von 100 mA·g-1 und einem Spannungsfenster von 2,0 ~ 3,8 V (gegenüber Na/Na+). Nach 340 Lade-Entlade-Zyklen kann die positive Elektrode des Lw-PBAs immer noch eine hohe spezifische Kapazität von 91 mAh·g-1 aufrechterhalten, mit einer Kapazitätserhaltungsrate von 88 % und einer durchschnittlichen Kapazitätsverlustrate bei einem einzelnen Lade-Entladevorgang von nur 0,035 %, zeigt eine hervorragende Zyklenstabilität. Unter den gleichen Lade-Entlade-Bedingungen beträgt die Kapazitätserhaltungsrate der positiven Hw-PBA-Elektrode ohne Entfernung von Kristallwasser nur 73 %, was die wichtige Rolle der Entfernung von Kristallwasser bei der Verbesserung der Zyklenstabilität der positiven PBA-Elektrode zeigt. Abbildung 3(b) zeigt die Konstantstrom-Lade-Entlade-Kurve der Lw-PBAs-Kathode bei einer Stromdichte von 100 mA·g-1 und zeigt ein typisches Doppelspannungsplattformmerkmal: (1) Die Spannungsplattform von etwa 3,2 V entspricht zum Redoxprozess von Low-Spin-Fe2+/Fe3+ (koordiniert mit C); (2) Die Spannungsplattform von etwa 2,9 V entspricht dem Redoxprozess von High-Spin-Fe2+/Fe3+ (koordiniert mit N). Das Erscheinen einer Spannungsplattform bei etwa 3,2 V weist darauf hin, dass die Entfernung von Kristallwasser zur Stärkung der Redoxreaktion von Low-Spin-Fe2+/Fe3+ in PBAs beiträgt, was zur Verbesserung seiner Natriumspeicherkapazität beiträgt. Im anschließenden Zyklusprozess blieb die Lade-Entlade-Kurve der Lw-PBAs-Kathode im Wesentlichen konsistent und zeigte eine gute strukturelle Stabilität. Bei Stromdichten von 10, 50, 100, 200 und 500 mA·g-1 kann die Lw-PBAs-Kathode hohe reversible spezifische Kapazitäten von 126, 112, 110, 108 und 107 mAh·g-1 aufrechterhalten (Abbildung 3). (C)). Insbesondere bei einer hohen Stromdichte von 500 mA·g-1 weist die Lw-PBAs-Kathode eine hervorragende Kapazitätserhaltung auf und ihre spezifische Kapazität ist etwa 13,4 % höher als die von Hw-PBAs. Wenn die Stromdichte wieder auf 10 mA·g-1 sinkt, kann die spezifische Kapazität der Lw-PBAs-Kathode auf 125 mAh·g-1 wiederhergestellt werden, was nahe an der anfänglichen spezifischen Kapazität liegt, was darauf hindeutet, dass sie eine hervorragende Struktur beibehalten kann Stabilität bei schneller Natriumspeicherung.
2.3 In-situ-Analyse des Natriumspeichermechanismus
Die positive Elektrode von Lw-PBAs wurde mit der negativen HC-Elektrode kombiniert und eine DMC/EC-Lösung mit 1,0 mol·L-1 NaClO4 und 5,0 Massen-% FEC wurde als flüssiger Elektrolyt (LE) zum Zusammenbau einer vollständigen Batterie (Lw) verwendet -PBAs|LE|HC, Abbildung 4(a)). Die dynamischen Strukturveränderungen der positiven und negativen Elektrodenmaterialien der gesamten Batterie während der Lade- und Entladereaktionen wurden mithilfe von In-situ-Analysetechnologie untersucht. Die In-situ-XRD-Analyse der Lw-PBAs-Positivelektrode zeigte, dass nach Erhöhung der Ladespannung auf 3,2 V die Beugungspeaks, die (110) und (104) entsprechen, allmählich zu einem breiten Peak verschmolzen (Abbildung 4(b)). ). Dieses Phänomen entspricht dem Prozess, bei dem Na+ aus der positiven Elektrode des Lw-PBAs entweicht, wodurch sich die Kristallstruktur von einer trigonalen Struktur in eine kubische Struktur ändert[21]. Während des Entladungsprozesses wurde keine erneute Aufspaltung dieses breiten Peaks in (110)- und (104)-Beugungspeaks beobachtet, was darauf hindeutet, dass der Phasenänderungsprozess irreversibel ist, was zum ersten Verlust der Coulomb-Effizienz führt. Darüber hinaus führt der auf der Oberfläche gebildete Festelektrolyt-Interphasenfilm (SEI) während des ersten Lade- und Entladevorgangs der HC-Negativelektrode zu einem irreversiblen Lithiumverlust (18 %), was auch einer der Gründe für die erste Coulomb-Effizienz ist Verlust der gesamten Batterie (Abbildung 4 (c, d)).
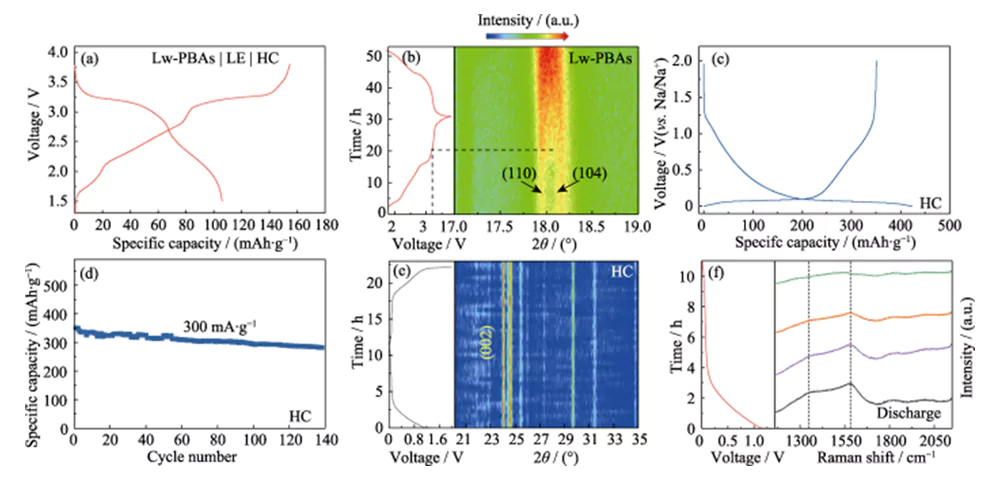
Im In-situ-XRD-Spektrum der HC-Anode wurde während des Lade- und Entladevorgangs keine offensichtliche (002)-Peakverschiebung beobachtet, was darauf hindeutet, dass Na+ nicht in die graphitierten Strukturschichten eingefügt wurde, und es wurden keine Beugungspeaks von Natriummetall beobachtet ( Abbildung 4( e)). Daher ist die Natriumspeicherkapazität der HC-Anode möglicherweise auf die Adsorption und Füllung von Na+ in den reichen Defektstellen und Poren von HC zurückzuführen und nicht auf eine Na+-Interkalation oder metallische Natriumausfällung [22]. Um den Reaktionsmechanismus der Natriumspeicherung in HC weiter zu untersuchen, wurde während des Lade- und Entladevorgangs eine In-situ-Raman-Analyse an der negativen HC-Elektrode durchgeführt (Abbildung 4 (f)). Die negative HC-Elektrode weist offensichtliche charakteristische Raman-Peaks bei 1350 und 1594 cm-1 auf. Der charakteristische Peak mit einer Wellenzahl von 1350 cm-1 entspricht der Streckschwingung der aromatischen Kohlenstoffkonfiguration (G-Modus) und der charakteristische Peak mit einer Wellenzahl von 1594 cm-1 entspricht der ungeordneten defekten Kohlenstoffstruktur (D-Modus). Das Intensitätsverhältnis von D-Modus und G-Modus (ID/IG) kann verwendet werden, um den Grad der Defekte und Unordnung von Kohlenstoffmaterialien zu messen. Während des Entladungsprozesses nahm der ID/IG der HC-Anode mit der kontinuierlichen Einlagerung von Na+ ab, was darauf hindeutet, dass das signifikante Adsorptionsverhalten von Na+ an seinen Defektstellen die Hauptquelle für die Natriumspeicherkapazität der HC-Anode ist.
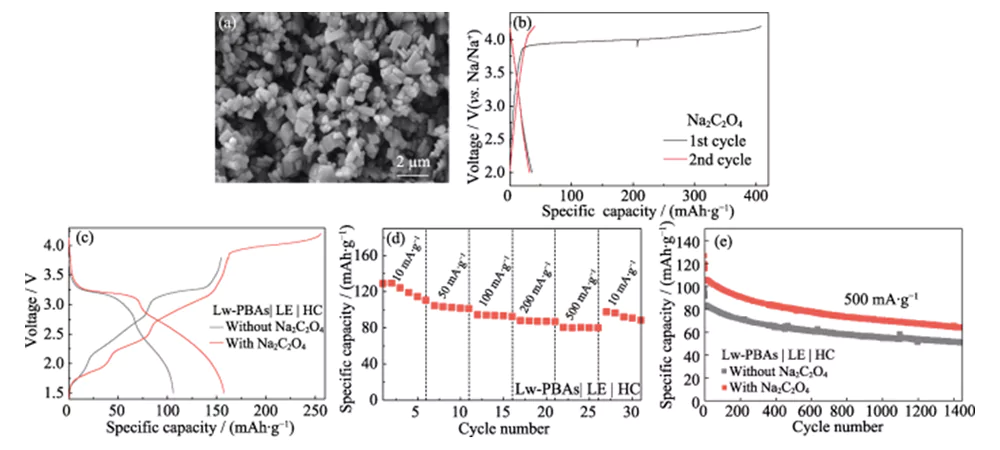
Der erste Coulomb-Wirkungsgrad der Natriumionen-Vollzelle, die unter Verwendung der positiven Lw-PBA-Elektrode und der negativen HC-Elektrode konstruiert wurde, beträgt nur 67,3 % (Abbildung 4(a)). Um dieses Problem anzugehen, wird umweltfreundliches, wenig toxisches und luftstabiles Na2C2O4 als selbstaufopfernder Natriumkompensator in der positiven Elektrode des Lw-PBAs verwendet, um den ersten Coulomb-Wirkungsgrad der Vollzelle zu verbessern [23]. Die Partikelgröße von kommerziellem Na2C2O4 beträgt mehr als Hunderte Mikrometer und weist eine geringe elektrochemische Aktivität auf. Daher wird es umkristallisiert, um Na2C2O4 mit einer Partikelgröße von mehreren Mikrometern zu erhalten (Abbildung 5(a)). Mikrometergroßes Na2C2O4 kann während des ersten Ladevorgangs innerhalb des Spannungsfensters von 2,0–4,2 V eine hohe spezifische Kapazität von 407 mAh·g·1 freisetzen und so den ersten irreversiblen Kapazitätsverlust der positiven Elektrode effektiv ausgleichen (Abbildung 5(b). )). Die anfängliche spezifische Entladungskapazität der Lw-PBAs|LE|HC-Vollzelle kann mit der Zugabe von Na2C2O4 (Massenanteil 20 %) 158 mAh·g-1 erreichen, was 92,7 % höher ist als die der Vollzelle ohne die Zugabe von Na2C2O4 (Abbildung 5(c)). Die Lw-PBAs|LE|HC-Vollzelle kann mit der Zugabe von Na2C2O4 eine reversible spezifische Kapazität von 110, 101, 92, 87 und 80 mAh·g-1 bei Stromdichten von 10, 50, 100, 200 und 500 mA aufrechterhalten ·g-1 (Abbildung 5(d)). Bei einer hohen Stromdichte von 500 mA·g-1 kann die Lw-PBAs|LE|HC-Vollzelle mit der Zugabe von Na2C2O4 nach 1400 stabilen Zyklen eine spezifische Kapazität von 64 mAh·g-1 aufrechterhalten, was 25,4 % entspricht. höher als der der gesamten Zelle ohne Zugabe von Na2C2O4 (Abbildung 5(e)).
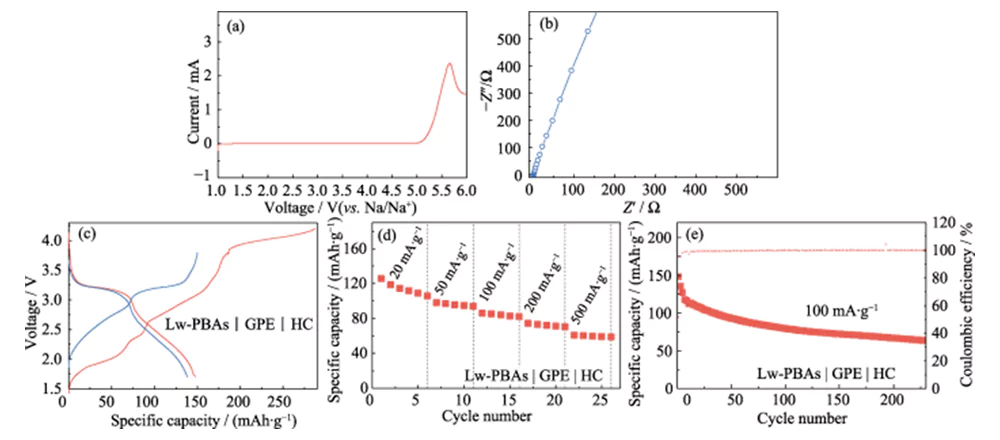
Auf dieser Basis wurde PEGDA mit 1,0 mol·L-1 NaClO4 und DMC/EC-Elektrolyt mit einem Massenanteil von 5,0 % FEC gemischt und AIBN als thermischer Polymerisationsinitiator verwendet, um einen leistungsstarken quasi-festen Elektrolyten (GPE) zu entwickeln ). Im Vergleich zu LE hat GPE die Vorteile, dass es weniger anfällig für Leckagen ist und eine geringe Volatilität aufweist. Es kann bei einer hohen Spannung von 4,9 V (gegenüber Na/Na+) stabil bleiben und weist ein breites elektrochemisches Stabilitätsfenster auf (Abbildung 6(a)). Im Vergleich zu Festelektrolyten weist GPE eine höhere Ionenleitfähigkeit und Grenzflächenkompatibilität auf, und die Ionenleitfähigkeit bei Raumtemperatur beträgt 3,51 mS·cm-1 (Abbildung 6(b)). Es wurde außerdem mit der positiven Elektrode aus Lw-PBAs mit niedrigem Wassergehalt und der negativen Elektrode aus HC kombiniert, um eine Quasi-Festkörper-Natriumionen-Vollbatterie (Lw-PBAs|GPE|HC) zu konstruieren. Bei einer Stromdichte von 100 mA·g-1 erreichte die erste Entladungskapazität der Quasi-Festkörperbatterie Lw-PBAs|GPE|HC 147,8 mAh·g-1 (Abbildung 6(c)). Bei Stromdichten von 20, 50, 100, 200 und 500 mA·g-1 können die spezifischen Kapazitäten bei 105, 94, 82, 70 und 58 mAh·g-1 gehalten werden (Abbildung 6(d)). Bei einer Stromdichte von 100 mA·g-1 kann es mehr als 200 Mal stabil zyklisch betrieben werden, und der Coulomb-Wirkungsgrad liegt nahe bei 100 % (Abbildung 6(e)).
3 Fazit
In dieser Studie wurden PBA-Kathodenmaterialien mit niedrigem Wassergehalt durch eine einfache und effiziente Wärmebehandlungsmethode hergestellt. Es wurde festgestellt, dass die Entfernung von Kristallwasser nicht nur die Kapazitätserhaltungsrate der PBA-Kathode von 73 % auf 88 % nach 340 Zyklen erhöhte, sondern auch dazu beitrug, die Redoxreaktion von Low-Spin-Fe2+/Fe3+ in PBAs zu verstärken und dadurch zu verbessern seine Natriumspeicherkapazität. Der dynamische Natriumspeichermechanismus der PBA-Kathode und HC-Anode wurde durch In-situ-Raman- und In-situ-XRD-Techniken aufgedeckt. Die Analyse zeigte, dass der Prozess des Na+-Entweichens aus der PBA-Kathode zu einer irreversiblen Veränderung der Kristallstruktur von der dreidimensionalen kubischen Struktur führte, was zum Verlust des ersten führteCoulomb-Effizienz und die Adsorption von Na+ an seinen Defektstellen waren die Hauptquelle für die Natriumspeicherkapazität der HC-Anode. Nach Zugabe von Na2C2O4-Natriumkompensator (Massenanteil 20 %) zur Kathode erhöhte sich die Erstentladungskapazität der PBA-Kathode um 92,7 %. Basierend auf der durch AIBN initiierten thermischen Polymerisation von PEGDA wurde ein leistungsstarker Quasi-Festelektrolyt mit einer Ionenleitfähigkeit bei Raumtemperatur von 3,51 mS·cm-1 und einem auf 4,9 V erweiterten elektrochemischen Stabilitätsfenster (gegenüber Na/Na+) entwickelt. Auf dieser Grundlage wurden eine PBA-Kathode mit niedrigem Wassergehalt und zugesetztem Na2C2O4-Natriumkompensator, eine HC-Anode und ein PEGDA-Benchmark-Festelektrolyt integriert, um eine Quasi-Festkörper-Natriumionenbatterie zu konstruieren, die mehr als 200 Mal stabil zyklisch betrieben werden kann eine Stromdichte von 100 mA·g-1. Studien haben gezeigt, dass eine effiziente Entfernung von Kristallwasser ein notwendiges Mittel ist, um die Zyklenstabilität der PBA-Kathode zu verbessern und die Schaffung leistungsstarker Quasi-Festkörper-Natriumionenbatterien zu ermöglichen.
[1] WANG WL, GANG Y, PENG J, et al. Wirkung der Wassereliminierung in der Preußischblau-Kathode für Natrium-Ionen-Batterien. Adv. Funktion. Mater., 2022, 32(25): 2111727.
[2] MENG X Y, LIU Y Z, WANG Z Y, et al. Eine wiederaufladbare Quasi-Festkörperzelle mit hoher Energie und überlegener Sicherheit, ermöglicht durch die stabile Redoxchemie von Li2S im Gelelektrolyten. Energieumwelt. Sci., 2021, 14(4): 2278.
[3] CHE H Y, CHEN S L, XIE Y Y, et al. Elektrolytdesignstrategien und Forschungsfortschritte für Raumtemperatur-Natriumionenbatterien. Energieumwelt. Sci., 2017, 10(5): 1075.
[4] LI W K, ZHAO N, BI Z J, et al. Na3Zr2Si2PO12-Keramikelektrolyte für Na-Ionen-Batterien: Herstellung mittels Sprühtrocknungsmethode und ihre Eigenschaften. J. Inorg. Mater., 2022, 37(2): 189.
[5] LI D, LEI C, LAI H, et al. Jüngste Fortschritte bei der Schnittstelle zwischen Kathode und Granat-Festelektrolyt für alle Festkörper-Li-Ionen-Batterien. J. Inorg. Mater., 2019, 34(7): 694.
[6] KIM KJ, BALAISH M, WADAGUCHI M, et al. Festkörper-Li-Metall-Batterien: Herausforderungen und Horizonte von Oxid- und Sulfid-Festelektrolyten und ihren Grenzflächen. Adv. Energy Mater., 2021, 11(1): 2002689.
[7] GAO H, GUO B, SONG J, et al. Ein zusammengesetzter Gel-Polymer/Glasfaser-Elektrolyt für Natriumionenbatterien. Adv. Energy Mater., 2015, 5(9): 1402235.
[8] LIU Y Z, MENG X Y, SHI Y, et al. Langlebige, anodenfreie Quasi-Festkörperbatterien, ermöglicht durch Li-kompensationsgekoppelte Schnittstellentechnik. Adv. Mater., 2023, 35(42): e2305386.
[9] DU G Y, TAO M L, LI J, et al. Niedrige Betriebstemperatur, leistungsstarke und langlebige Festkörper-Natriumionenbatterie auf Basis von Polymerelektrolyt und preußischblauer Kathode. Adv. Energy Mater., 2020, 10(5): 1903351.
[10] PENG J, ZHANG W, LIU QN, et al. Preußischblaue Analoga für Natriumionenbatterien: Vergangenheit, Gegenwart und Zukunft. Adv. Mater., 2022, 34(15): 2108384.
[11] LU YH, WANG L, CHENG JG, et al. Preußischblau: ein neues Gerüst für Elektrodenmaterialien für Natriumbatterien. Chem. Commun., 2012, 48(52): 6544.
[12] SÃNGELAND C, MOGENSEN R, BRANDELL D, et al. Stabile Zyklen von Natriummetall-Feststoffbatterien mit Polymerelektrolyten auf Polycarbonatbasis. ACS-Appl. Poly. Mater., 2019, 1(4): 825.
[13] KIM T, AHN S H, SONG Y Y, et al. Preußisch-blauer Natriumionen-leitender Festelektrolyt für alle Festkörperbatterien. Angew. Chem. Int. Hrsg., 2023, 62(42): e202309852.
[14] SONG J, WANG L, LU YH, et al. Entfernung von interstitiellem H2O in Hexacyanometallaten für eine hochwertige Kathode einer Natriumionenbatterie. J. Am. Chem. Soc., 2015, 137(7): 2658.
[15] LIU Y, FAN S, GAO Y, et al. Isostrukturelle Synthese eisenbasierter Preußischblau-Analoga für Natriumionenbatterien. Klein, 2023, 19(43): e2302687.
[16] WANG W, GANG Y, HU Z, et al. Reversible Strukturentwicklung von natriumreichem rhomboedrischem Berliner Blau für Natriumionenbatterien. Nat. Commun., 2020, 11: 980.
[17] YOU Y, YU X Q, YIN Y X, et al. Natriumeisenhexacyanoferrat mit hohem Na-Gehalt als Na-reiches Kathodenmaterial für Na-Ionen-Batterien. Nano Res., 2014, 8(1): 117.
[18] REN W H, QIN M S, ZHU Z X, et al. Aktivierung von Natriumspeicherstellen in Preußischblau-Analoga durch Oberflächenätzung. Nano Lett., 2017, 17(8): 4713.
[19] ZHANG H, GAO Y, PENG J, et al. Preußischblaue Analoga mit optimierter Kristallebenenorientierung und geringen Kristalldefekten für 450 Wh·kgâ1 Alkali-Ionen-Batterien. Angew. Chem. Int. Hrsg., 2023, 62(27): e202303953.
[20] ZHANG Z H, AVDEEV M, CHEN H C, et al. Lithiierte Preußischblau-Analoga als positive Elektroden-Aktivmaterialien für stabile nichtwässrige Lithium-Ionen-Batterien. Nat. Commun., 2022, 13: 7790.
[21] JIANG M, HOU Z, MA H, et al. Lösung der Deaktivierung von Low-Spin-Fe-Zentren durch Umverteilung der Elektronendichte hin zur hochenergetischen Natriumspeicherung. Nano Lett., 2023, 23(22): 10423.
[22] TANG Z, ZHANG R, WANG H Y, et al. Aufdeckung der geschlossenen Porenbildung von aus Abfallholz gewonnenem Hartkohlenstoff für fortschrittliche Natrium-Ionen-Batterien. Nat. Commun., 2023, 14: 6024.
[23] NIU Y B, GUO Y J, YIN Y X, et al. Hocheffiziente Kathoden-Natriumkompensation für Natrium-Ionen-Batterien. Adv. Mater., 2020, 32(33): e2001419.



