Kategorien
neuer Blog
- Leitfaden zur Auswahl von Batterieelektrolyten: Was Einkaufsmanager wissen müssen
- Ausrüstung für Knopfzellenlabore: Die vollständige Checkliste für Batterie-Forschungs- und Entwicklungslabore
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
Tags
Jüngste Fortschritte bei Materialien auf Borbasis in Lithium-Schwefel-Batterien
Jüngste Fortschritte von Borbasierte Materialien in Lithium-Schwefel-Batterien
Autor: LI Gaoran, LI Hongyang, ZENG Haibo
MIIT-Schlüssellabor von Advanced Display Materials and Devices, Institut für Nano-Optoelektronik Materialien, Fakultät für Materialwissenschaft und Werkstofftechnik, Universität Nanjing Wissenschaft und Technologie, Nanjing 210094
Zusammenfassung
Lithium-Schwefel-Batterien (Li-S) spielen eine entscheidende Rolle bei der Entwicklung der elektrochemischen Energie der nächsten Generation Speichertechnologie aufgrund ihrer hohen Energiedichte und geringen Kosten. Allerdings sind ihre Die praktische Anwendung wird immer noch durch die träge Kinetik und die geringe Geschwindigkeit behindert Reversibilität der Umwandlungsreaktionen, die dazu beitragen, relativ gering zu sein praktische Kapazität, Coulomb-Ineffizienz und zyklische Instabilität. Dabei Hinsichtlich der rationalen Gestaltung leitfähiger, adsorbierender und katalytischer Funktionen Materialien stellen einen entscheidenden Weg zur Stabilisierung und Förderung von Schwefel dar Elektrochemie. Profitieren Sie von den einzigartigen atomaren und elektronischen Strukturen von Bor weisen borbasierte Materialien vielfältige und abstimmbare physikalische, chemische und elektrochemische Eigenschaften und wurden umfassend erforscht Aufmerksamkeiten bei Li-S-Batterien. Dieser Artikel gibt einen Überblick über die jüngsten Forschungsfortschritte von Materialien auf Borbasis, einschließlich Borophen, mit Boratomen dotiertem Kohlenstoff und Metall Boride und Nichtmetallboride in Li-S-Batterien, schließt den Rest ab Probleme und schlägt die zukünftige Entwicklungsperspektive vor.
Schlüsselwörter:Lithium-Schwefel Batterie, Borid, chemische Dotierung, Borophen, Shuttle-Effekt, Rezension
Entwicklung grüner erneuerbarer Energien, Entwicklung fortschrittlicher Methoden zur Energieumwandlung und -speicherung und Einrichtung eines Ein effizientes und sauberes Energiesystem ist eine unvermeidliche Wahl, um damit umzugehen Energiekrise und Klimawandel in der heutigen Welt. Elektrochemische Energie Speichertechnologie, repräsentiert durch Batterien, kann neue saubere Energie umwandeln und speichern Energie und nutzen Sie sie in einer effizienteren und bequemeren Form, indem Sie eine spielen spielen eine wichtige Rolle bei der Förderung einer grünen Energiewirtschaft und einer nachhaltigen Entwicklung [1,2]. Unter vielen Batterietechnologien haben Lithium-Ionen-Batterien die Vorteile der hohen Energiedichte und kein Memory-Effekt. Es ist schnell gelungen Entwicklung seit seiner Kommerzialisierung im Jahr 1991 und wird in großem Umfang eingesetzt Elektrofahrzeuge, tragbare elektronische Geräte, Landesverteidigung und andere Felder [3,4]. Mit der kontinuierlichen Weiterentwicklung elektrischer Geräte Herkömmliche Lithium-Ionen-Batterien konnten den wachsenden Energiebedarf nicht decken Nachfrage. Vor diesem Hintergrund erfreuen sich Lithium-Schwefel-Batterien großer Beliebtheit Aufmerksamkeit aufgrund ihrer hohen theoretischen spezifischen Kapazität (1675 mAh·g-1) und Energiedichte (2600 Whâkg-1). Gleichzeitig, Schwefelressourcen sind reichlich vorhanden, weit verbreitet, preisgünstig und umweltfreundlich und macht Lithium-Schwefel-Batterien zu einem Forschungsschwerpunkt in auf dem Gebiet der neuen Sekundärbatterien in den letzten Jahren [5,6].
1 Funktionsprinzip und bestehende Probleme von Lithium-Schwefel-Batterien
Üblicherweise werden Lithium-Schwefel-Batterien verwendet elementarer Schwefel als positive Elektrode und metallisches Lithium als negative Elektrode Elektrode. Die grundlegende Batteriestruktur ist in Abbildung 1(a) dargestellt. Der Bei der elektrochemischen Reaktion handelt es sich um einen mehrstufigen Umwandlungsprozess mehrere Elektronentransfers, begleitet von einem Fest-Flüssig-Phasenübergang und a Reihe von Lithiumpolysulfid-Zwischenprodukten (Abbildung 1(b)) [7,8]. Darunter, elementarer Schwefel und kurzkettiges Li2S2/Li2S an beiden Enden des Reaktionskette sind im Elektrolyten unlöslich und liegen in Form vor Niederschlag auf der Elektrodenoberfläche. Langkettiges Lithiumpolysulfid (Li2Sx, 4â¤xâ¤8) hat eine höhere Löslichkeit und Migrationsfähigkeit im Elektrolyten. Bezogen auf die intrinsischen Eigenschaften von Elektrodenmaterialien und ihrer Fest-Flüssig-Phase Transformationsreaktionsmechanismus, Lithium-Schwefel-Batterien haben Energie und Kostenvorteile, stehen aber auch vor vielen Problemen und Herausforderungen [9,10,11,12]:
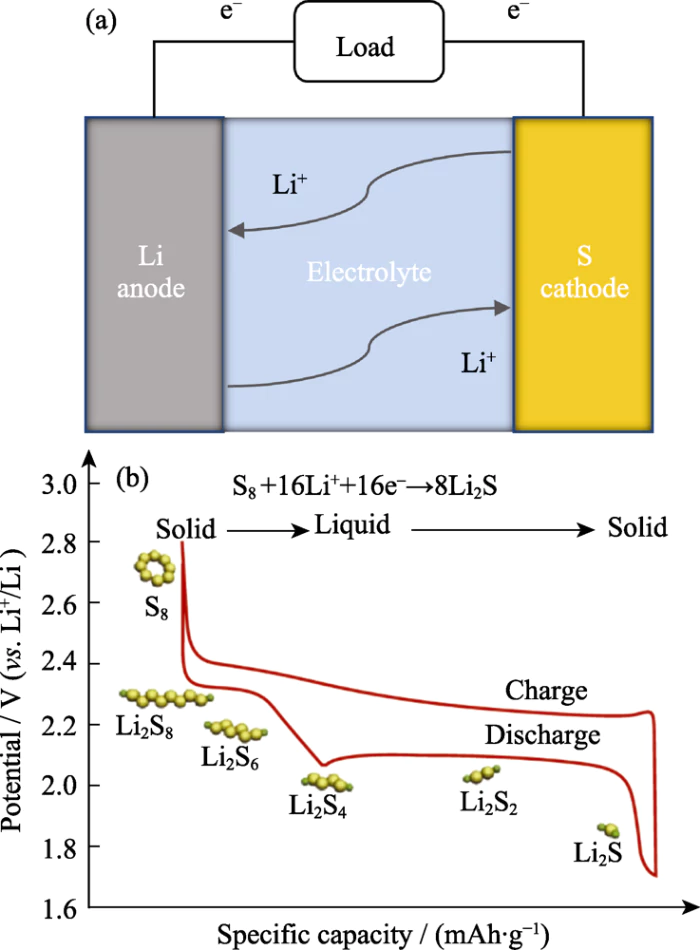
Abb. 1 Schematische Darstellung einer Lithium-Schwefel-Batterie Konfiguration und (b) entsprechender Lade-Entlade-Prozess[7]
1) Elementarer Schwefel und Li2S in fester Phase sammeln sich auf der Elektrodenoberfläche an und ihre intrinsischen Elektronen und Ionen sind vorhanden Trägheit führt zu Schwierigkeiten bei der Ladungsübertragung und einer langsamen Reaktionskinetik. Dadurch wird die Auslastungsrate aktiver Materialien und die tatsächliche reduziert Kapazität des Akkus.
2) Es besteht ein großer Dichteunterschied zwischen Schwefel und Li2S an beiden Enden der Reaktionskette (2,07 vs. 1,66 gâcm-3). Dabei erfährt das Material eine Volumenänderung von bis zu 80 % den Reaktionsprozess und die mechanische Strukturstabilität der Elektrode steht vor großen Herausforderungen.
3) Das Auflösungs- und Migrationsverhalten von Lithiumpolysulfid im Elektrolyten verursacht einen starken „Shuttle“. Effekt", was zu schwerem Aktivmaterialverlust und Coulomb-Verlust führt. In Darüber hinaus ist Lithiumpolysulfid an der chemischen/elektrochemischen Seite beteiligt Es kommt zu Reaktionen an der Anodenoberfläche, die nicht nur zu weiteren Aktivstoffverlusten führen Materialien, sondern passiviert und korrodiert auch die Anodenoberfläche, verschlimmert die Bildung und Wachstum von Lithiumdendriten und erhöhte Sicherheitsrisiken.
Diese Probleme hängen miteinander zusammen und beeinflussen sich gegenseitig, was die Komplexität der Batterie stark erhöht System, was es für aktuelle Lithium-Schwefel-Batterien schwierig macht, die Anforderungen zu erfüllen Bedürfnisse praktischer Anwendungen im Hinblick auf die aktive Materialnutzung, aktuell Energiedichte, Zyklenstabilität und Sicherheit. Aus der Analyse des oben Gesagten Probleme, es kann gesehen werden, dass vernünftige kontrolle der schwefel elektrochemische Der Reaktionsprozess ist die einzige Möglichkeit, die Leistung von Lithium-Schwefel zu verbessern Batterien. So erreichen Sie ein wirksames Management und eine Verbesserung des Schwefelgehalts Die Elektrochemie hängt von der gezielten Gestaltung, Entwicklung und Anwendung ab fortschrittliche Funktionsmaterialien. Unter ihnen ist die repräsentativste Strategie Funktionsmaterialien mit Leitfähigkeit, Adsorption und Katalyse zu entwickeln Eigenschaften als Schwefelkathodenwirte oder modifizierte Separatoren. Durch seine physische und chemische Wechselwirkung mit Lithiumpolysulfid, dem aktiven Material auf den Bereich der positiven Elektrode beschränkt, wodurch Auflösung und Diffusion gehemmt werden, und Förderung seiner elektrochemischen Umwandlung. Dadurch wird der Pendelverkehr erleichtert Wirkung und verbessert die Energieeffizienz und Zyklenfestigkeit der Batterie [13,14]. Basierend auf dieser Idee haben Forscher verschiedene Arten von entwickelt Funktionsmaterialien gezielt einzusetzen, darunter auch Carbon-Materialien, leitfähige Polymere, metallorganische Gerüste, Metalloxide/-sulfide/-nitride, usw. Es wurden gute Ergebnisse erzielt [15,16,17,18,19].
2 Anwendung von Materialien auf Borbasis in Lithium-Schwefel-Batterien
Bor ist das kleinste Metalloidelement. Sein kleiner Atomradius und seine große Elektronegativität erleichtern die Bildung metallische kovalente Verbindungen. Boratome haben einen typischen Elektronenmangel Struktur und ihre Valenzelektronenkonfiguration ist 2s22p1. Sie können teilen ein oder mehrere Elektronen mit anderen Atomen durch verschiedene Hybridisierungsformen bilden Mehrzentrenbindungen [20,21]. Diese Eigenschaften machen das Borid aus Die Struktur ist hochgradig abstimmbar und zeigt einzigartige und reichhaltige chemische und physikalische Eigenschaften Eigenschaften und können in vielen Bereichen wie der Leichtindustrie, Baumaterialien, Landesverteidigung, Energie usw. [22,23]. Im Vergleich dazu die Die Forschung zu borbasierten Materialien in Lithium-Schwefel-Batterien ist noch nicht abgeschlossen Kindheit. In den letzten Jahren haben Nanotechnologie und Charakterisierungsmethoden zugenommen weiter vorangetrieben, und die strukturellen Eigenschaften von Bor-basierten Materialien wurden kontinuierlich erforscht und weiterentwickelt, um ihre Ziele zu erreichen Auch die Erforschung und Anwendung von Lithium-Schwefel-Systemen zeichnet sich ab. In Vor diesem Hintergrund konzentriert sich dieser Artikel auf typische Materialien auf Borbasis wie z Borophen, mit Boratomen dotierter Kohlenstoff, Metallboride und Nichtmetallboride. Das Der Artikel gibt einen Überblick über die neuesten Forschungsfortschritte bei Lithium-Schwefel-Batterien. fasst bestehende Probleme zusammen und freut sich auf die zukünftige Entwicklung Wegbeschreibungen.
2.1 Boren
Als sehr repräsentatives Allotrop unter Bor-Elemente, Borophen hat eine einatomige zweidimensionale Struktur ähnlich wie Graphen. Im Vergleich zum Massenelement Bor ist es überlegen elektrische, mechanische und thermische Eigenschaften und ist ein aufstrebender Stern in zweidimensionale Materialien [24]. Basierend auf topologischen Unterschieden in der Aufgrund der Anordnung der Boratome weist Borophen reichhaltige Kristallstrukturen auf elektronische Eigenschaften sowie anisotrope Leitfähigkeitseigenschaften. Wie es sein kann Wie aus Abbildung 2(a, b) hervorgeht, neigen Elektronen in Borophen dazu, sich auf das zu konzentrieren Spitze der Boratome, und diese Elektronenpolarisationsbereiche weisen eine höhere Bindung auf Aktivität. Es wird erwartet, dass es gute chemische Adsorptionsstellen bietet Polysulfide in Lithium-Schwefel-Batteriesystemen [25]. Gleichzeitig ist die Borophenfilm hat eine gute elektrische Leitfähigkeit sowie physikalische und chemische Eigenschaften Stabilität, daher hat es ein gutes Anwendungspotenzial in Lithium-Schwefel-Batterien.
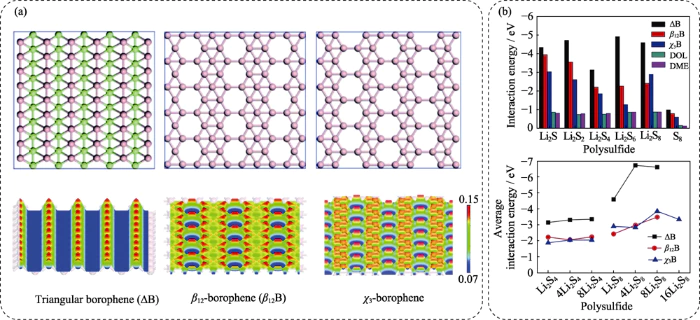
Abb. 2 (a) Strukturmodelle verschiedener Borophene und ihre entsprechenden Ladungsdichteverteilungen, (b) Adsorptionsenergien von Polysulfide auf verschiedenen Borophenen[25]
Jiang et al. [26] theoretisch gefunden Berechnungen zufolge weist Borophen eine starke Adsorptionsfähigkeit für Lithium auf Polysulfid. Allerdings kann diese starke Wechselwirkung auch leicht das auslösen Zersetzung von Li-S-Clustern, was zum Verlust des aktiven Schwefels führt Material. Im Vergleich dazu weist die Oberfläche von Borophen einen intrinsischen Defekt auf Struktur adsorbiert Lithiumpolysulfid sanfter [27], was dies ermöglicht Begrenzen Sie das Shuttle-Verhalten und vermeiden Sie gleichzeitig die Zersetzung und Zerstörung von die Ringstruktur. Es wird erwartet, dass es sich zu einem besser geeigneten Lithium entwickelt Polysulfid-Adsorptionsmaterial. Gleichzeitig erfolgt die Energiebandanalyse Ergebnisse der Borophen-Lithiumpolysulfid-Adsorptionsstruktur zeigen, dass die Adsorptionscluster sind metallisch, was hauptsächlich auf den intrinsischen Metallgehalt zurückzuführen ist Eigenschaften von Bor und seine starke elektroakustische Kopplungsstärke. Es Es wird erwartet, dass es dazu beiträgt, den elektrochemischen Umwandlungsprozess von Schwefel zu erhalten bessere Reaktionskinetik [28]. Darüber hinaus haben Grixti et al. [29] simulierte das Diffusionsprozess von Lithiumpolysulfidmolekülen auf der Oberfläche von β12-Boren. Es wurde festgestellt, dass β12-Boren eine starke Adsorption an eine Reihe zeigte von Lithiumpolysulfiden. Die niedrigsten Diffusionsenergiebarrieren von Li2S6 und Li2S4-Moleküle in Sesselrichtung betragen 0,99 bzw. 0,61 eV. was einfacher ist als die Diffusion in Zick-Zack-Richtung. Dank seiner guten Adsorptionskapazität und moderate Diffusionsenergiebarriere, β12-Boren ist gilt als ausgezeichnetes Lithiumpolysulfid-Adsorptionsmaterial Es wird erwartet, dass der Shuttle-Effekt in Lithium-Schwefel-Batterien unterdrückt und verbessert wird die Reversibilität elektrochemischer Schwefelreaktionen.
Die meisten aktuellen Forschungsergebnisse zu Die Borverdünnung in Lithium-Schwefel-Batterien entspricht immer noch der theoretischen Vorhersage Stadium, und experimentelle Bestätigungen werden selten gemeldet. Das liegt vor allem daran auf die Schwierigkeit, Bor verdünnt herzustellen. Die Existenz von Bor war in den 1990er Jahren vorhergesagt, aber erst 2015 tatsächlich vorbereitet [30]. Teil Der Grund könnte darin liegen, dass Bor nur drei Valenzelektronen hat und dies auch tun muss bilden eine Gerüststruktur, um die fehlenden Elektronen zu kompensieren Es ist einfacher, eine 3D- als eine 2D-Struktur zu bilden. Derzeit ist die Vorbereitung von Bei der Herstellung von Bor kommen in der Regel Technologien wie Molekularstrahlepitaxie und Hochtechnologie zum Einsatz Vakuum, hohe Temperatur und andere Bedingungen sowie die Syntheseschwelle hoch [31]. Daher ist es notwendig, eine einfachere und effizientere Lösung zu entwickeln Bor-verdünnte Synthesemethode und weitere experimentelle Erforschung und demonstrieren seine Wirkung und die damit verbundenen Mechanismen in Lithium-Schwefel-Batterien.
2.2 Mit Boratomen dotierter Kohlenstoff
Chemisch dotierte Kohlenstoffmaterialien sind heiß Materialien im Bereich der neuen Energieforschung. Eine entsprechende Elementdotierung kann Behalten Sie die Vorteile von Kohlenstoffmaterialien bei, z. B. geringes Gewicht und hohe Höhe Leitfähigkeit und verleihen ihnen gleichzeitig zusätzliche physikalische und chemische Eigenschaften Anpassung an verschiedene Anwendungsszenarien [32,33]. Chemisch dotierter Kohlenstoff Materialien wurden unter anderem in Lithium-Schwefel-Batterien umfassend untersucht [34,35]. was eine Dotierung mit stark elektronegativen Atomen wie Stickstoffatomen ist gemeinsam. Im Gegensatz dazu hat Bor eine elektronenarme Struktur und ist weniger vorhanden elektronegativ als Kohlenstoff. Nach der Einarbeitung wird es elektropositiv in das Kohlenstoffgitter. Es wird erwartet, dass eine gute Adsorptionswirkung entsteht negativ geladene Polysulfid-Anionen, wodurch der Shuttle-Effekt gemildert wird [36,37].
Yang et al. [38] verwendeten bordotiertes poröses Material Kohlenstoff als Schwefel-Kathodenwirtsmaterial und fanden heraus, dass Bordotierung nicht nur Die elektronische Leitfähigkeit des Kohlenstoffmaterials wurde verbessert, aber auch induziert positive Polarisation der Kohlenstoffmatrix. Negativ geladene Polysulfidionen werden durch elektrostatische Adsorption wirksam adsorbiert und verankert Lewis-Wechselwirkung, wodurch ihre Auflösung und Diffusion gehemmt wird (Abbildung 3(a, b)). Daher weist die Schwefelkathode einen mit Bor dotierten porösen Kohlenstoff auf höhere Anfangskapazität und stabilere Radfahrleistung als reines Carbon und stickstoffdotierte Proben. Xu et al. [39] erhielten mit Boratomen dotierten Kohlenstoff Nanoröhren/Schwefel-Verbundkathodenmaterial (BUCNTs/S) durch eine Hydrothermalanlage Ein-Topf-Methode. Durch die Flüssigphasen-In-situ-Synthese wird Schwefel gleichmäßiger hergestellt im Verbundwerkstoff verteilt, während Bordotierung den kohlenstoffbasierten Wirt ergibt Material höhere elektrische Leitfähigkeit und stärkere Fähigkeit zur Schwefelfixierung. Der Die resultierende BUCNTs/S-Elektrode erreichte eine anfängliche Kapazität von 1251 mAhâg-1 bei 0,2 °C und konnte nach 400 Zyklen immer noch eine Kapazität von 750 mAhâg-1 beibehalten. Zusätzlich zu Schwefelkathodenwirten, Auch mit Bor dotierte Kohlenstoffmaterialien spielen bei der Gestaltung eine wichtige Rolle Batterie-Funktionsseparatoren. Han et al. [40] beschichtet, leicht, bordotiert Graphen auf einem herkömmlichen Separator, um eine funktionelle Modifikation zu konstruieren Schicht, die durch Adsorption und Wiederverwendung von Polysulfiden wirksam gelindert wird den Shuttle-Effekt und verbessern die Ausnutzungsrate aktiver Materialien.
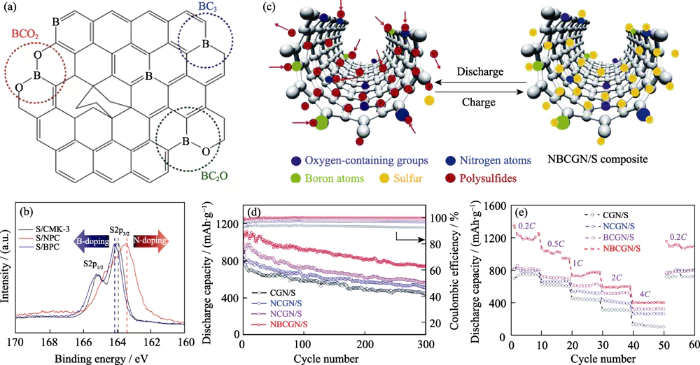
Abb. 3 (a) Schema des B-dotierten Kohlenstoffrückgrats, (b) S2p XPS Spektren von Schwefelkompositen auf Basis unterschiedlich elementdotierter poröser Kohlenstoffe; und (c) Schema des Lade-Entlade-Prozesses des NBCGN/S-Verbundwerkstoffs, (d) Zyklen bei 0,2C und (e) Ratenleistungen von Schwefelelektroden basierend auf verschiedene elementdotierte gebogene Graphen-Nanobänder[44]
Angesichts der grundlegenden Eigenschaften von verschiedene Dotierungselemente und ihre unterschiedlichen Wirkungsweisen im Kohlenstoff Gitterstruktur, Multi-Element-Co-Dotierung ist eine der wichtigen Strategien zur Regulierung der Oberflächenchemie von Kohlenstoffmaterialien und zur Verbesserung des Schwefelgehalts elektrochemische Reaktionen [41, 42, 43]. In diesem Zusammenhang Kuangs Forschungsgruppe [44] synthetisierten mit Stickstoff und Bor kodotierte Graphen-Nanobänder (NBCGNs) für erstmals durch eine hydrothermale Methode als Wirtsmaterial für die Schwefelkathode, wie in Abbildung 3(c) gezeigt. Die Studie ergab, dass die Synergie Der Effekt der gleichzeitigen Dotierung mit Stickstoff und Bor führt nicht nur dazu, dass NBCGNs größer werden spezifische Oberfläche, Porenvolumen und höhere Leitfähigkeit, sondern trägt auch dazu bei Schwefel gleichmäßig in der Kathode verteilen. Noch wichtiger ist, dass Bor und Stickstoff fungieren als elektronenarme und elektronenreiche Zentren im Codotierten System. Es kann über Lewis mit Sx2- bzw. Li+ verbunden werden Wechselwirkungen, wodurch Lithiumpolysulfid effizienter und signifikanter adsorbiert wird Verbesserung der Zyklus- und Geschwindigkeitsleistung der Batterie (Abbildung 3(d, e)). Basierend zu ähnlichen Dotierungsstrategien von Elementen mit hoher und niedriger Elektronegativität. Jin et al. [45] stellten einen mit Bor und Sauerstoff codotierten mehrwandigen Kohlenstoff-Nanoröhrchen-Wirt her Materialien, die Borsäure als Dotierungsmittel verwenden. Die resultierende Batterie hält immer noch eine spezifische Kapazität von 937 mAhâg-1 nach 100 Zyklen, was ist deutlich besser als die Batterieleistung auf Basis von gewöhnlichem Kohlenstoff Röhren (428 mAhâg-1). Darüber hinaus haben Forscher es auch versucht andere Formen des Co-Dopings. Einschließlich Borosilikat-codotiertes Graphen [46], Kobalt Mit Metall und Borstickstoff codotiertes Graphen [47] usw. haben wirksame Ergebnisse erzielt verbesserte Batterieleistung. Der synergistische Effekt der co-dotierten Komponenten spielt eine entscheidende Rolle bei der Verbesserung der elektrochemischen Schwefelreaktion.
Die Dotierung mit Borelementen kann wirksam sein verbessern die intrinsische Leitfähigkeit und die chemische Oberflächenpolarität von Kohlenstoff Materialien, verstärken die chemische Adsorption und hemmen das Pendelverhalten von Lithiumpolysulfid, wodurch die elektrochemische Reaktionskinetik von Schwefel verbessert wird und Stabilität sowie Verbesserung der Batterieleistung. Trotzdem gibt es sie immer noch viele Probleme bei der Erforschung bordotierter Kohlenstoffmaterialien in Lithium-Schwefel Batterien, die weiter erforscht und analysiert werden müssen. Zum Beispiel der Einfluss der Bor-Dotierungsmenge und der Dotierungskonfiguration auf der Leitfähigkeitsoberfläche Ladungsverteilung und Adsorptionsverhalten von Lithiumpolysulfid aus Kohlenstoff Materialien. Gleichzeitig geht es darum, Kohlenstoffmaterialien mit hohem Borgehalt zu erhalten Die Dotierungsniveaus und die genaue Steuerung der Dotierungskonfiguration hängen davon ab über die Entwicklung fortschrittlicher Zubereitungsmethoden und -technologien. In Darüber hinaus ist für kodotierte Systeme mit mehreren Elementen ein geeigneteres Dotierungselement geeignet Kombinationen müssen noch weiter untersucht werden. Richten Sie eine Systematik ein Struktur-Aktivitäts-Beziehung zur Klärung des synergistischen Wirkungsmechanismus von die co-dotierte Struktur und ihr Einfluss auf den Modus und die Intensität des Wirt-Gast-Verhältnisses Wechselwirkungen in der Schwefelelektrochemie.
2.3 Metallboride
Metallverbindungen waren schon immer ein Forschungsgegenstand Hotspot für Funktionsmaterialien in Lithium-Schwefel-Batterien intrinsische chemische Polaritätseigenschaften und gute morphologische und strukturelle Plastizität. Es unterscheidet sich von gewöhnlichen Metalloxiden, Sulfiden, Nitride und andere ionische Verbindungen. Metallboride bestehen normalerweise aus Bor und Metallelemente, die auf kovalenten Bindungen basieren, und ihre gefüllte Struktur erbt Teil der Metallizität. Es weist eine viel höhere Leitfähigkeit als andere Metalle auf Verbindungen (Abbildung 4) [48, 49, 50, 51, 52, 53, 54, 55, 56] und können a schnelle Bereitstellung von Elektronen für elektrochemische Reaktionen [57]. Gleichzeitig, Es gibt eine lokal begrenzte polare Ionenbindungsstruktur zwischen Metall und Bor. die gute Adsorptionsstellen für Polysulfide bieten können [58,59]. Zusätzlich, die Stabilität von stark elektronegativem Bor wird nach dem Legieren mit geschwächt Übergangsmetalle und es ist einfacher, an Redoxreaktionen teilzunehmen. Das ermöglicht die Beteiligung von Metallboriden an Lithium-Schwefel elektrochemische Reaktionen durch Oberflächenreaktionen als Vermittler [60].
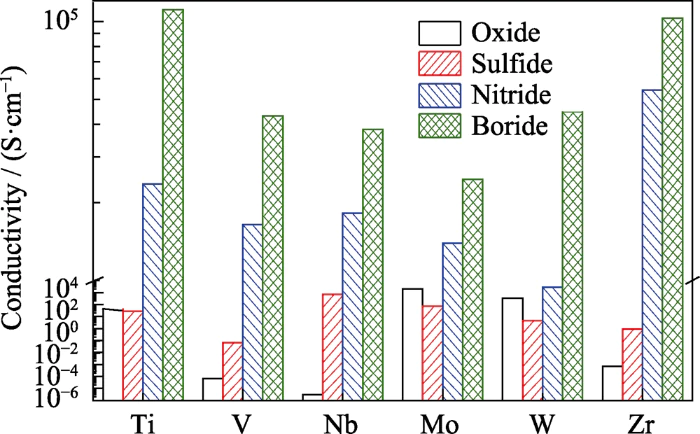
Abb. 4 Leitfähigkeitsvergleich mit mehreren Kategorien von Metall Verbindungen[48,49,50,51, 52,53,54,55,56]
Guan et al. [61] stellten ein Wirtsmaterial her für Schwefelkathoden durch Laden amorpher Co2B-Nanopartikel auf Graphen unter Verwendung von a Methode zur Reduktion der flüssigen Phase. Studien haben ergeben, dass sowohl Bor als auch Kobalt enthalten sind können dabei als Adsorptionsstellen zur chemischen Verankerung von Lithiumpolysulfid dienen Hemmung seiner Auflösung und Migration. Gepaart mit der hervorragenden Fernreichweite Aufgrund der Leitfähigkeit von Graphen verfügt die Batterie immer noch über eine entladungsspezifische Kapazität von 758 mAh·g-1 nach 450 Zyklen bei 1C Rate und die Kapazitätsabfallrate pro Der Zyklus beträgt 0,029 %, was eine hervorragende Zyklusleistung zeigt. Basierend auf einem ähnlichen synergistischer Adsorptionseffekt, das Co2B@CNT-Verbundmaterial, das als verwendet wird funktioneller Separator für Lithium-Schwefel-Batterien, hat eine Adsorptionskapazität von Li2S6 bis zu 11,67 mgâm-2 [62], was möglich ist Blockieren Sie effektiv die Diffusion und das Eindringen von Polysulfiden und erreichen Sie die Ziel ist es, den Shuttle-Effekt zu unterdrücken. Auf dieser Grundlage haben Guan et al. [63] verwendete außerdem zweidimensionales Metallcarbid (MXene) als Träger zur Herstellung von a Co2B@MXene-Heteroübergangs-Verbundmaterial (Abbildung 5(a~d)). Durch Durch theoretische Berechnungen wurde festgestellt, dass die elektronische Wechselwirkung an der Die Heteroübergangsschnittstelle führt zur Übertragung von Elektronen von Co2B auf MXene. Dieser Effekt verbessert die Adsorptions- und Katalysefähigkeit von Co2B Polysulfide (Abbildung 5(a, b)). Daher ist die Kapazitätsschwundrate des Batterie basierend auf Co2B@MXene funktionell modifiziertem Separator während 2000 Zyklen beträgt nur 0,0088 % pro Zyklus. Und bei einer Schwefelbeladung von 5,1 mgâcm-2 liegt die spezifische Kapazität immer noch bei 5,2 mAhâcm-2 (Abbildung 5(c, d)). Es ist zu beachten, dass im Vergleich zu kristalline Phasenstrukturen, diese Art von amorpher Phase Metallborid Materialien ist schonender und einfacher in der Materialaufbereitung. Allerdings ist die Kontrollierbarkeit und Stabilität seiner atomaren und molekularen Struktur sind relativ schlecht, was ein großes Hindernis für die Klärung seiner Komponenten darstellt Mikrostruktur und Erforschung ihres Einflussmechanismus auf den Schwefel elektrochemischer Reaktionsprozess.
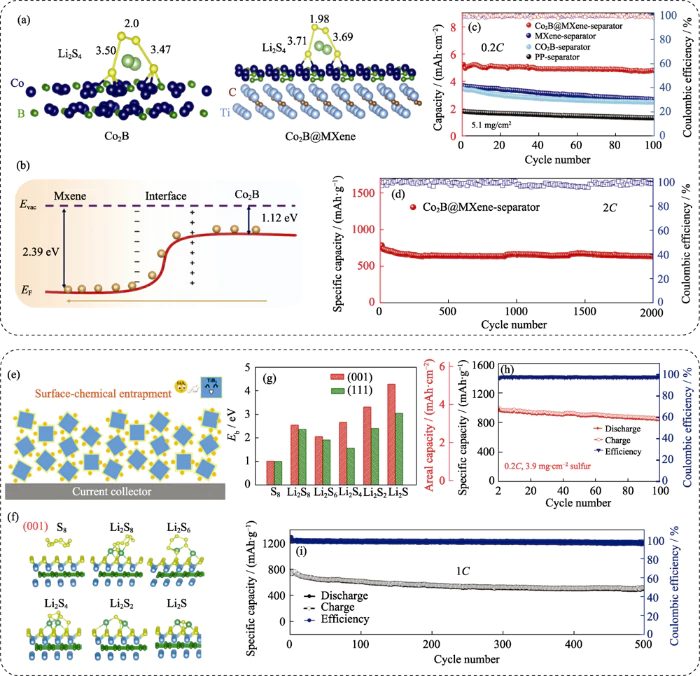
Abb. 5 (a) Li2S4-Adsorptionskonfigurationen Co2B- und Co2B@MXen-Oberflächen, (b) Schema der Elektronenumverteilung an der Schnittstellen zwischen Co2B und MXene, (c) Zyklenleistung von Zellen basierend auf Co2B@MXene und anderen Separatoren, (d) langfristige Zyklenleistung der Co2B@MXene-Zelle[63]; (e) schematische Darstellung des oberflächenchemischen Einschlusses von Polysulfide auf TiB2, (f) Adsorptionskonfigurationen und (g) Energien der Schwefelspezies auf (001)- und (111)-Oberflächen von TiB2, (h) Hochladeleistung und (i) Langzeitzyklen der auf TiB2 basierenden Schwefelelektrode[63,65]
TiB2 ist ein klassisches Metallborid mit ausgezeichnete elektrische Leitfähigkeit (~106 Sâcm-1) und wird häufig in verwendet Bereichen wie leitfähige Keramik, Präzisionsbearbeitung und Elektrochemie Geräte. TiB2 hat eine typische hexagonale Struktur und weist eine hohe Härte auf Strukturelastizität, die zur Anpassung an die Volumenänderung der Schwefelreaktion beiträgt. Gleichzeitig ist die große Anzahl ungesättigter Strukturen auf seiner Oberfläche vorhanden Es wird erwartet, dass eine starke chemische Grenzflächenwechselwirkung mit Lithium entsteht Polysulfid [64], wodurch gute Adsorptions- und Einschlusseffekte erzielt werden. Li et al. [65] berichteten erstmals, dass TiB2 als Wirtsmaterial für Schwefel verwendet wurde Kathoden. Wie in Abbildung 5 (z. B.) während des thermischen Compoundierungsprozesses gezeigt mit S ist die Oberfläche von TiB2 teilweise geschwefelt. Das Lithiumpolysulfid Während der Reaktion entsteht, wird durch Van-der-Waals effektiv adsorbiert Kräfte und Lewis-Säure-Base-Wechselwirkungen, und die Wirkung dieses Mechanismus ist auf der (001)-Oberfläche signifikanter. Die erhaltene Schwefelkathode erhielt a stabiler Zyklus von 500 Zyklen bei 1C-Rate und gleichzeitig die spezifische Die Kapazität beträgt nach 100 Zyklen bei a immer noch 3,3 mAhâcm-2 Schwefelbeladung von 3,9 mgâcm-2. hat sich gut gezeigt elektrochemische Leistung (Abbildung 5(h, i)). Basierend auf den Ergebnissen von XPS Analyse und theoretische Berechnungen, das ausgezeichnete Lithiumpolysulfid Der Adsorptionseffekt von TiB2 ist auf seine Oberfläche zurückzuführen „Passivierungs“-Mechanismus. Darüber hinaus hat Lus Forschungsgruppe [66] verglichen die Adsorptionseffekte von TiB2, TiC und TiO2 auf Lithiumpolysulfid und erforschte den Konkurrenzmechanismus zwischen der entsprechenden Chemikalie Adsorption und Solvatationsdesorption. Die Ergebnisse zeigen, dass Bor mit niedrigerem Die Elektronegativität sorgt dafür, dass TiB2 eine stärkere Adsorptionskapazität aufweist und kombiniert Mit Etherelektrolyt mit schwacher Solvatisierungskapazität kann es effektiv verbessert werden Schwefelnutzung und verbessern die Reversibilität elektrochemischer Reaktionen. Aus diesem Grund wurde TiB2 auch zur Konstruktion multifunktionaler Werkstoffe verwendet Separatoren [67], die Wirkstoffe effizient adsorbieren, verankern und wiederverwenden Materialien, wodurch die Zyklenstabilität der Batterie deutlich verbessert wird. Die Kapazität kann nach 300 Zyklen bei 0,5 °C 85 % des Ausgangswerts beibehalten.
Ähnlich wie TiB2 hat MoB eine gute Leitfähigkeit, und seine intrinsische zweidimensionale Struktur trägt dazu bei, das vollständig freizulegen Adsorptionsstellen und soll ein guter Schwefelkathodenkatalysator werden [68]. Die Manthiram-Forschungsgruppe an der University of Texas in Austin [69] verwendeten Sn als Reduktionsmittel und synthetisierten MoB-Nanopartikel durch a Festphasenmethode, die gute Adsorptions- und Katalysefähigkeiten zeigte Lithiumpolysulfid. MoB hat eine hohe elektronische Leitfähigkeit (1,7×105 Sâm-1), was eine schnelle Elektronenversorgung für Schwefel ermöglichen kann Reaktionen; Gleichzeitig werden die hydrophilen Oberflächeneigenschaften von MoB verbessert Fördert die Benetzung des Elektrolyten und unterstützt den schnellen Transport von Lithiumionen. Dies gewährleistet die Ausnutzung aktiver Materialien unter magerem Elektrolyt Bedingungen; Darüber hinaus kann nanoskaliges MoB den katalytischen Wirkstoff vollständig freilegen Stellen, die durch elektronenarme Boratome induziert werden und dem Material ermöglichen sowohl ausgezeichnete intrinsische als auch scheinbare katalytische Aktivität. Basierend auf diesen Vorteilen, selbst wenn MoB in einer kleinen Menge hinzugefügt wird, kann es die Leistung deutlich verbessern elektrochemische Leistung und weisen eine beträchtliche Praktikabilität auf. Das Ergebnis Der Akku hat nach 1.000 Zyklen einen Kapazitätsverlust von nur 0,03 % pro Zyklus im 1C-Tarif. Und bei einer Schwefelbelastung von 3,5 mgâcm-2 und ein Elektrolyt/Schwefel-Verhältnis (E/S) von 4,5 mLâg-1, Es wurde eine hervorragende Zyklusleistung der Soft-Package-Batterie erreicht. Darüber hinaus ist die Die Nazar-Forschungsgruppe [70] verwendete leichtes MgB2 als Elektrochemikalie Umwandlungsmedium für Lithiumpolysulfid. Es wurde festgestellt, dass sowohl B als auch Mg dies können dienen als Adsorptionsstellen für Polysulfid-Anionen, verstärken den Elektronentransfer, und erreichen eine bessere Zyklenstabilität bei hoher Schwefelbeladung (9,3 mg cm-2).
Diese Werke veranschaulichen dies vollständig Wirksamkeit und Überlegenheit von Metallboriden bei der Verbesserung von Schwefel Elektrochemische Reaktionen. Allerdings im Vergleich zu Systemen wie Metalloxiden und Sulfide gibt es noch relativ wenige Forschungsberichte zu Metallboriden in Lithium-Schwefel-Batterien sowie Forschung zu Materialien und zugehörigen Mechanismen muss ebenfalls ausgebaut und vertieft werden. Darüber hinaus kristalline Metallboride haben in der Regel eine hohe strukturelle Festigkeit, und der Herstellungsprozess erfordert Überwindung hoher Energiebarrieren und Einbeziehung hoher Temperaturen, hoher Drücke usw andere raue Bedingungen, was ihre Forschung und Anwendung einschränkt. Daher, die Entwicklung einfacher, milder und effizienter Metallborid-Synthesemethoden ist auch eine wichtige Richtung in der Metallboridforschung.
2.4 Nichtmetallboride
Im Vergleich zu Metallboriden, Nichtmetall Boride sind normalerweise weniger dicht und leichter, was für sie von Vorteil ist Entwicklung von Batterien mit hoher Energiedichte; jedoch ihre geringere Leitfähigkeit Erzeugt Widerstand gegen die Effizienz und Kinetik von elektrochemischem Schwefel Reaktionen. Derzeit haben Forscher beim Bau gewisse Fortschritte gemacht Schwefelfixierende Materialien für Lithium-Schwefel-Batterien auf Basis von Nichtmetallboriden einschließlich Bornitrid, Borcarbid, Borphosphid und Borsulfid [71, 72, 73].
Bornitrid (BN) und Borcarbid (BC) sind die beiden repräsentativsten und am häufigsten untersuchten Nichtmetallboride. BN ist besteht hauptsächlich aus abwechselnd verbundenen Stickstoffatomen und Boratomen umfasst vier Kristallformen: hexagonal, trigonal, kubisch und Leurit [74]. Unter In ihnen weist hexagonales Bornitrid (h-BN) Eigenschaften wie Breite auf Bandlücke, hohe Wärmeleitfähigkeit und gute thermische und chemische Stabilität bedingt zu seiner graphitähnlichen zweidimensionalen Struktur und lokalisierten elektronischen Polarisation Eigenschaften [75,76] . Die B-N-Struktur weist offensichtliche polare Eigenschaften auf und verfügt über eine starke chemische Adsorptionskapazität für Lithiumpolysulfid. Am Gleichzeitig können die chemischen Eigenschaften der Oberfläche dadurch gesteuert werden Elementdotierung und topologische Defektkonstruktion, um die Stabilität von zu gewährleisten die Molekularstruktur des Polysulfids und verbessert gleichzeitig seine Adsorptionsstärke [77]. Basierend auf dieser Idee haben Yi et al. [78] berichteten über eine stickstoffarme Wenigschicht Bornitrid (v-BN) als Wirtsmaterial für Schwefelkathoden (Abbildung 6(a)). Studien haben ergeben, dass die elektropositiven Leerstellen in v-BN nicht nur dazu beitragen nicht nur die Polysulfide fixieren und umwandeln, sondern auch die Diffusion und Migration beschleunigen von Lithium-Ionen. Im Vergleich zu Original-BN hat die v-BN-basierte Kathode eine höhere Anfangskapazität bei 0,1 °C (1262 vs. 775 mAhâg-1) und die Kapazität Die Zerfallsrate nach 500 Zyklen bei 1 °C beträgt nur 0,084 % pro Zyklus. Zeigt Gutes Fahrradstabilität. Darüber hinaus haben He et al. [79] fanden heraus, dass O-Dotierung weitere Auswirkungen haben kann Verbessern Sie die chemische Polarität der BN-Oberfläche und veranlassen Sie das Material zur Bildung von a größere spezifische Oberfläche und verbessern gleichzeitig die intrinsische und scheinbare Adsorptionseigenschaften.
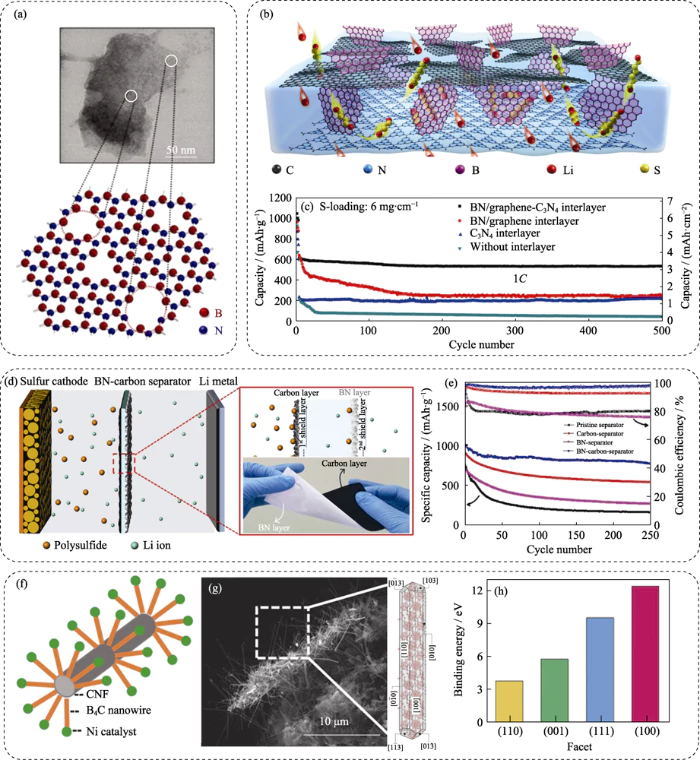
Abb. 6 (a) TEM-Bild und schematische Atomstruktur von v-BN[78]; (b) Schema des g-C3N4/BN/Graphen-Verbundionensiebs und (c) die entsprechende Li-S-Zellzyklusleistung[80]; (d) Schematisches und optisches Bild des dreischichtigen BN/Celgard/Kohlenstoff-Separators, und (e) die entsprechende Zellzyklusleistung[83]; (f) Schema und (g) SEM-Bild von B4C@CNF und dem Modell des B4C-Nanodrahts, (h) Li2S4-Adsorptionsenergien verschiedene Facetten von B4C[87]
Obwohl BN-Material gute chemische Eigenschaften aufweist Adsorptionseigenschaften, seine eigene schlechte Leitfähigkeit ist nicht förderlich für reaktive Ladungsübertragung. Daher ist die Gestaltung von Verbundstrukturen mit leitfähigen Materialien ist ein wichtiger Weg, ihre umfassende Adsorption weiter zu verbessern und katalytische Leistung. Vor diesem Hintergrund haben Deng et al. [80] entwarf a Komposit-Ionensieb auf Basis von graphitähnlichem Kohlenstoffnitrid (g-C3N4), BN und Graphen als multifunktionale Zwischenschicht für Lithium-Schwefel-Batterien (Abbildung 6(b)). Darunter die 0,3 nm großen geordneten Ionenkanäle im g-C3N4 Die Struktur kann Polysulfide effektiv blockieren und Lithiumionen passieren lassen durch. BN dient als Reaktionskatalysator zur Förderung der Umwandlung Polysulfide und Graphen dienen als eingebauter Stromkollektor ausgezeichnete Fernleitfähigkeit. . Dank der synergistischen Wirkung dieser Drei zweidimensionale Komponenten, die resultierende Batterie kann stabil zyklisch betrieben werden mehr als 500 Zyklen bei einer hohen Schwefelbeladung von 6 mgâcm-2 und einer Rate von 1C (Abbildung 6(c)). Darüber hinaus haben Forscher versucht, eine dünne Schicht aus BN-Nanoblatt/Graphen-Verbundfilm darauf aufzutragen Oberfläche der Kathode als Schutzschicht in einer einfacheren und direkteren Form [81,82]. Es hemmt wirksam die Auflösung und Diffusion von Lithium Polysulfid und verbessert die spezifische Kapazität und den Zyklus erheblich Stabilität der Schwefelkathode. Während 1000 Zyklen bei 3C beträgt die Kapazität Die Dämpfungsrate beträgt nur 0,0037 % pro Zyklus. Interessanterweise der Ungyu Paik Eine Forschungsgruppe an der Hanyang-Universität [83] übernahm eine andere Kombination von Ideen einen multifunktionalen Separator mit einem BN/Celgard/Kohlenstoff-Sandwich zu konstruieren Struktur. Wie in Abbildung 6(d) gezeigt, sind die kohlenstoffhaltige Schicht und die BN-Schicht jeweils auf der positiven und negativen Elektrodenseite des beschichtet gewöhnlicher Separator. Darunter können die Kohlenstoffschicht und die BN-Schicht gemeinsam sein blockieren den Transport von Lithiumpolysulfid und begrenzen dessen Diffusion an die Oberfläche der negativen Elektrode. Gleichzeitig liegt die BN-Schicht auf dem Negativ Die Elektrodenseite begrenzt auch das Wachstum von Lithiumdendriten. Dank dessen Durch den kooperativen Schutzmechanismus verfügt der Akku über eine hohe Kapazitätserhaltung Rate (76,6 %) und spezifische Kapazität (780,7 mAhâg-1) nach 250 Zyklen bei 0,5C. Deutlich besser als gewöhnliche Separatoren und Reinkohlenstoffmodifizierte Separatoren (Abbildung 6(e)).
Im Vergleich zu N hat C einen geringeren Elektronegativität, also der Elektronegativitätsunterschied zwischen B und C klein, was zu einer schwächeren chemischen Polarität der B-C-Struktur im Vergleich zu führt N-C. Gleichzeitig erfolgt aber auch die Elektronendelokalisierung in der B-C-Struktur verbessert und die Leitfähigkeit ist besser [84,85]. Daher zeigt BC im Allgemeinen relativ komplementäre physikalische und chemische Eigenschaften zu BN. Es ist niedrig Dichte, relativ gute Leitfähigkeit und gute katalytische Eigenschaften und hat vielversprechende Anwendungsaussichten im Energiebereich [86]. Luo et al. [87] wuchs Borcarbid-Nanodrähte (B4C@CNF) in situ auf Kohlenstofffasern als Kathodenwirt Material (Abbildung 6(f~h)). Unter ihnen adsorbiert und bindet B4C effizient Polysulfide durch B-S-Bindung. Gleichzeitig ist seine Kohlefaser leitfähig Das Netzwerk trägt zur schnellen Umwandlung des adsorbierten Schwefels bei und verbessert die Reaktion Kinetik. Die erhaltene Schwefelkathode weist eine Kapazitätserhaltung von 80 % nach 500 auf Zyklen und können stabile Zyklen bei hohem Schwefelgehalt (Massenanteil) erreichen 70 %) und Beladungskapazität (10,3 mgâcm-2). Lied et al. [88] konstruierte eine super-begrenzte Schwefelwirtsstruktur um B4C. Die Struktur verwendet aktivierten porösen Baumwollkohlenstoff als flexible Matrix, B4C Nanofasern als aktives Gerüst und reduziertes Graphenoxid für weitere Beschichtung. Kombiniert effizient physikalische und chemische Eingrenzung und lindert die Verlust an Wirkstoffen und erreicht eine hervorragende Zyklenstabilität. Im Hinblick auf die guten Adsorptions- und katalytischen Eigenschaften von B4C, Zhaos Forschungsgruppe [89] gleichmäßig verteilte B4C-Nanopartikel in Kohlefasergewebe durch eine katalytisch unterstützte In-situ-Wachstumsmethode zur effizienten Dispergierung und Belichtung aktive Websites. Die erhaltene Schwefelkathode hat eine Anfangskapazität von bis zu 1415 mAhâg-1 (0,1C) bei einer Beladung von 3,0 mgâcm-2 und eine extrem lange Lebensdauer von 3000 Zyklen bei 1 °C, was gute Anwendungsaussichten zeigt.
Das ist aus dem oben Gesagten ersichtlich Nichtmetallisches Borid hat eine gute Adsorption und katalytische Wirkung auf Lithium Polysulfid, aber seine Leitfähigkeit ist relativ gering und ein leitfähiger Träger wird noch benötigt, um die elektrochemische Schwefelreaktion zu unterstützen. Unter ihnen sind die Der Unterschied in der elektronischen Struktur benachbarter N- und C-Atome macht BN und BC-Materialien haben ihre eigenen Vor- und Nachteile Leitfähigkeit und Wechselwirkung mit Lithiumpolysulfid. In Anbetracht dessen, In Kombination mit Borsulfid, Borphosphid, Boroxid usw. ist diese Art von Nichtmetallisches Borid kann als guter Träger und Plattform für die Untersuchung verwendet werden Struktur-Aktivitäts-Beziehung zwischen lokaler chemischer Polarstruktur und Adsorptionskatalytische Fähigkeit. Es wird erwartet, dass weitere systematische Korrelation und Analyse helfen dabei, die relevante mikroskopische Reaktion zu verstehen Prozesse, regulieren die Feinstruktur von Materialien und verbessern die Elektrochemische Leistung von Batterien. Darüber hinaus die weitere Anwendung und die Entwicklung von Nichtmetallboriden in Lithium-Schwefel-Batterien muss noch erfolgen setzen auf die Verbesserung und Optimierung ihrer Vorbereitung. Einfach entwickeln und milde Aufbereitungstechnologien, während Materialstrukturen mit entwickelt werden höhere Eigenleitfähigkeit und Entwicklung effizienterer Verbundwerkstoffe um Leitfähigkeit, Adsorption und Katalyse auszugleichen und zu berücksichtigen Effekte.
3 Fazit
Zusammenfassend lässt sich sagen, dass Lithium-Schwefel-Batterien hohe theoretische Energiedichte aufgrund ihrer Mehrelektronentransferreaktionen. Ihr Umwandlungsreaktionsmechanismus und die intrinsische Reaktion sind jedoch schwach Leitfähigkeit der aktiven Materialien behindern die Realisierung der Vorteile. Materialien auf Borbasis haben einzigartige physikalische und chemische Eigenschaften Elektrochemische Eigenschaften. Ihre gezielte Gestaltung und rationelle Anwendung zeichnen sich aus wirksame Möglichkeiten zur Linderung des Shuttle-Effekts von Lithium-Schwefel-Batterien und Verbesserung der Reaktionskinetik und Reversibilität. Sie haben sich rasant entwickelt letzten Jahren. Die Erforschung und Anwendung borbasierter Materialien in Lithium-Schwefel-Batterien stecken noch in den Kinderschuhen, und die Materialstruktur Design und sein Wirkungsmechanismus auf die elektrochemische Reaktion der Batterie Der Prozess muss weiterentwickelt und erforscht werden. Kombinieren des Materials Merkmale und der oben genannte Forschungsfortschritt ist der Autor der Ansicht, dass die Die zukünftige Entwicklung borbasierter Materialien in Lithium-Schwefel-Batterien sollte dies tun Achten Sie besonders auf die folgenden Anweisungen:
1) Materialsynthese. Synthetik Die Herstellung ist ein häufiges Problem bei den oben genannten Produkten auf Borbasis Materialien. Es besteht ein dringender Bedarf, einfacher, milder und mehr zu entwickeln effiziente Materialvorbereitungsmethoden, um eine materielle Grundlage für Mechanismen bereitzustellen Forschungs- und Anwendungsförderung. Darunter die Herstellung von amorphem Metallboride durch die Flüssigphasenreduktionsmethode ist eine vielversprechende Entwicklung Richtung. Gleichzeitig nutzt es seine Vorteile und Erfahrungen, Erforschung und Entwicklung von Synthesewegen auf der Basis von Solvothermal- oder geschmolzenem Salz Methoden können auch neue Ideen für die Herstellung von borbasierten Verbindungen liefern Materialien. Darüber hinaus ist während des Herstellungsprozesses von Borid etwas Besonderes erforderlich Der Kontrolle und dem Design von Nanostrukturen und ihren Eigenschaften muss besondere Aufmerksamkeit gewidmet werden Stabilität, um die Anforderungen der Grenzflächenreaktionseigenschaften zu erfüllen Lithium-Schwefel-Batterien.
2) Erforschung des Mechanismus. Auf Borbasis Materialien verfügen über einzigartige und reichhaltige chemische Oberflächeneigenschaften. Vor Ort Charakterisierungsmethoden sollten verwendet werden, um den Wirt-Gast weiter zu untersuchen Wechselwirkungen zwischen borbasierten Materialien und Polysulfiden. Besondere Aufmerksamkeit Es sollte auf die irreversible Sulfatierung der Oberfläche geachtet werden, selbstelektrochemisch Oxidation und Reduktion usw., um die entscheidenden Strukturfaktoren davon aufzudecken Adsorptions- und katalytische Fähigkeiten sowie die Bereitstellung theoretischer Anleitungen und Grundlage für eine gezielte Gestaltung und Entwicklung von Materialien. Darüber hinaus für die Für repräsentative amorphe Metallboride ist eine Sonderzahlung erforderlich Aufmerksamkeit auf die Unterschiede in der Mikrostruktur und den damit verbundenen physikalischen und chemische Eigenschaften zwischen amorphen und kristallinen Boriden und kooperieren mit der Entwicklung entsprechender Statik und Liegenschaften Charakterisierungsanalysetechnologien. Vermeiden Sie es, auf die Interaktion zwischen ihnen zu schließen amorphe Materialien, Lithiumpolysulfid und sein Reaktionsprozess basieren ausschließlich darauf auf der Kristallstruktur.
3) Leistungsbewertung. Zur Optimierung der Material- und Batteriebewertungssystem bei gleichzeitiger Vergrößerung der Schwefeloberfläche Beim Laden sollte der Regulierung wichtiger Parameter wie z. B. mehr Aufmerksamkeit geschenkt werden Dicke und Porosität der Elektrode, um gleichzeitig die Qualität zu verbessern und volumetrische Energiedichte der Elektrode. Darüber hinaus ist die Die elektrochemischen Eigenschaften unter Bedingungen niedriger Elektrolytdosierung (E/S<5 mLâg-1S) und niedrigem negativem/positivem Elektrodenkapazitätsverhältnis (N/P<2) wurden weiter untersucht. Gleichzeitig untersuchen wir den Verstärkungseffekt und damit verbundene wissenschaftliche und technische Fragen von Laborknopfzellen bis hin zur tatsächlichen Produktion zylindrischer oder flexibler Verpackungsbatterien und nehmen eine vernünftige und umfassende Bewertung der Leistungswettbewerbsfähigkeit der Batterieebene vor. Bereitstellung von Leitlinien und Referenzen für die kommerzielle Entwicklung von Lithium-Schwefel-Batterien.
Zusammenfassend konzentriert sich dieser Artikel auf Materialien auf Borbasis und gibt einen Überblick über die neuesten Forschungsfortschritte zu Borophen. Mit Boratomen dotierter Kohlenstoff, Metallboride und Nichtmetallboride in Lithium-Schwefel Batteriesysteme. Ich hoffe, es kann Kollegen als Referenz und Inspiration dienen, Erweiterung der Entwicklung und Anwendung borbasierter Materialien im Bereich neue Energie und fördern die praktische Entwicklung von Lithium-Schwefel-Batterien.
Referenzen
[1] DUNN B, KAMATH H, TARASCON J M. Elektrische Energiespeicherung für das Netz: eine Batterie voller Möglichkeiten. Wissenschaft, 2011,334(6058):928-935.
[2] ARICO A S, BRUCE P, SCROSATI B, et al. Nanostrukturierte Materialien für fortschrittliche Energieumwandlungs- und Speichergeräte. Nature Materials, 2005,4(5):366-377.
[3] LIANG YR, ZHAO CZ, YUAN H, et al. A Überprüfung von wiederaufladbaren Batterien für tragbare elektronische Geräte. InfoMat, 2019,1(1):6-32.
[4] GOODENOUGH J B, PARK K S. Das Li-Ion wiederaufladbare Batterie: eine Perspektive. Zeitschrift der American Chemical Society, 2013,135(4):1167-1176.
[5] TARASCON J M, ARMAND M. Probleme und Herausforderungen für wiederaufladbare Lithiumbatterien. Nature, 2011,414:171-179.
[6] JIN G Y, HE H C, WU J, et al. Kobaltdotiertes hohles Kohlenstoffgerüst als Schwefelwirt für die Lithiumkathode Schwefelbatterie. Journal of Inorganic Materials, 2021,36(2):203-209.
[7] FANG R, ZHAO S Y, SUN ZH, et al. Mehr Zuverlässige Lithium-Schwefel-Batterien: Tatus, Lösungen und Perspektiven. Fortschrittlich Materialien, 2017,29(48):1606823.
[8] HU J J, LI G R, GAO X P. Aktuell Status, Probleme und Herausforderungen bei Lithium-Schwefel-Batterien. Zeitschrift für Inorganic Materials, 2013,28(11):1181-1186.
[9] LI G R, WANG S, ZHANG YN, et al. Überprüfung der Rolle von Polysulfiden in Lithium-Schwefel-Batterien. Fortschrittlich Materialien, 2018,30(22):1705590.
[10] PENG HJ, HUANG J Q, ZHANG Q. Eine Rezension aus flexiblem wiederaufladbarem Lithium-Schwefel- und analogem Alkalimetall-Chalkogen Batterien. Chemical Society Reviews, 2017,46(17):5237-5288.
[11] JANA M, XUR, CHENG XB, et al. Rationales Design zweidimensionaler Nanomaterialien für Lithium-Schwefel-Batterien. Energy & Environmental Science, 2020,13(4):1049-1075.
[12] HE J R, MANTHIRAM A. Eine Rezension zum Status und Herausforderungen von Elektrokatalysatoren in Lithium-Schwefel-Batterien. Energie Speichermaterialien, 2019,20:55-70.
[13] SEH ZW, SUN YM, ZHANG QF, et al. Entwicklung hochenergetischer Lithium-Schwefel-Batterien. Bewertungen der Chemical Society, 2016,45(20):5605-5634.
[14] JI X L, EVERS S, BLACK R, et al. Stabilisierung von Lithium-Schwefel-Kathoden mithilfe von Polysulfid-Reservoirs. Natur Kommunikation, 2011,2:325.
[15] ZHANG Z, KONG L L, LIU S, et al. A Hocheffizienter Schwefel-Kohlenstoff-Verbundstoff auf Basis von 3D-Graphen-Nanoblättern@Kohlenstoff Nanoröhrenmatrix als Kathode für Lithium-Schwefel-Batterie. Fortschrittliche Energie Materialien, 2017,7(11):1602543.
[16] XU W C, PAN X X, MENG X, et al. A leitfähiges Schwefel enthaltendes Material mit ultrafeinem Vanadiumnitrid Nanopartikel für Hochleistungs-Lithium-Schwefel-Batterien. Electrochimica Acta, 2020,331:135287.
[17] LIU Y T, LIU S, LI G R, et al. Hoch volumetrische Energiedichte-Schwefelkathode mit schwerem und katalytischem Metalloxid Host für Lithium-Schwefel-Batterie. Advanced Science, 2020,7(12):1903693.
[18] CHEN HH, XIAO YW, CHEN C, et al. Leitfähiger MOF-modifizierter Separator zur Abschwächung des Shuttle-Effekts von Lithium- Schwefelbatterie durch eine Filtrationsmethode. ACS Angewandte Materialien & Schnittstellen, 2019,11(12):11459-11465.
[19] YOO J, CHO S J, JUNG G Y, et al. COF-Netz auf CNT-Netz als molekular gestaltete, hierarchische poröse chemische Falle für Polysulfide in Lithium-Schwefel-Batterien. Nano-Buchstaben, 2016,16(5):3292-3300.
[20] HU Y, LIU C. Einführung von 1,2-Migration für Organoborverbindungen. Universitätschemie, 2019,34(12):39-44.
[21] SOREN K M, SUNING W. Borbasiert auf Reize reagierende Materialien. Chemical Society Reviews, 2019,48(13):3537-3549.
[22] HUANG Z G, WANG S N, DEWHURST R D, et al. Bor: seine Rolle in energiebezogenen Prozessen und Anwendungen. Angewandte Chemie International Edition, 2020,59(23):8800-8816.
[23] ZHU Y H, GAO S M, HOSMANE N S. Mit Bor angereicherte fortschrittliche Energiematerialien. Inorganica Chimica Acta, 2017,471:577-586.
[24]KHAN K, TAREEN A K, ASLAM M, et al. Synthese, Eigenschaften und neue elektrokatalytische Anwendungen der 2D-Borophen-Xene. Progress in Solid State Chemistry, 2020,59:100283.
[25] RAO DW, LIU XJ, YANG H, et al. Grenzflächenkonkurrenz zwischen einer Kathode auf Borophenbasis und einem Elektrolyten für die Mehrfachsulfid-Immobilisierung einer Lithium-Schwefel-Batterie. Zeitschrift für Materials Chemistry A, 2019,7(12):7092-7098.
[26] JIANG H. R., SHYY W., LIU M. et al. Borophen und defektes Borophen als potenzielle Verankerungsmaterialien für Lithium-Schwefel-Batterien: eine First-Principles-Studie. Zeitschrift für Materialien Chemie A, 2018,6(5):2107-2114.
[27] ZHANG C Y, HE Q, CHU W, et al. Mit Übergangsmetallen dotierte Borophen-Graphen-Heterostruktur für Robustheit Polysulfidverankerung: eine erste Grundsatzstudie. Angewandte Oberflächenwissenschaft, 2020,534:147575.
[28] ZHANG L, LIANG P, SHU HB, et al. Borophen als effiziente Schwefelwirte für Lithium-Schwefel-Batterien: Unterdrückung Shuttle-Effekt und Verbesserung der Leitfähigkeit. Journal of Physical Chemistry C, 2017,121(29):15549-15555.
[29] GRIXTI S, MUKHERJEE S, Singh C V. Zweidimensionales Bor als eindrucksvolle Kathode einer Lithium-Schwefel-Batterie Material. Energiespeichermaterialien, 2018, 13:80-87.
[30] MANNIX AJ, ZHOU XF, KIRALY B, et al. Synthese von Borophenen: anisotrope, zweidimensionale Borpolymorphe. Science, 2015,350(6267):1513-1516.
[31] FENG BJ, ZHANG J, ZHONG Q, et al. Experimentelle Realisierung zweidimensionaler Borschichten. Naturchemie, 2016,8(6):564-569.
[32] PARAKNOWITSCH J P, THOMAS A. Doping Kohlenstoffe jenseits von Stickstoff: Ein Überblick über fortgeschrittene Heteroatom-dotierte Kohlenstoffe mit Bor, Schwefel und Phosphor für Energieanwendungen. Energie & Environmental Science, 2013,6(10):2839-2855.
[33] WANG H B, MAIYALAGAN T, WANG X. Rezension über die jüngsten Fortschritte bei stickstoffdotiertem Graphen: Synthese, Charakterisierung und seine möglichen Anwendungen. ACS Catalysis, 2012,2(5):781-794.
[34] XIE Y, MENG Z, CAI TW, et al. Wirkung der Bordotierung des Graphen-Aerogels, das als Kathode für den Lithiumschwefel verwendet wird Batterie. ACS Applied Materials & Interfaces, 2015,7(45):25202-25210.
[35] SHI P C, WANG Y, LIANG X, et al. Gleichzeitig wurden mit Bor dotierte Graphenschichten abgeblättert, um Schwefel einzukapseln Anwendungen in Lithium-Schwefel-Batterien. ACS Nachhaltige Chemie & Ingenieurwesen, 2018,6(8):9661-9670.
[36] YANG L J, JIANG S J, ZHAO Y, et al. Bordotierte Kohlenstoffnanoröhren als metallfreie Elektrokatalysatoren für den Sauerstoff Reduktionsreaktion. Angewandte Chemie Internationale Ausgabe, 2011,50(31):7132-7135.
[37] AI W, LI J W, DU Z Z, et al. Dual Einschluss von Polysulfiden in einem mit Bor dotierten porösen Kohlenstoffkügelchen/Graphen-Hybrid für moderne Li-S-Batterien. Nanoforschung, 2018,11(9):4562-4573.
[38] YANG C P, YIN Y X, YE H, et al. Einblick in die Wirkung der Bor-Dotierung auf Schwefel-/Kohlenstoff-Kathoden in Lithium-Schwefel-Batterien. ACS Angewandte Materialien und Schnittstellen, 2014,6(11):8789-8795.
[39] XU C X, ZHOU H H, FU C P, et al. Hydrothermale Synthese von mit Bor dotierten, entpackten Kohlenstoffnanoröhren/Schwefel Verbundwerkstoff für Hochleistungs-Lithium-Schwefel-Batterien. Electrochimica Acta, 2017,232:156-163.
[40] HAN P, MANTHIRAM A. Bor- und Mit Stickstoff dotierte, mit reduziertem Graphenoxid beschichtete Separatoren für hohe Leistung Li-S-Batterien. Journal of Power Sources, 2017,369:87-94.
[41] HOU T Z, CHEN X, PENG H J, et al. Designprinzipien für Heteroatom-dotierten Nanokohlenstoff zur Erzielung einer starken Verankerung von Polysulfiden für Lithium-Schwefel-Batterien. Klein, 2016,12(24):3283-3291.
[42] XIONG DG, ZHANG Z, HUANG XY, et al. Verstärkung des Polysulfideinschlusses in B/N-kodotierten hierarchisch porösen Stoffen Kohlenstoffnanoblätter über Lewis-Säure-Base-Wechselwirkung für stabile Li-S-Batterien. Journal of Energy Chemistry, 2020,51:90-100.
[43] YUAN S Y, BAO J L, WANG LN, et al. Graphengestützte, stickstoff- und borreiche Kohlenstoffschicht zur Verbesserung Leistung von Lithium-Schwefel-Batterien aufgrund der verbesserten Chemisorption von Lithiumpolysulfide. Advanced Energy Materials, 2016,6(5):1501733.
[44] CHEN L, FENG JR, ZHOU HH, et al. Hydrothermale Herstellung von mit Stickstoff und Bor kodotiertem gebogenem Graphen Nanobänder mit hohen Dotierungsmengen für Hochleistungs-Lithiumschwefel Batteriekathoden. Journal of Materials Chemistry A, 2017,5(16):7403-7415.
[45] JIN C B, ZHANG W K, ZHUANG Z Z, et al. Verbesserte Sulfid-Chemisorption mit doppelt dotiertem mehrwandigem Bor und Sauerstoff Kohlenstoffnanoröhren für fortschrittliche Lithium-Schwefel-Batterien. Zeitschrift für Materialien Chemie A, 2017,5(2):632-640.
[46] ULLAH S, DENIS P A, SATO F. Ungewöhnlich Steigerung der Adsorptionsenergien von Natrium und Kalium Schwefel-Stickstoff- und Silizium-Bor-kodotiertes Graphen. ACS Omega, 2018,3(11):15821-15828.
[47] ZHANG Z, XIONG DG, SHAO AH, et al. Integration metallischer Kobalt- und N/B-Heteroatome in poröse Kohlenstoffnanoblätter als effiziente Schwefel-Wegfahrsperre für Lithium-Schwefel-Batterien. Kohlenstoff, 2020,167:918-929.
[48] WANG P, KUMAR R, SANKARAN E M, et al. Unter hohem Druck synthetisiertes Vanadiumdiborid (VB2): elastisch, mechanisch, elektronische und magnetische Eigenschaften und thermische Stabilität. Anorganische Chemie, 2018,57(3):1096-1105.
[49] HE GJ, LING M, HAN XY, et al. Freistehende Elektroden mit Kern-Schale-Strukturen für hohe Leistung Superkondensatoren. Energiespeichermaterialien, 2017,9:119-125.
[50] WANG C C, AKBAR S A, CHEN W, et al. Elektrische Eigenschaften von Hochtemperaturoxiden, Boriden, Karbiden und Nitride. Journal of Materials Science, 1995,30(7):1627-1641.
[51] XIAO Z B, YANG Z, ZHANG L J, et al. NbS2@S@I-dotiertes Graphen vom Sandwich-Typ für hochschwefelbeladene, ultraschnelle, und langlebige Lithium-Schwefel-Batterien. ACS Nano, 2017,11(8):8488-8498.
[52] WANG LJ, LIU FH, ZHAO BY, et al. Mit MoS2-Nanoblättern gefüllte Kohlenstoff-Nanoschalen als Elektrodenmaterialien für Superkondensatoren. ACS Applied Nano Materials, 2020,3(7):6448-6459.
[53] BALACH J, LINNEMANN J, JAUMANN T, et al. Metallbasierte nanostrukturierte Materialien für fortschrittliche Lithium-Schwefel-Batterien. Journal of Materials Chemistry A, 2018,6(46):23127-23168.
[54] BEN-DOR L, SHIMONY Y. Kristall Struktur, magnetische Suszeptibilität und elektrische Leitfähigkeit von reinem und NiO-dotiertes MoO2 und WO2. Materials Research Bulletin, 1974,9(6):837-44.
[55] SAMSONOV G. é¾çååç©æå. å京:ä¸å½å·¥ä¸åºç社, 1965: 1-147.
[56] FENG L S, QUN C X, LIN M Y, et al. Nb-basierte Oxide als Anodenmaterialien für Lithium-Ionen-Batterien. Fortschritte in Chemie, 2015,27(2/3):297-309.
[57] TAO Q, MA S L, CUI T, et al. Strukturen und Eigenschaften funktioneller Übergangsmetallboride. Acta Physica Sinica, 2017,66(3):036103.
[58] SHEN Y F, XU C, HUANG M, et al. Forschungsfortschritte bei Borclustern, Boran und metalldotierten Borverbindungen. Progress in Chemistry, 2016,28(11):1601-1614.
[59] GUPTA S, PATEL M K, MIOTELLO A, et al. Katalysatoren auf Metallboridbasis für die elektrochemische Wasserspaltung: ein Überblick. Advanced Functional Materials, 2020,30(1):1906481.
[60] WU F, WU C. Neue Sekundärbatterien und ihre Schlüsselmaterialien basierend auf dem Konzept der Mehrelektronenreaktion. Chinese Science Bulletin, 2014,59(27):3369-3376.
[61] GUAN B, FAN L S, WU X, et al. Der einfache Synthese und verbesserte Leistung einer Lithium-Schwefel-Batterie amorphes Kobaltborid (Co2B)@Graphen-Verbundkathode. Zeitschrift für Materialien Chemie A, 2018,6(47):24045-24049.
[62] GUAN B, ZHANG Y, FAN L S, et al. Blockierung von Polysulfid mit Co2B@CNT durch „synergetischen Adsorptionseffekt“ in Richtung Ultrahochleistungsfähiger und robuster Lithium-Schwefel-Akku. ACS Nano, 2019,13(6):6742-6750.
[63] GUAN B, SUN X, ZHANG Y, et al. Der Entdeckung der elektronischen Grenzflächenwechselwirkung innerhalb von Kobaltborid@MXene für Hochleistungs-Lithium-Schwefel-Batterien. Chinesische chemische Buchstaben, 2020,32(7):2249-2253.
[64] BASU B, RAJU GSURI A. Verarbeitung und Eigenschaften monolithischer TiB2-basierter Materialien. Internationale Materialbewertungen, 2006,51(6):352-374.
[65] LI C C, LIU X B, ZHU L, et al. Leitfähiges und polares Titanborid als Schwefelwirt für Fortgeschrittene Lithium-Schwefel-Batterien. Chemistry of Materials, 2018,30(20):6969-6977.
[66] LI Z J, JIANG H R, LAI N C, et al. Entwurf einer effektiven Lösungsmittel-Katalysator-Schnittstelle für die katalytische Schwefelumwandlung in Lithium-Schwefel-Batterien. Mistry of Materials, 2019,31(24):10186-10196.
[67] JIN L M, NI J, SHEN C, et al. Metallisch leitfähiges TiB2 als multifunktionaler Separatormodifikator für verbesserte Lithium-Schwefel-Batterien. Journal of Power Sources, 2020,448:227336.
[68] WU R, XU H K, ZHAO Y W, et al. Borophenähnliche Boruntereinheiten mit eingefügtem Molybdängerüst von MoB2 ermöglichen stabile und schnell reagierende Lithium-Schwefel-Batterien auf Li2S6-Basis. Energiespeicher Materialien, 2020,32:216-224.
[69] HE J R, BHARGAV A, MANTHIRAM A. Molybdänborid als effizienter Katalysator für die Polysulfid-Redoxaktivierung Lithium-Schwefel-Batterien mit hoher Energiedichte. Fortschrittliche Materialien, 2020,32(40):2004741.
[70] PANG Q, KWOK C Y, KUNDU D, et al. Leichtes metallisches MgB2 vermittelt Polysulfid-Redox und verspricht Lithium-Schwefel-Batterien mit hoher Energiedichte. Joule, 2019,3(1):136-148.
[71] YU T T, GAO P F, ZHANG Y, et al. Borphosphid-Monoschicht als potenzielles Ankermaterial für Lithium-Schwefel Batterien: eine First-Principles-Studie. Angewandte Oberflächenwissenschaft, 2019,486:281-286.
[72] JANA S, THOMAS S, LEE CH, et al. B3S Monoschicht: Vorhersage eines Hochleistungsanodenmaterials für Lithium-Ionen Batterien. Journal of Materials Chemistry A, 2019,7(20):12706-12712.
[73] SUN C, HAI C X, ZHOU Y, et al. Hoch Katalytische Bornitrid-Nanofaser, die in situ auf vorbehandeltem Ketjenblack gezüchtet wird Kathode für eine verbesserte Leistung von Lithium-Schwefel-Batterien. ACS angewendet Energiematerialien, 2020,3(11):10841-10853.
[74] ARENAL R, LOPEZ BEZANILLA A. Boron Nitridmaterialien: ein Überblick von 0D- bis 3D-(Nano-)Strukturen. Wiley Interdisziplinäre Rezensionen – Computational Molecular Science, 2015,5(4):299-309.
[75] JIANG XF, WENG QH, WANG XB, et al. Jüngste Fortschritte bei der Herstellung und Anwendung von Bornitrid Nanomaterialien: eine Rezension. Zeitschrift für Materialwissenschaft und Technologie, 2015,31(6):589-598.
[76] PRAKASH A, NEHATE S D, SUNDARAM K B. Metall-Isolator-Metall-UV-Detektoren auf Basis von Bornkohlenstoffnitrid für raue Umgebungen Umweltanwendungen. Optics Letters, 2016,41(18):4249-4252.
[77] ZHAO Y M, YANG L, ZHAO J X, et al. Wie um inerte Bornitrid-Nanoblätter für die Immobilisierung aktiv zu machen Polysulfide für Lithium-Schwefel-Batterien: eine rechnerische Studie. Körperlich Chemie Chemische Physik, 2017,19(28):18208-18216.
[78] YI YK, LI H P, CHANG H H, et al. Wenigschichtiges Bornitrid mit künstlichen Stickstoff-Leerstellen zur Förderung Umwandlung von Polysulfid als Kathodenmatrix für Lithium-Schwefel-Batterien. Chemie, 2019,25(34):8112-8117.
[79] HE B, LI W C, ZHANG Y, et al. Paragenese BN/CNTs-Hybrid als monokliner Schwefelwirt für hohe Raten und Lithium-Schwefel-Batterie mit extrem langer Lebensdauer. Zeitschrift für Materialchemie A, 2018,6(47):24194-24200.
[80] DENG D R, BAI C D, XUE F, et al. Multifunktionales Ionensieb aus 2D-Materialien als Zwischenschicht für Li-S Batterien. ACS Applied Materials & Interfaces, 2019,11(12):11474-11480.
[81] SUN K, GUO P Q, SHANG X N, et al. Mesoporöse, mit Bornkohlenstoffnitrid/Graphen modifizierte Separatoren als effizient Polysulfidbarriere für hochstabile Lithium-Schwefel-Batterien. Zeitschrift für Elektroanalytische Chemie, 2019,842:34-40.
[82] FAN Y, YANG Z, HUA W X, et al. Funktionalisierte Bornitrid-Nanoblätter/Graphen-Zwischenschicht für schnelle und langlebige Lithium-Schwefel-Batterien. Fortschrittliche Energiematerialien, 2017,7(13):1602380.
[83] KIM PJH, SEO J, FU K, et al. Synergistischer Schutzeffekt eines BN-Kohlenstoff-Separators für hohe Stabilität Lithium-Schwefel-Batterien. NPG Asia Materials, 2017,9(4):e375.
[84] PRAMANICK A, DEY P P, DAS P K. Mikrostruktur-, Phasen- und elektrische Leitfähigkeitsanalysen von Funkenplasma gesintertes Borkarbid, bearbeitet mit WEDM. Keramik International, 2020,46(3):2887-2894.
[85] YEGANEH M, SARAF HH, KAFI F, et al. Erste prinzipielle Untersuchung von Schwingungen, Elektronik und Optik Eigenschaften von graphenähnlichem Borcarbid. Festkörperkommunikation, 2020,305:113750.
[86] CHANG YK, SUN XH, MA MD, et al. Anwendung der harten Keramikmaterialien B4C in der Energiespeicherung: Design B4C@C Kern-Schale-Nanopartikel als Elektroden für flexible Festkörper-Mikropartikel Superkondensatoren mit ultrahoher Zyklenfestigkeit. Nanoenergie, 2020,75:104947.
[87] LUO L, CHUNG S H, ASL H Y, et al. Langlebige Lithium-Schwefel-Batterien mit bifunktionellem Kathodensubstrat konfiguriert mit Borcarbid-Nanodrähten. Fortschrittliche Materialien, 2018,30(39):1804149.
[88] SONG N N, GAO Z, ZHANG Y Y, et al. B4C Nanoskelett-fähige, flexible Lithium-Schwefel-Batterien. Nanoenergie, 2019,58:30-39.
[89] ZHANG RH, CHI C, WU M C, et al. A langlebiger Li-S-Akku mit einer Kathode aus gut verteiltem B4C Nanopartikel dekorierten aktivierte Baumwollfasern. Zeitschrift für Energiequellen, 2020,451:227751.



