Kategorien
neuer Blog
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
- Hauptursachen für Undichtigkeiten an der Zellversiegelung von Beuteln
- Formation und Grading in der Lithium-Ionen-Batterieherstellung
Tags
Jüngste Fortschritte bei der Anode für sulfidbasierte Festkörper-Lithiumbatterien
Jüngste Fortschritte bei Anode für Festkörper-Lithiumbatterien auf Sulfidbasis
ââ Teil 1 Lithium-Metallanode
Autor:
JIA Linan, DU Yibo, GUO Bangjun, ZHANG Xi
1. Schule of Mechanical Engineering, Shanghai Jiao Tong University, Shanghai 200241, China
2. Shanghai Yili New Energy Technology Co., LTD. , Shanghai 201306, China
Zusammenfassung
All-Solid-State-Lithiumbatterien (ASSLBs) weisen eine höhere Energiedichte auf und mehr Sicherheit als aktuelle flüssige Lithiumbatterien, die die wichtigsten sind Forschungsrichtung für Energiespeichergeräte der nächsten Generation. Gegenüber Andere Festkörperelektrolyte sind Sulfid-Festkörperelektrolyte (SSEs). die Eigenschaften von ultrahoher Ionenleitfähigkeit, geringer Härte, einfach Verarbeitung und guter Grenzflächenkontakt, die zu den vielversprechendsten gehören Wege zur Realisierung von Festkörperbatterien. Es gibt jedoch einige Grenzflächenprobleme zwischen Anoden und SSEs, die ihre Anwendungen einschränken, z B. Grenzflächennebenreaktionen, schlechter starrer Kontakt und Lithiumdendriten. Das Die Studie skizziert die aktuellen Fortschritte bei Anodenmaterialien für sulfidbasierte Anwendungen ASSLBs fassen den Entwicklungsstatus, Anwendungsvorteile und Schnittstellen zusammen Probleme und gängige Lösungsstrategien der wichtigsten Anodenmaterialien einschließlich Lithiummetall, Lithiumlegierungen, Siliziumanode für Sulfidbasis ASSLBs und liefert Leitvorschläge für die nächste Entwicklung von Anoden Materialien und die Lösung von Grenzflächenproblemen.
Schlüsselwörterï¼ All-Solid-State Lithiumbatterien ; Sulfidelektrolyt ; Lithiumanode ; Legierungsanode ; Anode/Elektrolyt Schnittstellen
Einführung
Lithium-Ionen-Batterien werden häufig verwendet Aufgrund ihrer hohen Spannung und hohen Energiedichte sind sie für verschiedene tragbare Geräte geeignet. Sie sind ein wichtiges Industrieprodukt für die Elektrifizierung von Fahrzeugen Einsatz von Energiespeichersystemen in einer kohlenstoffarmen Gesellschaft. Allerdings flüssig Lithium-Ionen-Batterien verwenden negative Graphitelektroden und organische Flüssigkeiten Elektrolyte und metallische Lithiumoxid-Positivelektroden (wie LiCoO2). Einerseits ist die spezifische Energie der zusammengebauten Batterien begrenzt Der Bereich liegt zwischen 200 und 250 W·h·kg-1, was es schwierig macht, weiter zu erreichen Durchbrüche in der spezifischen Energie. Auf der anderen Seite haben organische Elektrolyte Nachteile wie schlechte thermische Stabilität und Entflammbarkeit. Darüber hinaus ist die Auch Lithiumdendriten, die während des Batteriezyklus entstehen, bergen große Risiken Es kann zu einem Kurzschluss oder sogar einer Explosion der Batterie kommen. Diese Reihe von Problemen hat verursacht Viele Forscher achten auf die Sicherheit von Lithium-Ionen und denken darüber nach Batterien. Ersetzen brennbarer organischer Flüssigelektrolyte durch Feststoffe Elektrolyte können ein thermisches Durchgehen grundsätzlich verhindern und die Sicherheit lösen Gefahren durch brennbare flüssige Elektrolyte, die in flüssigen Lithium-Ionen-Akkus verwendet werden Batterien. Gleichzeitig sind die hohen mechanischen Eigenschaften solide Elektrolyte gelten auch als einer der Durchbrüche bei der Hemmung das Wachstum von Lithiumdendriten.
Derzeit der Mainstream-Festkörper Es gibt vier Arten von Elektrolyten: Sulfid-Festkörperelektrolyt und Oxid Festkörperelektrolyt, Polymer-Festkörperelektrolyt und Halogenid-Festkörperelektrolyt Elektrolyt. Unter diesen haben Oxidelektrolyte die Vorteile von gut Stabilität und mäßige Ionenleitfähigkeit, aber schlechter Grenzflächenkontakt. Polymerelektrolyte haben eine gute Stabilität gegenüber Lithiummetall und relativ ausgereifte Verarbeitungstechnologie, aber schlechte thermische Stabilität, schmal elektrochemische Fenster und eine geringe Ionenleitfähigkeit schränken den Anwendungsbereich ein Anwendung. Als neuer Elektrolyttyp haben sich Halogenidelektrolyte erhalten Aufgrund ihrer hohen Ionenleitfähigkeit erfreuen sie sich großer Beliebtheit. Allerdings ist das Hoch Valenzmetallelemente in Halogenidelektrolyten bestimmen, dass dies nicht möglich ist Kontaktieren Sie Lithiummetall direkt, um eine stabile Anodenschnittstelle zu bilden. Forschung zu Halogenidelektrolyte erfordern weitere Untersuchungen. Sulfidelektrolyte sind gilt als einer der vielversprechendsten Wege zur Realisierung von All-Solid-State Lithiumbatterien (ASSLBs) Elektrolyte aufgrund ihrer hohen Ionenleitfähigkeit, geringe Härte, einfache Verarbeitung, gute Formbarkeit und guter Grenzflächenkontakt.
In den letzten Jahren wurden entsprechende Forschungen zu Sulfid durchgeführt Elektrolyte wurden weiterentwickelt und ihre Ionenleitfähigkeit erreicht ein Niveau, das mit dem von flüssigen organischen Elektrolyten vergleichbar ist. Typisches Sulfid Zu den Elektrolyten gehören glasartiges Li-P-S-Sulfid (LPS) und abgeleitete Glaskeramiken. Silbersulfid-Germaniumerz (Li6PS5X, X=Cl, Br, I) und Lithiumsulfidion Supraleiter (Thio-Lithium-Superionenleiter, Thio-LISICONs), Li10GeP2S12 (LGPS) und ähnliche Verbindungen.
Unter diesen verschiedenen Sulfidmaterialien sind Elektrolyte vom LGPS-Typ weisen mit Abstand die beste Ionenleitfähigkeit auf. Im Jahr 2016, Kato et al. berichteten über den Superlithium-Ionenleiter Li9.54Si1.74P1.44S11.7Cl0.3 (LSPSCl), dessen Ionenleitfähigkeit bei Raum bis zu 25×10-2 S·cm-1 beträgt Temperatur. LGPS verfügt außerdem über eine ultrahohe Ionenleitfähigkeit von 1,2·10-2 S·cm-1 at Raumtemperatur. Die schwache anisotrope Ionenleitfähigkeit von einkristallinem LGPS in (001)-Richtung sogar 27Ã10-2 S·cm-1. Glaskeramik (Li7P3S11) und Sulfidgermanit (Li6PS5Cl) können hohe Ionenleitfähigkeiten von 10-3 erreichen S·cm-1. Festkörperbatterien, die Sulfidelektrolyte mit kombinieren Schichtkathoden mit hohem Nickelgehalt und Hochenergieanoden (z. B. Si oder Metall). Lithium) kann sogar eine ultrahohe spezifische Energie von 500 kW·h·kg-1 aufweisen. Jedoch, die Anwendung von Sulfidelektrolyten in Festkörper-Lithiumbatterien Hat immer noch Probleme wie schmales elektrochemisches Fenster, schlecht Stabilität der Elektroden-Elektrolyt-Grenzfläche, schlechte Luftstabilität, Mangel an groß angelegte Herstellungsverfahren und hohe Kosten. Die enge elektrochemische Das Fenster bestimmt, dass die Reduktionsreaktion des Elektrolyten stattfindet wenn der aktive Sulfidelektrolyt mit dem meisten Negativ in Kontakt kommt Elektroden, was zu einer wichtigen Grenzflächeninstabilität führt Engpass, der die Entwicklung von Festkörper-Lithiumbatterien einschränkt. Dieser Artikel fasst hauptsächlich den Entwicklungsstand der Mainstream-Anode zusammen Materialien für Festkörper-Lithiumbatterien auf Basis von Sulfidelektrolyten, und fasst die Schnittstellenprobleme und Lösungsstrategien zwischen ihnen weiter zusammen Sulfid-Festelektrolyte und Anodenmaterialien. Geben Sie Leitvorschläge für die Entwicklung und kommerzielle Anwendung von Festkörper-Lithiumbatterien basierend auf Sulfidelektrolyten.
1 Lithium-Metallanode
Metallisches Lithium ist ein wichtiger Kandidat Material zur Realisierung der nächsten Generation von Lithium mit hoher Energiedichte Batterien aufgrund seiner hohen theoretischen Kapazität (3860 mA·h·g-1) und extrem niedriges Elektrodenpotential (-3,040 V vs. SHE). Lithiumanoden sorgen für Batterie Energiedichte, die zehnmal höher ist als bei herkömmlichen Graphitanoden. Allerdings ist die Sein extrem niedriges elektrochemisches Potenzial bestimmt das metallische Lithium Ultrahohe chemische Reaktivität und elektrochemische Aktivität. Daher wenden Sie sich bitte an uns Mit jedem Elektrolyten kann es leicht zu einer Reduktionsreaktion im Elektrolyten kommen Elektrolyt. Die Volumenausdehnungsrate von metallischem Lithium ist groß Die Grenzflächenimpedanz wird erhöht, es bilden sich Lithiumdendriten und schließlich es kommt zu einem Kurzschluss. Da sind All-Solid-State-Lithiumbatterien vorhanden Probleme wie schlechte Zyklenstabilität, Schnittstellenfehler und geringe Lebensdauer Während des Betriebs ist es immer noch sehr wichtig, die Schnittstellenprobleme zu untersuchen zwischen metallischen Lithiumanoden und Festelektrolyten. Allgemein gesprochen, Die meisten Sulfid-Festelektrolyte weisen thermodynamische und kinetische Instabilität auf gegenüber metallischem Lithium. Gleichzeitig werden die Korngrenzen und Defekte sichtbar Im Inneren des Festelektrolyten kommt es zur Bildung von Lithiumdendriten. Dies kann die Probleme des Lithium-Dendriten-Wachstums und des Batterie-Kurzschlusses nicht lösen Schaltung. . Es ist erwähnenswert, dass bei hohen Stromdichten die Besonders problematisch ist der Ausfall der Lithium/Sulfid-Elektrolyt-Schnittstelle erheblich, was die Verbesserung der Energiedichte stark einschränkt Festkörper-Lithiumbatterien.
1.1 Lithium-/Sulfid-Elektrolyt chemische Stabilität der Grenzfläche
Wie in Abbildung 1 gezeigt, haben Wenzel et al. klassifizierten die Lithium/Festelektrolyt-Grenzflächentypen thermodynamisch Perspektive in thermodynamisch stabile Grenzflächen und thermodynamisch instabile Schnittstellen.
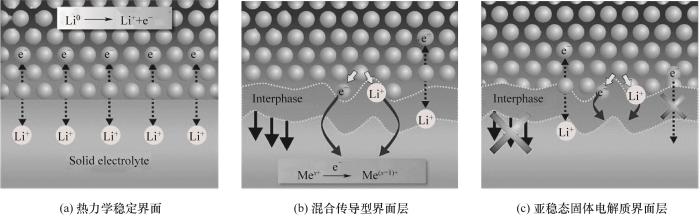
Abb.1 Arten von Grenzflächen zwischen Lithiummetall und Festkörperelektrolyt
(1) Thermodynamisch stabile Grenzfläche: As Wie in Abbildung 1(a) dargestellt, befinden sich die beiden in Kontakt stehenden Phasen in einem thermodynamischen Zustand Gleichgewicht. Metallisches Lithium reagiert überhaupt nicht mit dem Elektrolyten und bildet sich eine scharfe zweidimensionale Ebene, wie LiF, Li3N und andere Lithium-Binärmoleküle Verbindungen.
(2) Thermodynamisch instabile Grenzfläche: Aufgrund der thermodynamisch getriebenen chemischen Reaktion zwischen den Kontakten Elektrolyt und Elektrode kann eine dreidimensionale Grenzschicht gebildet werden. Abhängig davon, ob die Grenzschicht das Reaktionsprodukt gebildet hat Bei ausreichender elektronischer und ionischer Leitfähigkeit kann weiter unterschieden werden in die folgenden zwei Schnittstellen.
â Gemischte leitfähige Grenzflächenschicht: Wenn die Das Produkt verfügt über eine ausreichende elektronische und ionische Leitfähigkeit, die Grenzschicht kann stabil in den Festelektrolyten einwachsen. Die Bildung dieses Hybrids Die leitfähige Zwischenschicht ermöglicht letztendlich den Elektronentransport durch die Elektrolyt, was zur Selbstentladung der Batterie führt [Abbildung 1(b)]. Der Grenzflächeninstabilität von Sulfid-Festelektrolyten führt zur Entstehung Es kommt zu Nebenreaktionen an der Grenzfläche, die zu einer schnellen Entladung der Batterie führen können Kapazität oder sogar Ausfall. Wenzel et al. In-situ-Röntgenphotoelektronen verwendet Spektroskopie (XPS) kombiniert mit zeitaufgelösten elektrochemischen Messungen. Detaillierte Informationen zur chemischen Reaktion an der Schnittstelle zwischen LGPS und Es wird metallisches Lithium bereitgestellt und die Zersetzung von LGPS nachgewiesen führt zur Bildung einer Festelektrolyt-Grenzflächenphase bestehend aus Li3P, Li2S und Li-Ge-Legierungen. Unter ihnen sind Li3P und Li2S Ionenleiter Die Li-Ge-Legierung ist ein elektronischer Leiter. Die gemischte leitfähige Grenzflächenschicht gebildet wird, führt dazu, dass sich LGPS weiter zersetzt und die negative Elektrode zerstört Die Schnittstellenimpedanz wird weiter ansteigen, was schließlich zu einer Batterieladung führt Fehler.
â¡Metastabile Festelektrolytschnittstelle Schicht: Wenn das Reaktionsprodukt nicht leitend ist oder nur geringe elektronische Werte aufweist Leitfähigkeit kann die Grenzflächenschicht so begrenzt werden, dass sie zu einem sehr dünnen Film wächst. und eine stabile Festkörperelektrolyt-Interphase, SEI, kann gebildet werden. . Wie gezeigt In Abbildung 1(c) hängt die Leistung dieser Batterie vom Ion ab Leitungseigenschaften des SEI. Der Elektrolyt vom Sulfid-Germanit-Typ ist relativ stabil, und seine Zersetzungsprodukte Li2S, Li3P und LiX (X=Cl, Br und ich) haben eine ausreichend niedrige elektronische Leitfähigkeit, um eine weitere Zersetzung zu vermeiden des Elektrolyten und bilden leicht eine stabile SEI. Gleichzeitig hat Li3P hohe Ionenleitfähigkeit, die eine effiziente Übertragung von Lithiumionen gewährleistet Festkörperbatterien.
1.2 Forschung zum Mechanischen Eigenschaften von Lithiummetall
Der aktuelle Festkörper-Schnittstellenkontakt Zwischen der negativen Elektrode und dem Festelektrolyten liegt ein begrenzter Punkt Kontakt, was leicht zu einer Erhöhung des Grenzflächenwiderstands führt. Jedoch, die mechanischen Eigenschaften von metallischem Lithium, insbesondere das Kriechen von metallischem Lithium, wird den Grenzflächenkontakteffekt weiter beeinflussen, was dazu führt Bildung von Grenzflächenhohlräumen und sogar Ablösung der negativen Elektrode bei hohen Temperaturen aktuelle Dichten. Daher untersuchen wir die mechanischen Eigenschaften von Metallen Lithium, insbesondere das Kriechverhalten von metallischem Lithium, ist entscheidend für die Zyklenfestigkeit von Festkörperbatterien.
Tian et al. durchgeführte Kontaktmechanik Forschung und etablierte relevante theoretische Modelle, um die Grenze zu ermitteln Bedingungen, die die Spannungsverteilungsfunktion von elastischen, plastischen und viskose Kontakte an der Lithiummetallanode. Prognostizieren Sie die Kontaktfläche des metallische Lithium-Sulfid-Festelektrolyt-Grenzfläche und berechnen Sie die Kapazität Verlust durch Ionendiffusion an der Grenzfläche und Verlust der Kontaktfläche. Experimente zeigen, dass bei einer niedrigeren Abschaltspannung (3,8 V) der Zusammenhang besteht Der Unterschied zwischen der Abnahme der Batteriekapazität und dem Verlust der Kontaktfläche beträgt nahezu linear, mit einer Steigung von 1. Bei einer höheren Abschaltspannung (4,0 V) ist die Steigung ist kleiner als 1 und die Kapazitätsabfallrate nimmt mit zunehmender Entladung ab Rate. Fincher et al. verwendeten Zugversuche, um die mechanischen Auswirkungen von zu testen kommerzielle Lithiumfolie und stellte fest, dass die Streckgrenze von metallischem Lithium lag im Bereich von 0,57 bis 1,26 MPa bei einer Dehnungsrate von 5×10-4~5×10-1 s-1. Für die Beim Eindrucktest mit einem Zielwert von 0,05 sâ1 fiel die Härte stark ab fast 43,0 MPa auf 7,5 MPa, als die Eindringtiefe von 250 nm auf 10 zunahm µm. Die in Nanoindentationstests gemessenen Kunststoffeigenschaften zeigten starke Ergebnisse Dehnungsratenabhängigkeit mit Spannungsexponenten von 6,55 bzw. 6,90. Die Finite-Elemente-Analyse wird verwendet, um die Eindringtiefe mit der relevanten Länge in Beziehung zu setzen Waagen in Batterieanwendungen. Es kann wichtige Hinweise geben Optimierung der Struktur von Lithiumanoden und Sicherstellung des Ladens und Entladens Stabilität, um die ungleichmäßige Ablagerung von Lithium während des Prozesses zu reduzieren Elektrochemische Zyklen. Masias et al. systematisch die elastischen gemessen, Plastische und zeitabhängige mechanische Eigenschaften von polykristallinem Lithium bei Raumtemperatur. Sein Elastizitätsmodul, sein Schubmodul und sein Poisson-Verhältnis waren bestimmt, 7,82 GPa, 2,83 GPa bzw. 0,38 zu betragen, und die Ausbeute Die Festigkeit lag zwischen 0,73 und 0,81 GPa. Darunter dominiert das Potenzgesetzkriechen Spannung, mit einem Stressindex von 6,56. Im Inneren wurde ein Kompressionstest durchgeführt der batterierelevante Spannungsbereich (0,8~2,4 MPa) und deutliche Streifenbildung und a Es wurde eine Abnahme der Dehnungsrate mit der Zeit beobachtet. Narayan et al. gegründet a Reaktionsmodell für eine Festkörperbatterie mit Lithiumanode basierend auf großen Deformationstheorie, die die Wechselwirkung zwischen der Lithiumanode und simuliert der Sulfid-Festelektrolyt bei der elastisch-viskoplastischen Reaktion von Lithium. Es zeigt, dass die Dehnungsreaktion mit der Volumenverformung von zusammenhängt Lithiumanode, die der Hauptgrund für das Versagen des Festkörpers ist Batterien. Durch Batch-Zug- und Nanoindentationstests wurde Lithiummetall nachgewiesen offensichtliche Abhängigkeit von der Dehnungsrate und Größenabfall während des Kriechens. hat das gezeigt Eine Feinabstimmung der Verformungsmechanik kann durch die Anpassung von Lithium erreicht werden Ablagerungen, um die Robustheit der Lithiumanode zu verbessern und Instabilität zu mildern Lithiumwachstum während des elektrochemischen Kreislaufs.
Zusätzlich zur gesamten mechanischen Studie von metallischem Lithium liefert das Studium der Nanomechanik recht wichtige und äußerst detaillierte Oberflächen- und Ortsinformationen in kleinen Maßstäben. Nanoindentationsexperimente sind eines der am häufigsten verwendeten Analysewerkzeuge für Oberflächen- und lokale Eigenschaften. Nanoindentationsexperimente durchgeführt in Inertgas kann die mechanische, elektrochemische und umfassendere Analyse durchführen morphologisches Kopplungsverhalten von metallischem Lithium. Herbert et al. durchgeführt eine Reihe von Nanoindentationsexperimenten an hochreinen, aufgedampften Lithiumfilmen und gesammelte Daten zu plastischen Fließeigenschaften, einschließlich Elastizitätsmodul, Härte und Streckgrenze. Die Entwicklung der oben genannten Daten mit Schlüsselvariablen wie Längenskala, Dehnungsrate, Temperatur, kristallographische Orientierung und elektrochemischer Kreislauf wurde untersucht, was darauf hindeutet, dass der plastische Fluss von Lithium hängt hauptsächlich mit dem stationären Kriechen unter konstanter Last zusammen oder Druck. Das Kriechen von Lithium beim elektrochemischen Laden und Entladen kann ein Knicken an der Schnittstelle hervorrufen und zusätzliche Spannungen erzeugen. Am Gleichzeitig wird das viskoplastische Verhalten von Lithium die noch weiter beeinflussen Die Kontaktfläche der Grenzfläche wird beschädigt, was zu einer Verschlechterung der Ionendiffusionskanäle führt und Schnittstelleninstabilität. Allerdings ist die aktuelle nanomechanische Forschung am metallisches Lithium befindet sich noch im Anfangsstadium und weitere Forschungen sind bereits geplant sehr wichtig. Einige neue Technologien wie Nanosäulenkomprimierung und In-situ-Echtzeitbeobachtungen der Nanomechanik von metallischem Lithium wurden ebenfalls durchgeführt vorgeschlagen, die Kopplung der metallischen Lithium-Anodenschnittstelle zu analysieren und Stellen Sie High-Fidelity-Informationen über die Schnittstelle bereit, um sie besser zu verstehen mechanischer Kopplungseffekt von metallischem Lithium, wodurch die Möglichkeit geschaffen wird für das Design nanoskaliger metallischer Lithiumanoden.
1.3 Keimbildung und Wachstum von Lithium Dendriten
Lithiumdendriten gehören dazu grundsätzliche Fragen zur Stabilität und Sicherheit von Lithium-Ionen-Batterien. Feste Elektrolyte gelten seit langem als mögliche Lösung für Lithium Aufgrund ihrer hohen mechanischen Festigkeit verhindern sie das Wachstum von Dendriten. Allerdings zahlreich Forschungsergebnisse zeigen, dass das Problem der Lithiumdendriten im Feststoff besteht Elektrolyten existiert immer noch und ist sogar noch schwerwiegender als bei flüssigem Lithium Batterien. Bei Festkörperbatterien gibt es viele Gründe für das Wachstum Lithiumdendriten, einschließlich ungleichmäßiger Kontakte an der Grenzfläche zwischen den Elektrolyt und metallisches Lithium, Defekte, Korngrenzen, Hohlräume innerhalb der Elektrolyt, Raumladungen usw. Monroe et al. berichteten über einen Lithiumdendrit Wachstumsmodell basierend auf metallischer Lithiumanode und Festelektrolyt. Faktoren wie Elektrolytelastizität, Kompressionskraft, Oberflächenspannung und Verformungskräfte wurden im Modell berücksichtigt. Simulationsergebnisse zeigen das wenn der Schermodul des Elektrolyten dem von Lithium entspricht, a Es entsteht eine stabile Schnittstelle. Wenn der Schermodul des Elektrolyten ist ungefähr doppelt so viel wie Lithium (4,8 GPa), die Erzeugung von Lithium Dendriten können unterdrückt werden. Allerdings handelt es sich tatsächlich um eine Festkörper-Lithiumbatterie Untersuchungen ergaben, dass Lithiumdendriten immer noch im Feststoff produziert werden Elektrolyte mit hohem Schermodul [wie Li7La3Zr2012 (LLZO), elastisch Modul â 100 GPa]. Daher ist dieses Modell nur ideal anwendbar Grenzflächen ohne mikroskopische Defekte und ungleichmäßige Verteilung. Porz et al. fanden heraus, dass der hohe Schermodul des Elektrolyten zu einer hohen Endfestigkeit führt Stromdichte, die die Keimbildung und das Wachstum von metallischem Lithium induziert Korngrenzen und Hohlräume des Festelektrolyten. Nagao et al. vor Ort eingesetzt Rasterelektronenmikroskopie zur Beobachtung der Lithiumablagerung und -auflösung Prozess an der negativen Elektrodenschnittstelle in All-Solid-State-Lithium Batterien, die die Veränderungen in der Morphologie der Lithiumablagerung aufdecken unterschiedliche angelegte Stromdichten. Wenn die Stromdichte 1 überschreitet mA·cm-2, lokale Lithiumablagerung führt zu größeren Rissen, was zu a führt Verringerung der Reversibilität der Lithiumablagerung und -auflösung und die Risse werden sich weiter ausdehnen, bis sich Lithiumdendriten bilden. Auf der anderen Seite Andererseits kann eine gleichmäßige und reversible Lithiumabscheidung und -auflösung erreicht werden bei einer geringen Stromdichte von 0,01 mA·cm-2, nahezu ohne Risse. Daher, Eine alleinige Konzentration auf den hohen Schermodul des Elektrolyten kann das Problem nicht lösen Problem des Lithiumdendritenwachstums und kann die Ionenleitfähigkeit verringern den Elektrolyten und beeinflussen die Energiedichte von Festkörperbatterien.
Porz et al. untersuchte die Keimbildung und Wachstumsmechanismus von Lithiumdendriten in verschiedenen Elektrolyten und zeigte dies Der Beginn der Lithiumpenetration hängt von der Oberflächenmorphologie des Feststoffs ab Elektrolyt. Insbesondere die Größe und Dichte der Defekte sowie die Ablagerung Lithium in Defekten kann Spitzenspannungen erzeugen, die die Rissausbreitung vorantreiben. In Darüber hinaus können Unterschiede in der Leitfähigkeit zwischen Körnern, Korngrenzen oder Grenzflächen können auch zur Bildung von Lithiumdendriten führen. Yu et al. untersuchte theoretisch die Energetik, Zusammensetzung und Transporteigenschaften von drei niederenergetische, symmetrisch geneigte Korngrenzen in Festelektrolyten. Es zeigt, dass der Transport von Lithiumionen an Korngrenzen stärker ist schwieriger als in Körnern und ist temperatur- und korngrenzenempfindlich Struktur. Raj et al. untersuchte theoretisch den Effekt der Korngrenze Widerstand gegen die Keimbildung von Lithiumdendriten am Feststoff Elektrolyt/Lithium-Grenzfläche. Sie schlugen vor, dass der hohe Ionenwiderstand von die Korngrenzen und die physikalischen Unregelmäßigkeiten der Anodengrenzfläche würde zu einer Erhöhung des lokalen elektrochemischen mechanischen Potenzials führen Lithium und fördert dadurch die Bildung von Lithiumdendriten. Daher, Im Vergleich zu Kristallkörnern sind Korngrenzen mit hohem Ionenwiderstand vorhanden Es ist wahrscheinlicher, dass es die Keimbildung und das Wachstum von Lithiumdendriten induziert. Der Wachstumsmechanismus von Lithiumdendriten in Festkörperbatterien werden mit weiterer Recherche nach und nach klarer. Es besteht jedoch immer noch ein Mangel wirksamer Methoden zur vollständigen Unterdrückung von Lithiumdendriten und Ähnlichem Die Forschung muss weiterhin intensiv sein, um die Anwendung zu realisieren metallische Lithiumanoden in Festkörperbatterien so bald wie möglich.
1.4 Lösungsstrategien für Schnittstellenprobleme
Zur Lösung wurden viele Methoden vorgeschlagen die Herausforderungen bei der Anwendung von Lithiumanoden, einschließlich der Anwendung Außendruck, Verwendung von SEI-Schichten, Optimierung von Elektrolyten und Modifikation von metallischem Lithium. Dies verringert die Auswirkungen des Lithiumkriechens die Batterie, vergrößert die Kontaktfläche der Fest-Fest-Grenzfläche, hemmt Nebenreaktionen an der Grenzfläche zwischen dem Sulfid-Festelektrolyten und dem metallische Lithiumanode, verbessert die Lithophilie der Anodenschnittstelle und verhindert die Bildung und das Wachstum von Lithiumdendriten.
1.4.1 Externen Druck anwenden
Die Anwendung von Druck von außen kann zu einer Vergrößerung führen Kontaktfläche der Fest-Fest-Grenzfläche, reduzieren Sie den durch Kriechen verursachten Schaden die negative elektrode interface, und verbessern die zyklus stabilität der Batterie. Zhang et al. berichtet über eine mehrskalige dreidimensionale Zeitabhängigkeit Kontaktmodell zur Beschreibung der Entwicklung des Festelektrolyten/Lithiumanodens Schnittstelle unter Stapeldruck. Theoretische Berechnungen zeigen, dass der Stapel hoch ist Drücke von etwa 20 GPa hemmen tendenziell die Bildung von Hohlräumen, was vielversprechend ist Methode, um einen konsistenten Schnittstellenkontakt sicherzustellen und möglicherweise eine Stabilität zu erreichen Batterieleistung. Ein höherer Stapeldruck ist für die Batterie nicht vorteilhafter Leistung. Ein geringerer Stapeldruck kann den Kontakt grundsätzlich nicht lösen Problem an der Festkörper-Grenzfläche. Es kann leicht ein übermäßiger Stapeldruck entstehen Lithiumdendriten und verursachen Kurzschlüsse in der Batterie. Wang et al. studiert die Auswirkung des Stapeldrucks auf die Leistung des Lithium/Sulfid-Elektrolyten Batterien und stellte fest, dass während des Lithium-Stripping-Prozesses das Maximum erreicht wurde Die zulässige Abisolierstromdichte ist proportional zur angelegten externen Druck. Während des Abscheidungsprozesses verringert sich der höhere angewandte Druck Der maximal zulässige Abscheidungsstrom, d. h. ein hoher Stapeldruck, wird erreicht führen leicht zur Bildung von Lithiumdendriten (Abbildung 2).
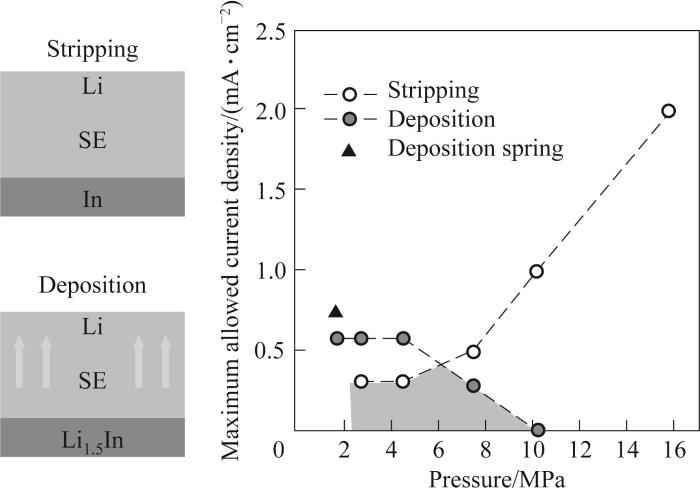
Abb.2 Zusammenhang zwischen dem maximal zulässigen Strom Dichte (MACD) und externer Druck zum Strippen und Abscheiden in ASSLBs
1.4.2 Künstlicher Festelektrolyt Schnittstellenschicht
Platzierung eines stabilen SEI am Sulfidfeststoff Durch die Elektrolyt/Lithium-Schnittstelle kann ein direkter Kontakt zwischen metallischem Lithium vermieden werden und der Sulfid-Festelektrolyt, wodurch das Auftreten von wirksam verhindert wird Grenzflächennebenreaktionen und die Bildung und das Wachstum von Lithiumdendriten. Im Allgemeinen gibt es zwei Methoden zur Bildung von SEI: In-situ-SEI und Ex-situ-SEI. Wang et al. etablierte eine in-situ ionenleitende Schutzschicht auf dem Oberfläche aus poliertem Lithiummetall durch Spin-Coating-Technologie. Eine Mischung aus Zur Einbettung wird Polyacrylnitril (PAN) und Fluorethylencarbonat (FEC) verwendet Künstliche Schutzschicht (LiPFG), bestehend aus einer organischen Matrix aus anorganischen Stoffen Li3N und LiF auf der Lithiumoberfläche. Fördert effektiv die gleichmäßige Ablagerung von Lithium und verbessert die Schnittstellenstabilität und -kompatibilität. Li et al. entworfen eine in situ polymerisierte Zwischenschicht aus 1,3-Dioxolan in Lithium Difluor(oxalat)phosphat. Das an der Li/LGPS-Grenzfläche gebildete SEI hat eine doppelschichtiger Aufbau. Die obere Schicht ist reich an Polymeren und elastisch Die untere Schicht ist voll von anorganischen Substanzen, die die Keimbildung hemmen und Wachstum von Lithiumdendriten. Gleichzeitig ist der nahtlose Kontakt der Es wird eine Li/LGPS-Schnittstelle erreicht, die die gleichmäßige Übertragung von fördert Lithiumionen und hemmt den kontinuierlichen Abbau von LGPS. Lithium Symmetrische Batterien mit dieser Gel-Polymer-Beschichtung weisen eine stabile Zyklenfestigkeit auf 500 h unter den Bedingungen 0,5 mA·cm-2/0,5 mA·h·cm-2. Gao et al. berichtete a Nanokomposit auf Basis organischer elastischer Salze [LiO-(CH2O) n -Li] und anorganischer Nanopartikelsalze (LiF, -NSO2-Li, Li2O), die als Zwischenprodukt verwendet werden können Phase zum Schutz von LGPS. Das Nanokompositmaterial wird in situ auf Li gebildet durch die elektrochemische Zersetzung des flüssigen Elektrolyten, wodurch reduziert wird der Grenzflächenwiderstand, weist eine gute chemische und elektrochemische Stabilität auf und Schnittstellenkompatibilität und verhindert wirksam das Auftreten von LGPS Reduktionsreaktion. Stabile Lithiumabscheidung von mehr als 3000 Stunden und einem Zyklus Lebensdauer von 200 Mal erreicht wurden. Die mechanische Festigkeit von SEI ist extrem wichtig für die Zyklenfestigkeit von Festkörperbatterien. Wenn die Wenn die mechanische Festigkeit von SEI zu gering ist, kommt es zum Eindringen von Dendriten. Wenn die Ist SEI nicht zäh genug, kommt es zu Biegerissen [Abb. 3(a)]. Duan et al. stellten durch chemische Joddampfabscheidung eine strukturierte LiI-Schicht her künstlicher SEI zwischen metallischem Lithium und LGPS [Abbildung 3(b)]. Die LiI-Schicht Das in situ erzeugte Material weist einen einzigartigen, schlanken, reisförmigen, ineinander verschlungenen LiI-Kristall auf Struktur, die eine hohe mechanische Festigkeit und ausgezeichnete Zähigkeit bietet, und kann das Wachstum von Lithiumdendriten wirksam hemmen. und passt sich gut an Änderungen des Lithiumvolumens, wodurch eine starke Li/LGPS-Grenzfläche aufrechterhalten wird [Abbildung 3(c)]. Gleichzeitig weist diese LiI-Schicht eine hohe Ionenleitfähigkeit auf eine gewisse chemische Inertheit und zeigt eine hohe Stabilität sowohl gegenüber Lithium als auch gegenüber LGPS. Der Die vorbereitete Li/LiI/LGPS/S-Batterie zeigte eine hohe Kapazität von 1400 mA·h·g-1 bei 0,1 C und zeigte eine hohe Kapazitätserhaltungsrate von 80,6 % nach 150 Zyklen bei Raumtemperatur Temperatur. Selbst unter rauen Bedingungen von 1,35 mA·h·cm-1 und 90°C bleibt es ruhig weist eine hohe Kapazität von 1500 mA·h·g-1 und eine hervorragende Stabilität für 100 auf Zyklen. Zeigt sein großes Potenzial in verschiedenen Anwendungsszenarien. Bezogen auf die Lösungsmethode, Liang et al. synthetisierten in situ eine Li x SiS y-Schicht auf dem Oberfläche aus metallischem Lithium als SEI zur Stabilisierung der Li/Li3PS4-Grenzfläche. Das Die Li x SiS y-Schicht ist luftstabil und kann Nebenreaktionen wirksam verhindern zwischen Lithium und der Umgebung. Es kann stabil gefahren werden mehr als 2000 Stunden in einer symmetrischen Batterie. Das Team berichtete auch a Lösungsstrategie unter Verwendung von Polyacrylnitril-Schwefel-Verbundwerkstoffen (PCE) als Ex-situ künstlicher SEI. Verwendung von PCE als Zwischenschicht an der Schnittstelle zwischen Lithiummetall und LGPS unterdrücken die Grenzflächenreaktion zwischen LGPS und Li-Metall. Die zusammengebaute Festkörperbatterie weist eine hohe Anfangsleistung auf Kapazität. 148 mA·h·g-1 bei 0,1 C Rate. Sie beträgt 131 mA·h·g-1 bei 0,5 °C. Der Die Kapazität bleibt nach 120 Zyklen bei 0,5 C bei 122 mA·h·g-1. Zeigen hervorragende Leistung.
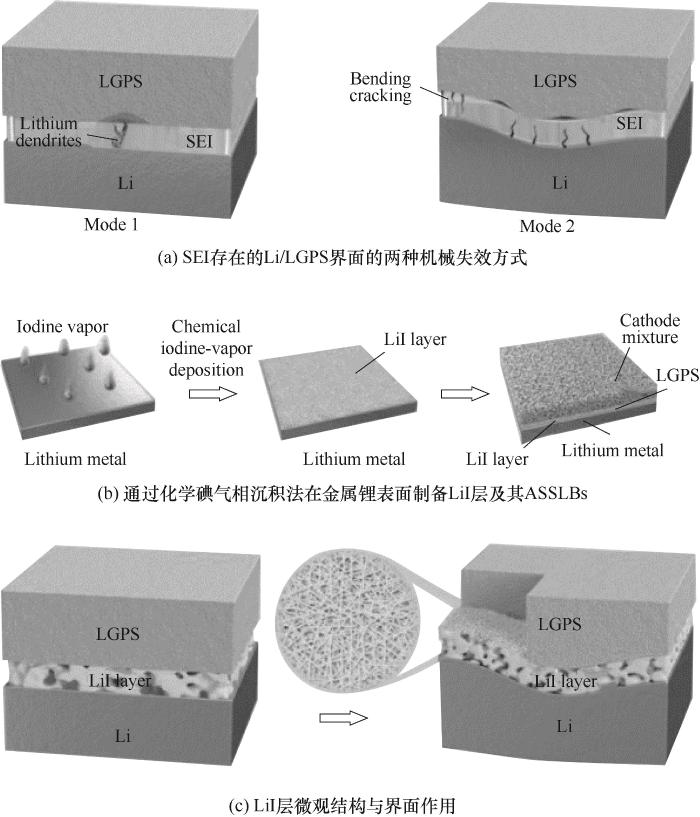
Abb.3 Schematische Darstellung der Schnittstelle zwischen LGPS und Li Anode
1.4.3 Elektrolytoptimierung
Elektrolytoptimierung kann nicht nur die Ionenleitfähigkeit des Sulfidelektrolyten verbessern, aber auch vermeiden oder reduzieren die Reduktion des Elektrolyten durch die Lithiumanode auf ein bestimmtes Maß Ausmaß. Unter diesen ist die Verwendung einer geeigneten Elementsubstitution eine wirksame Methode Strategie zur Verbesserung der Ionenleitfähigkeit und Stabilisierung der Anodenschnittstelle. Experimente von Sun et al. zeigen, dass Sauerstoffdotierung die Ionenleitfähigkeit erhöhen kann (Li10GeP2S11.7O0.3: 8,43 × 10-2 S·cm-1; LGPS: 1,12 × 10-2 S·cm-1). Gleichzeitig Mit der Zeit werden Grenzflächenreaktionen verhindert und dadurch die Stabilität verbessert die Lithium/Sulfid-Elektrolyt-Grenzfläche. Neben Sauerstoff auch Metallsulfid Durch Dotierung kann auch die Impedanz des Lithium/Sulfid-Elektrolyten verringert werden Schnittstelle. Zum Beispiel Li7P2.9S10.85Mo0.01 (verbesserte Li2S-P2S5-Glaskeramik). mit MoS2-Dotierung) weist eine geringere Grenzflächenimpedanz auf als L7P3S11. Li3.06P0.98Zn0.02S3.98O0.02 (ZnO dotiert in Li3PS4) zeigt ebenfalls einen guten Zyklus Stabilität (100 Zyklen Kapazitätserhaltungsrate von 81 %, reines Li3PS4 beträgt nur 35 %). Obwohl eine geeignete Elementsubstitution gute Ergebnisse für die gezeigt hat Lithium/Sulfid-Elektrolyt-Grenzfläche. Allerdings sind diese Modifikationsmethoden immer noch Probleme wie das Auftreten von Nebenreaktionen und die Bildung von Lithiumdendriten während langer Zyklen. Die Obergrenze der Rolle von Kinetik zu Grenzflächenproblemen sollte weiter bestätigt werden, und andere Strategien sollten kombiniert werden, um die chemische Stabilität des Lithiums/Sulfids zu verbessern Elektrolytschnittstelle. Das Design der Elektrolytstruktur kann dies ebenfalls verhindern das Auftreten von Nebenreaktionen verhindern und die Keimbildung und das Wachstum von Lithium verhindern Dendriten. Ye et al. schlug ein geniales Design einer Sandwichstruktur vor Elektrolyt [Abbildung 4(a)]. Den instabilen Elektrolyten zwischen mehr einschichten Stabile Elektrolyte vermeiden direkten Kontakt durch gute lokale Zersetzung die Schicht des weniger stabilen Elektrolyten. Es kann sowohl das Wachstum von verhindern Lithiumdendriten und füllen die entstandenen Risse. Diese Dehnschraube ist schraubenartig Das Designkonzept erreicht einen stabilen Zyklus aus metallischer Lithiumanode gepaart mit LiNi0,8Mn0,1Co0,1O2-Kathode [wie in Abbildung 4(b) gezeigt, die Kapazitätserhaltung Die Rate beträgt 82 % nach 10.000 Zyklen bei 20 °C. Noch wichtiger ist, dass diese Arbeit es nicht ist auf bestimmte Materialien beschränkt. Stabile Zyklen können mit LGPS beobachtet werden, LSPSCl, Li9,54 Si1,74P0,94S11,7Cl0,3 (LSPS), Li3YCl6 usw. als zentrale Schichtmaterialien. Es bietet eine äußerst anwendbare Entwurfsmethode zur Verbesserung der Stabilität des Grenzfläche zwischen Lithiumanode und Sulfidelektrolyt.
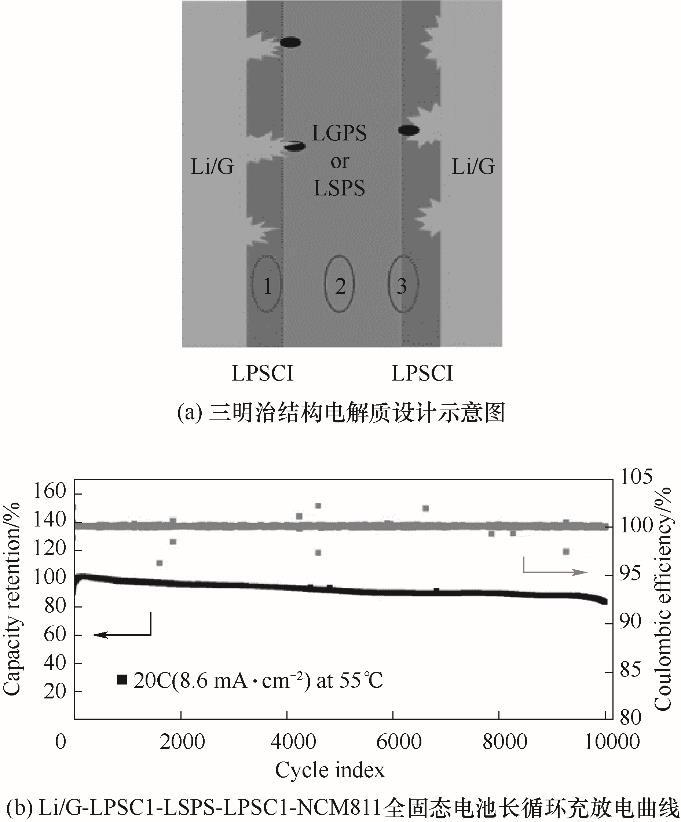
Abb.4 Schematische Darstellung eines Elektrolyten mit Sandwichstruktur Design und elektrochemische Leistungskurve für lange Zyklen
1.4.4 Modifikation der Lithiumanode
Modifikation der Lithium-Anodendose das Auftreten von durch das Kriechen verursachten Elektrolytrissen verringern oder vermeiden Verhalten von metallischem Lithium während des Zyklierens und hemmt dadurch die Bildung von Lithiumdendriten. Wie in Abbildung 5 gezeigt, haben Su et al. Dazu wurde eine Graphitfolie verwendet Schützen Sie die negative Lithiumelektrode und trennen Sie die LGPS-Elektrolytschicht aus dem Lithiummetall und hemmen die Zersetzung von LGPS. Basierend auf der Beim mechanischen Schrumpfmechanismus wird ein Außendruck von 100 bis 250 GPa ausgeübt zum Batteriesystem. Diese externe Kraftbeschränkung optimiert die Schnittstelle Kontakt zwischen Elektrolytpartikeln und zwischen der Elektrolytschicht und dem Li/G-Anode. Die Festkörperbatterie erreicht eine hervorragende Zyklenleistung. Darüber hinaus ist auch das Legieren von metallischem Lithium ein wichtiger Lösungsansatz Problem der Lithium-Anoden-Schnittstelle bei Festkörper-Lithiumbatterien. In Aktuellen Berichten zufolge haben Lithiumlegierungen gewisse Vorteile bei der Lösung gezeigt Probleme wie schwerwiegende Nebenreaktionen an der Grenzfläche und die Entstehung von Lithium Dendriten in Lithiumanoden, die im Folgenden ausführlich vorgestellt werden.

Abb.5 Schutzdesign einer Graphitfolie für Li/LGPS Schnittstelle
Unvollendet, Fortsetzung folgt.



