Kategorien
neuer Blog
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
- Hauptursachen für Undichtigkeiten an der Zellversiegelung von Beuteln
- Formation und Grading in der Lithium-Ionen-Batterieherstellung
Tags
LiNi0,91Co0,06Al0,03O2@Ca3(PO4)2-Kathodenmaterialien mit ultrahohem Nickelgehalt
Verbesserter Lithium-Lagerungsstabilitätsmechanismus von LiNi0.91Co0.06Al0.03O2@Ca3(PO4)2-Kathodenmaterialien mit ultrahohem Nickelgehalt
Autor: ZHU Hezhen, WANG Xuanpeng, HAN Kang, YANG Chen, WAN Ruizhe, WU Liming, MAI Liqiang. Verbesserter Lithium-Lagerungsstabilitätsmechanismus von LiNi0.91Co0.06Al0.03O2@Ca3(PO4)2-Kathodenmaterialien mit ultrahohem Nickelgehalt. Journal of Inorganic Materials, 2022, 37(9): 1030-1036 DOI:10.15541/jim20210769
Ultra-Nickel-Material als neue Lithium-Ionen-Batteriekathode hat aufgrund seiner hohen spezifischen Kapazität, hohen Spannung und niedrigen Kosten viel Aufmerksamkeit auf sich gezogen. Die erzeugten Mikrorisse, die mechanische Pulverisierung und die irreversible Phasenumwandlung während des Zyklierens führen jedoch zu einer schlechten Zyklenstabilität. Hier wurde eine Reihe von Ca3(PO4)2-beschichteten LiNi0.91Co0.06Al0.03O2-Materialien mit ultrahohem Nickelgehalt und unterschiedlichen Dicken (NCA@nCP) durch eine einfache nasschemische Strategie hergestellt. Unter ihnen zeigte NCA@1CP eine spezifische Entladekapazität von 204,8 mAh/g unter 2,7–4,3 V bei 1 C (1 C = 200 mA/g) mit einer Kapazitätserhaltungsrate von 91,5 % nach 100 Zyklen. Selbst nach 300 Zyklen bei 2°C blieb die spezifische Entladekapazität bei 153,4 mAh/g. Die Ergebnisse der Materialcharakterisierung bestätigen weiter, dass die Beschichtungshülle die Li/Ni-Mischung hemmt, irreversible Phasenumwandlung und mechanische Pulverisierung des NCA@1CP, was die Zyklenstabilität stark verbessert. Diese Arbeit zeigt, dass die Ca3(PO4)2-Beschichtungsstrategie ein großes Anwendungspotenzial bei der Verbesserung der Lithium-Lagerstabilität von Ultra-High-Nickel-Kathodenmaterialien hat.
Um die Nachfrage nach hoher Energiedichte von Lithium-Ionen-Batterien zu erfüllen, haben Forscher eine Reihe von Fortschritten auf dem Gebiet der Entwicklung von Kathodenmaterialien mit hoher reversibler spezifischer Kapazität und hoher Betriebsspannung erzielt. Kathodenmaterialien mit ultrahohem Nickelgehalt wie LiNixM1-xO2 (M ist ein Übergangsmetall, x≥0,9) haben die Vorteile hoher Kapazität, hoher Spannung und niedriger Kosten und sind eine wichtige Entwicklungsrichtung von Kathodenmaterialien für Lithium- Ionenbatterien der Zukunft. Kim synthetisierte LiNi0,90Co0,05Mn0,05O2-Material mit ultrahohem Nickelgehalt durch ein Kopräzipitationsverfahren, und die anfängliche spezifische Entladungskapazität einer Li-Ionen-Batterie, die es als Kathodenmaterial verwendete, betrug 229,0 mAh/g. Das von Ryu synthetisierte LiNi0,90Co0,09W0,01O2 zeigte eine ultrahohe spezifische Anfangsentladungskapazität von 231,2 mAh/g. Jedoch, Das Problem des Kapazitätsschwunds schränkt die kommerzielle Anwendung dieser Art von Materialien ein, und eine große Anzahl von Studien hat bewiesen, dass die Gründe auf die folgenden drei Aspekte zurückzuführen sind: (1) Ein hoher Ni-Gehalt erschwert die Li/Ni-Mischung und hemmt Lithiumionen Diffusion und erhöhen die Reaktionsimpedanz, was zu einem tatsächlichen Kapazitätsverlust führt. (2) Das unter der Bedingung der Lithiumentfernung gebildete hochaktive Ni4+ kann leicht Nebenreaktionen mit dem Elektrolyten haben und die Elektrode und den Elektrolyten verbrauchen. Es fördert die Strukturumwandlung des Materials von der geschichteten Phase in die ungeordnete Spinellphase und die Steinsalzphase und schädigt die Kristallstruktur des Materials stark, wodurch die Zyklenfestigkeit verringert wird.
Die Beschichtungsmodifikation wird häufig verwendet, um das Problem des Kapazitätsschwunds von Kathodenmaterialien mit hohem Nickelgehalt zu lösen und die Zyklenstabilität zu verbessern, unter denen Oxidmaterialien wie Al2O3, TiO2, SiO2 und ZrO2 am häufigsten vorkommen. Verglichen mit Oxiden haben Phosphate eine bessere Lithiumionenmobilität und chemische Stabilität und haben in den letzten Jahren große Aufmerksamkeit auf dem Gebiet der Oberflächenmodifikation von Kathodenmaterialien mit hohem Nickelgehalt erhalten. Xiao(XIAO YH, MIARA LJ, WANG Y, et al.) bestätigten durch rechnerisches Screening, dass Phosphat als Kathodenbeschichtungsmaterial die Stabilität deutlich verbessern kann. Gängige Phosphatbeschichtungsmittel sind Mn3(PO4)2, BPO4, AlPO4 und Li3PO4. Yan (YAN PF, ZHENG JM, LIU J, et al.) verwendete Atomlagenabscheidungstechnologie, um Li3PO4 auf der Oberfläche des Kathodenmaterials LiNi0,76Mn0,14Co0,10O2 mit hohem Nickelgehalt zu beschichten, was den irreversiblen Phasenübergang des Materials unterdrückte und die Kinetik der Kathoden-Elektrolyt-Grenzfläche verbesserte. Feng (FENG Z, RAJAGOPALAN R, SUN D, et al.) beschichtete Li3PO4-AlPO4-Al(PO3)3 auf LiNi0.8Co0.1Mn0.1O2-Material und die Zyklusleistung wurde signifikant verbessert. Unter den Phosphatmaterialien hat Ca3(PO4)2(CP) aufgrund der starken Bindung zwischen Ca2+ und [PO4]3- eine hervorragende chemische und thermische Stabilität. Über die durch CP-Beschichtung modifizierten Ultrahochnickel-Kathodenmaterialien wurde jedoch noch nicht berichtet. Daher wurde eine Reihe von CP-beschichteten LiNi0,91Co0,06Al0,03O2-Kathodenmaterialien mit ultrahohem Nickelgehalt (NCA@nCP, n=0,5, 1, 3) durch ein einfaches nasschemisches Verfahren hergestellt. Die Struktur, Morphologie und der elektrochemische Leistungsverbesserungsmechanismus von NCA@nCP wurden im Detail untersucht und analysiert.
Herstellung von Kathodenmaterial
Ni0,91Co0,06Al0,03(OH)2 und LiOH·H2O wurden in einem Molverhältnis von 1:1,05 gemischt, dann auf 500°C für 5 h mit einer Geschwindigkeit von 5°C/min in einer Sauerstoffatmosphäre erhitzt und dann zur Isolierung auf 720°C erhitzt. Nach 15 h und schließlich natürlich auf Raumtemperatur abgekühlt, wurde schwarzes NCA-Pulver erhalten. 0,74 g NH4H2PO4 und 2,28 g Ca(NO3)2·4H2O wiegen und in 100,0 ml Wasser bzw. 100,0 ml wasserfreiem Ethanol auflösen. Zunächst wurden 0,5 ml Ca(NO3)2-Lösung (Lösung A) und 0,5 ml NH4H2PO4-Lösung (Lösung B) zu 50,0 ml absolutem Ethanol gegeben, dann 1,00 g NCA-Pulver langsam hinzugefügt und schließlich das Lösungsmittel entfernt durch Rühren und Eindampfen bei 80°C, um ein Pulver zu erhalten. Dann wurde das Pulver in einer Sauerstoffatmosphäre bei 550°C (Heizrate von 5°C/min) für 2 h gesintert. Zu diesem Zeitpunkt betrug der Massenanteil von CP 0,5 %, und das erhaltene Produkt wurde als NCA@0,5CP definiert. Wenn jede der A- und B-Lösungen 1,0 ml beträgt, beträgt der Massenanteil von CP 1,0 % und das erhaltene Produkt wird als NCA@1CP definiert; wenn die A- und B-Lösungen jeweils 3,0 ml sind, beträgt der Massenanteil von CP 3,0 % und das erhaltene Produkt wird als NCA@3CP definiert.
Materialcharakterisierung
Die Kristallstruktur des Materials wurde durch Röntgenbeugung (Röntgenbeugung, XRD, D8 Discover X, CuKα-Strahlung) charakterisiert. Die verfeinerten XRD-Daten wurden von der GSAS-Software unter Verwendung der Rietveld-Methode berechnet. Die Morphologie und Mikrostruktur der Materialien wurden durch Rasterelektronenmikroskopie (SEM, JEOL JSM-7100F) und Transmissionselektronenmikroskopie (TEM, JEM-2100F) charakterisiert. Die Elementverteilung des Materials wurde mit einem Röntgenenergiedispersionsspektrometer (Energiedispersionsspektrometer, EDS, EDX-GENESIS 60S) beobachtet. Mittels Röntgen-Photoelektronen-Spektroskopie (Röntgen-Photoelektronen-Spektroskopie, XPS, VG MultiLab 2000) wurde die Zusammensetzung und Wertigkeit von Elementen auf der Materialoberfläche analysiert.
Elektrochemische Prüfung
Das aktive Kathodenmaterial Super-P und Polyvinylidenfluorid wurden in einem Massenverhältnis von 8:1:1 gemischt, in N-Methyl-2-pyrrolidon (NMP) dispergiert und für 12 h magnetisch gerührt, es bildete sich eine einheitliche Aufschlämmung , auf Aluminiumfolie aufgetragen und schließlich in einem Vakuumofen bei 120 °C für 12 h getrocknet, um NMP zu entfernen. Schneiden Sie die Aluminiumfolie in ein positives Elektrodenblatt mit einem Durchmesser von 10 mm, und die Massenbelastung des geschnittenen positiven Elektrodenblatts beträgt 2 bis 3 mg/cm2. Als Gegenelektrode und Separator für Halbzellen (bzw. Vollzellen) wurden Lithiumbleche (oder Graphit) und poröse Polypropylenmembranen (Celgard 2500) verwendet. Als Elektrolyte in Halb- und Vollzelle werden 1 mol/L LiPF6-Lösungen gelöst in Ethylencarbonat/Ethylmethylcarbonat/Diethylcarbonat (Volumenverhältnis 1:1:1) verwendet. Montieren Sie CR2016-Knopfzellen in einem Argon-Handschuhfach. Elektrochemische Lade-/Entladeexperimente wurden bei Intervallen von 2,7–4,3 V und 2,7–4,5 V unter Verwendung eines Batterietestsystems durchgeführt. Verwendung einer elektrochemischen Workstation zum Testen der zyklischen Voltammetrie (CV) bei 0,1 mV/s und 2,7–4,3 V.
Resultate und Diskussion
Abbildung 1(a) zeigt die XRD-Muster von NCA- und NCA@nCP-Materialien. Die XRD-Muster aller Materialien zeigen ähnliche Spitzenpositionen und Spitzenformen und keine anderen Verunreinigungsspitzen. Außerdem waren die (006)/(102)- und (108)/(110)-Beugungspeaks des Materials nach dem Beschichten und vor dem Beschichten offensichtlich geteilt, was anzeigt, dass die CP-Beschichtung die ursprüngliche Schichtstruktur des NCA-Materials nicht veränderte. Da der Ionenradius (0,069 nm) von Ni2+ in solchen Materialien auf Nickelbasis ähnlich dem von Li+ (0,076 nm) ist, kann es leicht zur Lithiumschicht wandern, was zu einer gemischten Anordnung von Li/Ni führt, und die Verhältnis von I(003)/I(104) kann das Li/Ni-Mischphänomen des Materials aufdecken. Die Ergebnisse zeigen, dass, wenn I(003)/I(104) größer als 1,2 ist, das Material auf Nickelbasis normalerweise als Material mit einer wohlgeordneten Schichtstruktur angesehen wird. und je größer I(003)/I(104) ist, desto kleiner ist der Grad der Li/Ni-Mischung. Wie in Tabelle S1 gezeigt, sind I(003)/I(104) sowohl von NCA- als auch von NCA@nCP-Materialien größer als 1,2, von denen NCA@1CP am höchsten ist (2,261), was größer als NCA (1,426) ist. was anzeigt, dass die CP-Beschichtung das Li von NCA hemmt. /Ni gemischte Anordnung. Abbildung 1(b) und Abbildung S1 sind die verfeinerten XRD-Ergebnisse von NCA@1CP bzw. NCA und NCP@nCP. Alle Beugungspeaks gehören zu der hexagonalen Schichtstruktur vom O3-Typ. Der Unterschied in den Gitterparametern zwischen NCA und NCA@nCP ist gering, was darauf hindeutet, dass das CP nicht in das Gitter des NCA-Materials eintritt (Tabelle S2), die Fehlerfaktoren (Rp und Rwp) der Verfeinerung gering sind und die Anpassungszuverlässigkeit ist hoch. die I(003)/I(104) von NCA- und NCA@nCP-Materialien sind größer als 1,2, von denen NCA@1CP am höchsten ist (2,261), was größer ist als NCA (1,426), was anzeigt, dass die CP-Beschichtung inhibiert das Li von NCA. /Ni gemischte Anordnung. Abbildung 1(b) und Abbildung S1 sind die verfeinerten XRD-Ergebnisse von NCA@1CP bzw. NCA und NCP@nCP. Alle Beugungspeaks gehören zu der hexagonalen Schichtstruktur vom O3-Typ. Der Unterschied in den Gitterparametern zwischen NCA und NCA@nCP ist gering, was darauf hindeutet, dass das CP nicht in das Gitter des NCA-Materials eintritt (Tabelle S2), die Fehlerfaktoren (Rp und Rwp) der Verfeinerung gering sind und die Anpassungszuverlässigkeit ist hoch. die I(003)/I(104) von NCA- und NCA@nCP-Materialien sind größer als 1,2, von denen NCA@1CP am höchsten ist (2,261), was größer ist als NCA (1,426), was anzeigt, dass die CP-Beschichtung inhibiert das Li von NCA. /Ni gemischte Anordnung. Abbildung 1(b) und Abbildung S1 sind die verfeinerten XRD-Ergebnisse von NCA@1CP bzw. NCA und NCP@nCP. Alle Beugungspeaks gehören zu der hexagonalen Schichtstruktur vom O3-Typ. Der Unterschied in den Gitterparametern zwischen NCA und NCA@nCP ist gering, was darauf hindeutet, dass das CP nicht in das Gitter des NCA-Materials eintritt (Tabelle S2), die Fehlerfaktoren (Rp und Rwp) der Verfeinerung gering sind und die Anpassungszuverlässigkeit ist hoch. Abbildung 1(b) und Abbildung S1 sind die verfeinerten XRD-Ergebnisse von NCA@1CP bzw. NCA und NCP@nCP. Alle Beugungspeaks gehören zu der hexagonalen Schichtstruktur vom O3-Typ. Der Unterschied in den Gitterparametern zwischen NCA und NCA@nCP ist gering, was darauf hindeutet, dass das CP nicht in das Gitter des NCA-Materials eintritt (Tabelle S2), die Fehlerfaktoren (Rp und Rwp) der Verfeinerung gering sind und die Anpassungszuverlässigkeit ist hoch. Abbildung 1(b) und Abbildung S1 sind die verfeinerten XRD-Ergebnisse von NCA@1CP bzw. NCA und NCP@nCP. Alle Beugungspeaks gehören zu der hexagonalen Schichtstruktur vom O3-Typ. Der Unterschied in den Gitterparametern zwischen NCA und NCA@nCP ist gering, was darauf hindeutet, dass das CP nicht in das Gitter des NCA-Materials eintritt (Tabelle S2), die Fehlerfaktoren (Rp und Rwp) der Verfeinerung gering sind und die Anpassungszuverlässigkeit ist hoch.
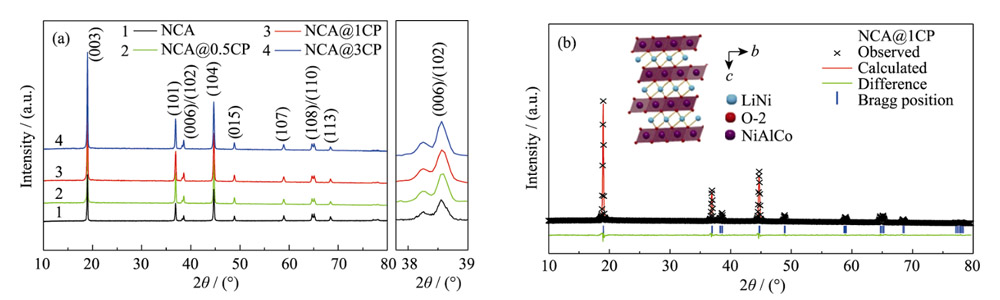
Abb. 1 (a) XRD-Muster von NCA und NCA@nCP (n=0,5 , 1, 3) und (b) Rietveld-Verfeinerungsergebnisse von NCA@1CP
Abbildung 2(a) und Abbildung S2 sind die SEM-Charakterisierungsergebnisse von NCA@1CP- bzw. NCA- und NCP@nCP-Materialien. Die Morphologie aller Materialien ist kugelförmig, und die kugelförmige Morphologie der Materialien ändert sich nach der CP-Beschichtung nicht. TEM-Charakterisierungsergebnisse zeigen, dass das NCA-Material eine gute Kristallinität mit einem Gitterrandabstand von 0,47 nm aufweist, was der (003)-Kristallebene von NCA entspricht (Fig. 2(b)). Im Gegensatz dazu wurde eine amorphe Mantelschicht mit einer Dicke von etwa 5 nm deutlich auf der Oberfläche des NCA@1CP-Materials beobachtet (Fig. 2(c)), was anzeigt, dass das CP effektiv auf der Oberfläche des NCA-Materials aufgetragen war. Die Elementverteilung von NCA@1CP- und NCA-Materialien wurde mit EDS analysiert (Abbildung 2 (d) und Abbildung S3).

Abb. 2 (a) SEM-Bild von NCA@1CP, hochauflösende TEM-Bilder von (b) NCA und (c) NCA@1CP und (d) EDS-Elementkartierungen von NCA@1CP
Die Zusammensetzung und der Wertigkeitszustand von Elementen auf der Oberfläche der Materialien wurden durch XPS-Analyse von NCA- und NCA@1CP-Materialien bestimmt. Wie in Abbildung 3(a) gezeigt, werden in NCA vier Elemente von Ni, Co, Al und O nachgewiesen, während zusätzlich zu den obigen vier Elementen auch Ca- und P-Elemente in NCA@1CP nachgewiesen werden, was beweist, dass CP es ist erfolgreich auf die Oberfläche von NCA-Material aufgetragen. Wie in Fig. 3(b) gezeigt, gehören die zwei Peaks bei 856,5 und 873,3 eV zu Ni2p3/2 bzw. Ni2p1/2. Der Ni2p3/2-Peak kann weiter an zwei Unterpeaks bei 854,7 und 855,8 eV angepasst werden, die zweiwertigem bzw. dreiwertigem Ni entsprechen. Die Peakfläche von zweiwertigem Ni in NCA@1CP-Material ist kleiner als die in NCA-Material, was darauf hindeutet, dass die CP-Beschichtungsmodifikation den Gehalt an zweiwertigem Ni in NCA verringert und bis zu einem gewissen Grad das Li/Ni-Mischen hemmen kann. Die beiden Peaks bei 795,5 und 779,9 eV gehören zu Co2p1/2 bzw. Co2p3/2, was darauf hinweist, dass Co dreiwertig ist (Abbildung 3(c)), während der Al2p3/2-Peak bei 73,1 eV gut mit dem dreiwertigen Al-Peak übereinstimmt ( Abbildung 3(d)). Außerdem wurden die Peaks bei 133,4 eV, die P2p entsprechen (Abbildung 3(e)) und 347,0 und 350,6 eV, die Ca2p3/2 und Ca2p1/2 entsprechen (Abbildung 3(f)), auf der NCA@1CP-Materialoberfläche nachgewiesen, während im NCA-Material wurden keine P- und Ca-Peaks nachgewiesen.
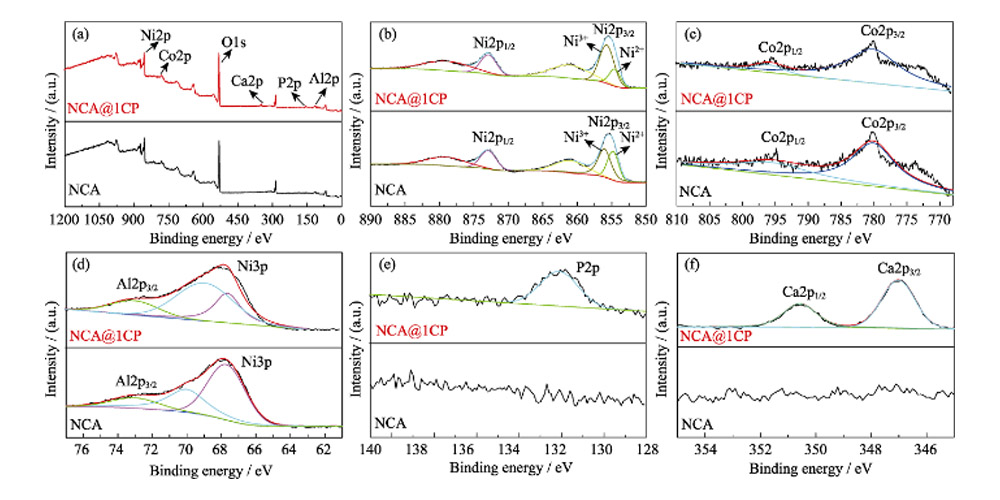
Abb. 3 (a) Vollbild, (b) Ni2p, (c) Co2p, (d) Al2p, (e) P2p und (f) Ca2p XPS-Spektren für NCA und NCA@1CP
In Abbildung 4 (a, b) und Abbildung S4 zeigen die CV-Kurven der ersten drei Windungen der Lithiumionen-Halbzelle, die mit NCA- und NCA@nCP-Materialien als positive Elektroden zusammengebaut sind, dass es im Test drei Paare unterschiedlicher REDOX-Peaks gibt Intervall von 2,7–4,3 V, was verschiedenen Phasenübergangsprozessen entspricht: Im Prozess der Li+-Extraktion stellt der Oxidationspeak bei 3,83 V den Übergang von der hexagonalen Phase zur monoklinen Phase (H1-M) dar, und die Oxidationspeaks bei 4,01 und 4,20 V repräsentiert den Übergang von der monoklinen Phase zur hexagonalen Phase (M-H2) bzw. den Übergang von der hexagonalen Phase zur hexagonalen Phase (H2-H3). Die Reduktionsspitzen des Li+-Einbettungsprozesses sind 3,64 V, 3,96 V bzw. 4,15 V. Die Potentialdifferenz zwischen dem Oxidationspeak und dem Reduktionspeak während des Zyklus kann die elektrochemische Kinetik des Materials widerspiegeln. Die Potentialdifferenz des anfänglichen REDOX-Peaks von NCA beträgt 0,185 V, was größer ist als die von NCA@0,5CP (0,154 V), NCA@1CP (0,112 V) und NCA@3CP (0,143 V) nach dem Beschichten. Die Polarisierung von NCA@1CP-Material ist während der elektrochemischen Lithium-Inkalation/Lithium-Entfernung am geringsten. FEIGE. 4(c) zeigt die anfänglichen Lade- und Entladekurven einer Lithiumionen-Halbzelle, die mit NCA- und NCA@nCP-Material als positive Elektrode bei 0,2 C (1 C = 200 mA/g) und 2,7–4,3 V zusammengesetzt ist. Die anfängliche Entladekapazität von NCA beträgt 212,4 mAh/g, während die von NCA@nCP(n = 0,5, 1, 3) 211,1, 210,4 bzw. 203,3 mAh/g beträgt. Abbildung 4(d) zeigt die Halbzellenzyklusleistung von NCA- und NCA@nCP-Material bei 1 °C und 2,7–4,3 V. Um das Elektrodenmaterial vollständig zu aktivieren, wurde die Batterie zuerst bei 0,2 C für 2 Zyklen geladen und entladen, NCA@1CP bei 1 C Entladung spezifische Kapazität von 204,8 mAh/g, 100 Zyklen nach 187,5 mAh/g, die entsprechende Kapazitätsretention beträgt 91,5 %. Die spezifische Kapazität von NCA beträgt jedoch 203,2 mAh/g bei 1 °C und nur 168,0 mAh/g nach 100 Zyklen (die Kapazitätserhaltungsrate beträgt 82,6 %). Die obigen Ergebnisse zeigen, dass das NCA@1CP-Material sowohl bei niedrigen als auch bei hohen Grenzspannungen eine hervorragende Zyklenstabilität aufweist. Abbildung 4(f) zeigt die Langzyklusleistung von NCA- und NCA@1CP-Material bei 2 °C und 2,7–4,3 V. Die anfängliche Entladekapazität von NCA@1CP beträgt 184,9 mAh/g, und nach 300 Zyklen verbleiben 153,4 mAh/g, was 82,9 % des Anfangswerts entspricht. Die spezifische Anfangsentladungskapazität von NCA bei 2C beträgt jedoch 173,5 mAh/g und nur 115. 3 mAh/g nach 300 Zyklen, das sind nur noch 66,4 % des Ausgangswertes. Abbildung S5(a~c) zeigt die Ratenleistung von NCA- und NCA@nCP-Materialien im Bereich von 2,7 bis 4,3 V. Die Ratenleistung von NCA ist schlecht, insbesondere die spezifische Kapazität von 105,1 mAh/g bei einer ultrahohen Rate von 10 °C. Im Gegensatz dazu hat NCA@1CP eine spezifische Entladungskapazität von bis zu 130,4 mAh/g bei 10 °C, was eine hervorragende Ratenleistung zeigt.
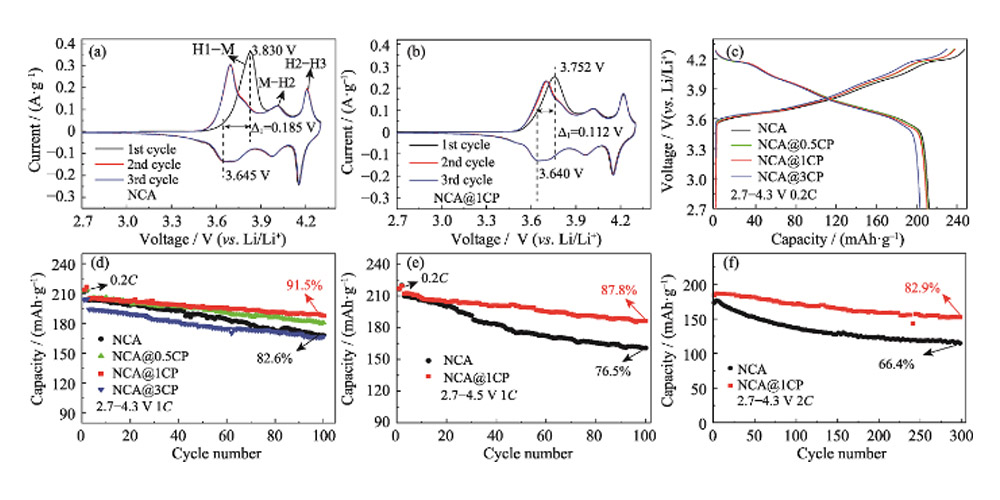
Abb. 4 CV-Kurven für (a) NCA und (b) NCA@1CP; (c) Anfängliche Lade-Entlade-Kurven unter 2,7-4,3 V bei 0,2 C und (d) Zykleneigenschaften unter 2,7-4,3 V bei 1 C für NCA und NCA@nCP; Zykluseigenschaften für NCA und NCA@1CP (e) unter 2,7–4,5 V bei 1 °C und (f) unter 2,7–4,3 V bei 2 °C
Die Entwicklung der Kristallstruktur von NCA- und NCA@1CP-Materialien während des Lade-Entlade-Zyklus wurde in Echtzeit durch In-situ-XRD überwacht (Abb. 5). Wie in 5(a, b) gezeigt, geht der Kristall während des ersten Ladezyklus auf 4,1 V von der H1-Phase in die H2-Phase über, die (003)-Beugungsspitze verschiebt sich zu einem niedrigen Winkel und der Gitterparameter c allmählich steigt. Dieses Phänomen kann der Extraktion von Lithiumionen aus dem Gitter, der verstärkten elektrostatischen Abstoßung zwischen den Übergangsmetallschichten und dem größeren Zwischenschichtabstand zugeschrieben werden. Nach weiterer Aufladung wechselt der Kristall von der H2-Phase in die H3-Phase, was zu einer scharfen Verschiebung des (003)-Beugungspeaks zu einem hohen Winkel und einer scharfen Kontraktion des Gitterparameters c führt. Dies kann zurückzuführen sein auf: (1) Die kovalente Natur der Ni4+-O2-Bindung in der Übergangsmetallschicht wird verstärkt, die elektrostatische Abstoßung zwischen den Übergangsmetallschichten wird geschwächt und der Zwischenschichtabstand ist deutlich kleiner. (2) Die kontinuierliche Extraktion von Lithiumionen zwischen Übergangsmetallschichten schwächt die Stützwirkung und verringert den Zwischenschichtabstand. Die maximale Winkelverschiebung des (003)-Beugungspeaks des NCA-Materials während des H2-H3-Phasenübergangs beträgt 0,76° (Fig. 5(e)). Obwohl das NCA@1CP-Material auch den H2-H3-Phasenübergangsprozess zeigt (Fig. 5 (c, d)). Die maximale Winkelverschiebung des (003)-Beugungspeaks beträgt jedoch nur 0,57° (Fig. 5(f)). 5(g) zeigt die Entwicklungskurven des Gitterparameters c während der Delithiierung von NCA- und NCA@1CP-Materialien. Die Schrumpfung des Gitterparameters c von NCA@1CP (3. 5 %) ist kleiner als die von NCA (4,1 %). Es zeigt sich, dass NCA@1CP eine bessere strukturelle Stabilität aufweist. In-situ-XRD-Ergebnisse zeigen, dass die CP-Beschichtung den irreversiblen H2-H3-Phasenübergang des NCA-Materials unterdrücken kann, wodurch die elektrochemische Leistung des Materials verbessert wird.
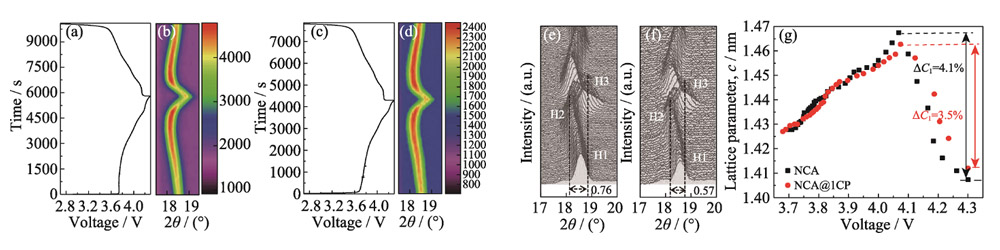
Abb. 5 Spannungs-Zeit-Variationskurven während in-situ XRD für (a) NCA und (c) NCA@1CP; In-situ-XRD-Muster für (b, e) NCA und (d, f) NCA@1CP; (g) Variationskurven des Gitterparameters c während des Ladens für NCA und NCA@1CP
Um die Auswirkung der CP-Beschichtung auf die Morphologie und Mikrostruktur von Materialien während des elektrochemischen Prozesses umfassend zu bewerten, wurden die Polstücke von NCA- und NCA@1CP-Halbzellen nach 100 Lade-Entlade-Zyklen (1C, 2,7~4,3 V) charakterisiert . Die SEM-Charakterisierungsergebnisse zeigten, dass nur wenige Mikrorisse auf der Oberfläche des NCA@1CP-Materials auftraten, während eine große Anzahl von Rissen auf der Oberfläche des NCA-Materials auftrat und einige Partikel pulverisiert waren (Abb. S6 (a, b). ). Es zeigt, dass die CP-Überzugsschicht die Oberflächenmikrorisse und die mechanische Pulverisierung des Materials bis zu einem gewissen Grad hemmt. Abbildung S6(c–f) zeigt die XRD-Muster von NCA- und NCA@1CP-Materialien vor und nach 100 Zyklen. Die (006)- und (102)-Beugungspeaks von NCA überlappen sich nach 100 Zyklen (Abb. S6(d)). während die (006)- und (102)-Beugungspeaks von NCA@1CP nach 100 Zyklen immer noch geteilt sind (Fig. S6(f))). Es zeigt, dass die CP-Überzugsschicht die Stabilität der NCA-Struktur verbessern kann. Um die Lithium-Lagerstabilität von NCA@1CP weiter zu verifizieren, wurde eine Vollbatterie vom Münztyp mit NCA- und NCA@1CP-Materialien als positive Elektrode bzw. Graphit als negative Elektrode zusammengebaut (Abb. 6). Bei 1C (1C=200 mA/g) und 2,7~4,25 V beträgt die spezifische Anfangsentladungskapazität der NCA@1CP-Vollzelle 201,4 mAh/g. Nach 70 Zyklen behielt die spezifische Entladungskapazität 84,6 % des Anfangswerts bei (Fig. 6(a)). Jedoch beträgt die anfängliche spezifische Entladungskapazität der NCA-Vollzelle 198,6 mAh/g, und die spezifische Entladungskapazität nach 70 Zyklen beträgt nur 65,6 % des Anfangswerts.
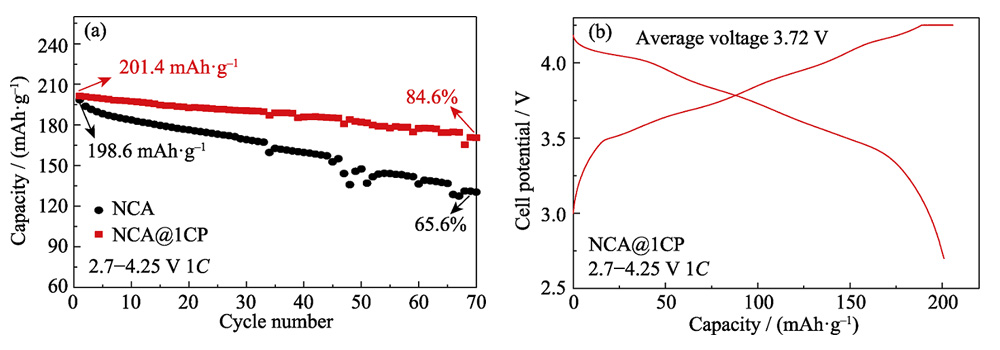
Abb. 6 (a) Zykluseigenschaften von Vollzellen sowohl NCA als auch NCA@1CP als Kathode, Graphit als Anode unter 2,7–4,25 V bei 1C und (b) Lade-Entlade-Kurven des zweiten Zyklus für NCA@1CP in Vollzelle
Fazit
In dieser Studie wurden NCA@1CP-Kathodenmaterialien durch eine einfache nasschemische Strategie hergestellt, die die elektrochemische Lithium-Lagerstabilität von NCA-Materialien deutlich verbesserte. Das NCA@1CP-Material weist eine Kapazitätserhaltungsrate von 91,5 % nach 100 Zyklen bei 1 °C auf und zeigt selbst bei einer hohen Rate von 2 °C eine ultralange Lebensdauer von über 300 Zyklen.
Die CP-Beschichtung verlängert die Lebensdauer von NCA-Kathodenmaterialien erheblich, hauptsächlich aufgrund der folgenden Aspekte:
(1) Die Einführung der CP-Überzugsschicht verringert den Grad der Li/Ni-Mischanordnung.
(2) Die CP-Beschichtung verringert die Schrumpfung des Gitterparameters c und unterdrückt den irreversiblen Phasenübergang von H2-H3.
(3) Die CP-Überzugsschicht hemmt die Mikrorisse und die mechanische Pulverisierung der Materialoberfläche.
Diese Studie zeigt, dass die CP-Überzugsschicht ein großes Anwendungspotenzial bei der Oberflächenmodifikation von Ultrahochnickel-Kathodenmaterialien hat, um die Stabilität der Lithiumspeicherung zu verbessern, und liefert eine neue Idee für die Optimierungsstrategie der elektrochemischen Stabilität von Ultrahochnickel-Kathodenmaterialien .
Ergänzungsmaterial

Abb. S2 SEM-Bilder von (a, b) NCA, (c, d) NCA@0.5CP und (e, f) NCA@3CP
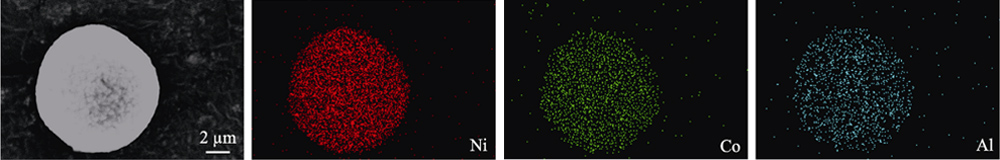
Abb. S3 EDS-Elementkartierungen von NCA
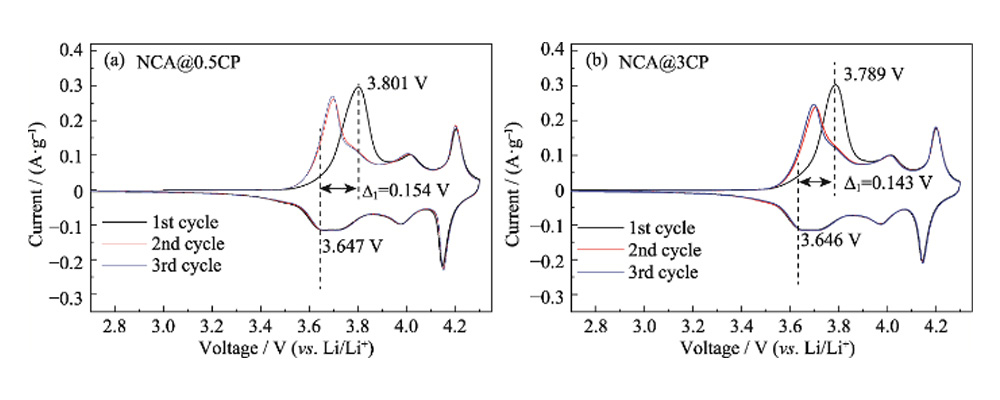
Abb. S4 CV-Kurven für (a) NCA@0,5CP und (b)NCA@3CP
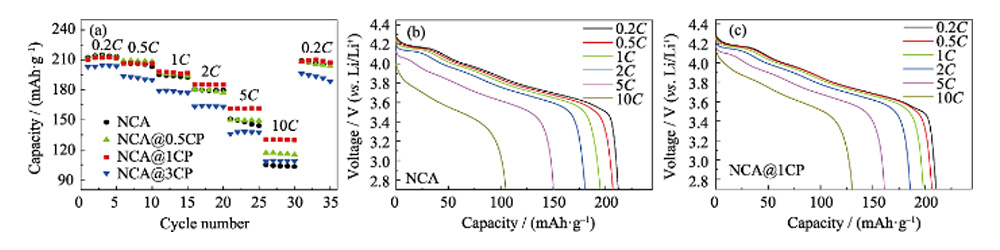
Abb. S5 (a) Ratenleistung für NCA, NCA@0,5CP, NCA@1CP und NCA@3CP; Entsprechende Entladungskurven während Ratentests von (b) NCA und (c) NCA@1CP
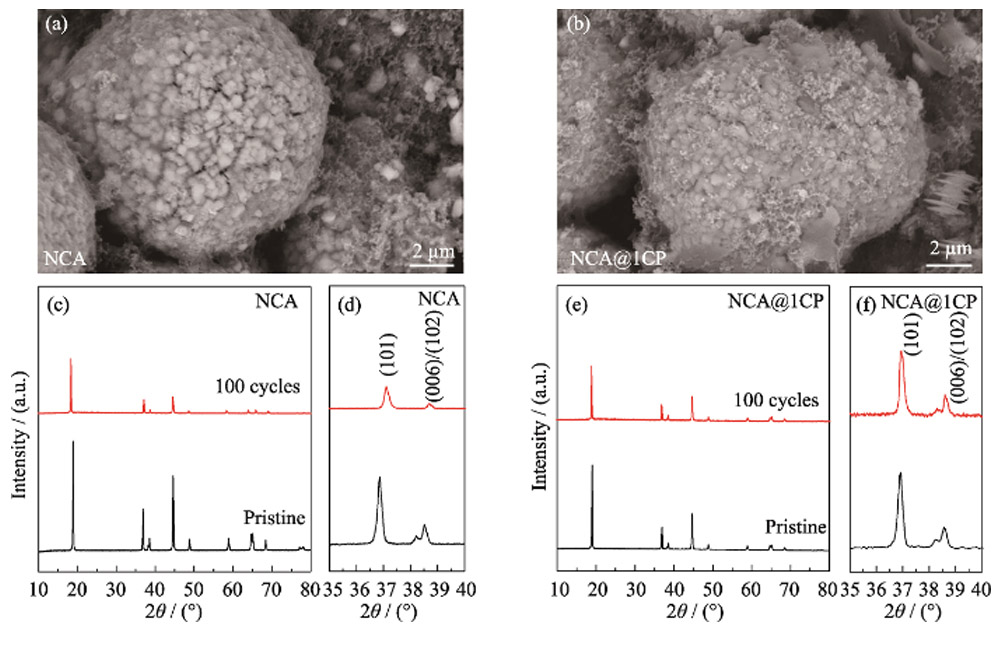
Abb. S6 (a, b) SEM-Bilder und (cf) XRD-Muster von NCA und NCA@1CP nach 100 Zyklen unter 2,7-4,3 V bei 1C
|
Probe
|
NCA
|
NCA@0,5CP
|
NCA@1CP
|
N
CA@3CP
|
|
I(003)/I(104)
|
1.426
|
2.120
|
2.261
|
1.981
|
Tabelle S2 Gitterparameter von NCA, NCA@0.5CP, NCA@1CP und NCA@3CP, berechnet aus XRD-Rietveld-Verfeinerung
| Probe | ein/nm | c/nm | V/nm3 | c/a | Rwp | Rp |
| NCA | 0,287398 | 1.421071 | 0,101652 | 4.944609 | 7.13 | 4.18 |
| NCA@0,5CP | 0,287296 | 1.420733 | 0,101556 | 4,9451 88 | 6.63 | 4.73 |
| NCA@1CP | 0,287286 | 1.42044 | 0,101527 | 4.944341 | 5.86 | 4.39 |
| NCA@3CP | 0,287305 | 1.420646 | 0,101556 | 4.944731 | 6.74 | 4.82 |



