Kategorien
neuer Blog
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
- Hauptursachen für Undichtigkeiten an der Zellversiegelung von Beuteln
- Formation und Grading in der Lithium-Ionen-Batterieherstellung
Tags
Amorpher LiSiON-Dünnschichtelektrolyt für Festkörper-Dünnschicht-Lithiumbatterien
Autor: XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
Schule für Materialien Wissenschaft und Technik, Nanjing Universität für Wissenschaft und Technologie, Nanjing 210094, China
Zusammenfassung
Als Ideal gilt eine All-Solid-State-Dünnschicht-Lithiumbatterie (TFLB). Stromquelle für mikroelektronische Geräte. Allerdings ist die relativ geringe ionische Die Leitfähigkeit des amorphen Festkörperelektrolyten begrenzt die Verbesserung elektrochemische Leistung für TFLB. In dieser Arbeit handelt es sich um amorphes Lithium-Silizium Oxynitrid (LiSiON)-Dünnfilme werden durch Magnetronsputtern hergestellt Festkörperelektrolyt für TFLB. Bei optimierten Abscheidungsbedingungen ist die Der dünne LiSiON-Film weist bei Raum eine hohe Ionenleitfähigkeit von 6,3×10-6 Sâcm-1 auf Temperatur und ein breites Spannungsfenster über 5 V, was ihn zu einem geeigneten dünnen Film macht Elektrolyt für TFLB. Ein MoO3/LiSiON/Li TFLB ist Konstruiert auf Basis des LiSiON-Dünnschichtelektrolyten mit großem spezifischem Gewicht Kapazität (282 mAhâg-1 bei 50 mAâg-1), guter Wert Kapazität (50 mAhâg-1 bei 800 mAâg-1) und akzeptabel Lebensdauer (78,1 % Kapazitätserhalt nach 200 Zyklen), was die zeigt Machbarkeit dieses Elektrolyten für praktische Anwendungen.
Schlüsselwörterï¼ LiSiON; dünner Film Elektrolyt; Festkörper-Lithiumbatterie; Dünnschichtbatterie
Die rasante Entwicklung der Mikroelektronikindustrie, wie z Mikroelektromechanische Systeme (MEMS), Mikrosensoren, intelligente Karten und implantierbare mikromedizinische Geräte führen zu einer steigenden Nachfrage nach integrierten Mikro-Energiespeicher[1,2]. Zu den verfügbaren Batterietechnologien gehören Als Ideal gilt eine All-Solid-State-Dünnschicht-Lithiumbatterie (TFLB). Stromquelle für mikroelektronische Geräte aufgrund ihrer hohen Sicherheit, geringen Größe, Power-on-Chip-Design, lange Lebensdauer und niedrige Selbstentladungsrate. Als einer von Als Schlüsselkomponenten in TFLB spielt der Festkörper-Dünnschichtelektrolyt eine entscheidende Rolle Rolle bei der Bestimmung der Eigenschaften von TFLB[3]. Daher, Die Entwicklung von Hochleistungs-Festkörper-Dünnschichtelektrolyten ist immer eine Herausforderung wichtiges Ziel für die Entwicklung von TFLB. Derzeit am weitesten verbreitet Der Elektrolyt in TFLB ist amorphes Lithiumphosphoroxynitrid (LiPON), das Hat eine mäßige Ionenleitfähigkeit (2×10-6 Sâcm-1), eine niedrige elektronische Leitfähigkeit (~10-14 Sâcm-1) und einen breiten Spannungsbereich Fenster (~5,5 V) und gute Kontaktstabilität mit Lithium[4,5]. Allerdings ist es Die Ionenleitfähigkeit ist relativ gering, was die zukünftige Entwicklung von behindert Hochleistungs-TFLB für die kommende Ära des Internets der Dinge (IoT)[6]. So ist es Es ist dringend erforderlich, neue Dünnschichtelektrolyte mit erhöhter Ionenleitfähigkeit zu entwickeln. sowie großes Spannungsfenster und gute Kontaktstabilität mit Lithium für TFLB der nächsten Generation.
Zu den verschiedenen anorganischen Festkörperelektrolytmaterialien gehört der Feststoff Li2O-SiO2 Lösungssystem und ihre deuterogenen Phasen wurden als potenziell dünn identifiziert Filmelektrolyten aufgrund ihrer schnellen dreidimensionalen Lithiumleitung Kanäle[7]. Zum Beispiel Chen et al.[8] gemeldet dass der Al-substituierte Festelektrolyt Li4,4Al0,4Si0,6O4-0,3Li2O eine hohe Ionenleitfähigkeit aufweist 5,4Ã10-3 Sâcm-1 bei 200 â. Adnan et al.[9] fand die Li4Sn0.02Si0.98O4-Verbindung besitzt bei Umgebungstemperatur einen maximalen Leitfähigkeitswert von 3,07Ã10-5 Sâcm-1. Jedoch, Frühere Arbeiten zu Li2O-SiO2-Elektrolytsystemen konzentrierten sich hauptsächlich auf Pulver Materialien mit hoher Kristallinität, obwohl nur über sehr begrenzte Arbeiten berichtet wurde ihre amorphen Dünnfilm-Gegenstücke für TFLB. Da TFLB typischerweise ist aufgebaut durch Abscheiden dünner Filme aus Kathoden-, Elektrolyt- und Anodenschicht Schicht muss der Elektrolytfilm bei relativ niedriger Temperatur hergestellt werden um die ungünstigen Wechselwirkungen zwischen Kathode und Elektrolyt zu vermeiden, die zu Rissen und Kurzschlüssen des TFLB[1,2] führen. Daher, Entwicklung eines Li2O-SiO2-Elektrolyten mit amorphen Merkmalen, hergestellt bei niedrigen Temperaturen Die Temperatur ist wichtig für TFLB. Obwohl neuere Arbeiten[6] zeigen dass durch amorphes Li-Si-P-O-N eine hohe Lithiumionenleitfähigkeit von 2,06×10-5 Sâcm-1 erreicht werden kann Dünnfilm, seine Kontaktstabilität mit den Elektroden und elektrochemisch Die Stabilität von TFLB muss noch untersucht werden. Daher ist es kritisch Es ist wichtig, leistungsstarke Dünnschichtelektrolyte auf Li2O-SiO2-Basis zu entwickeln demonstrieren seine tatsächliche Anwendung in TFLB.
In dieser Arbeit wurde ein dünner Film aus amorphem Lithium-Silizium-Oxinitrid (LiSiON) verwendet hergestellt durch Hochfrequenz-(RF)-Magnetronsputtern bei Raumtemperatur und als Festkörperelektrolyt für TFLB untersucht. Die Sputterleistung und die Der Fluss des N2/Ar-Arbeitsgases wurde optimiert, um die besten Abscheidungsbedingungen zu erzielen für den LiSiON-Dünnfilm. Darüber hinaus soll die Anwendbarkeit demonstriert werden optimierter LiSiON-Elektrolyt für TFLB, eine MoO3/LiSiON/Li-Vollzelle wurde konstruiert und ihre Die elektrochemische Leistung wurde systematisch untersucht.
1 Experimentell
1.1 Herstellung von LiSiON-Dünnfilmen
LiSiON-Dünnfilme wurden durch HF-Magnetronsputtern hergestellt (Kurt J. Lesker) unter Verwendung eines Li2SiO3-Targets (76,2 mm Durchmesser) bei Raumtemperatur für 12 Std. Vor der Abscheidung wurde der Druck in der Kammer auf weniger als reduziert 1Ã10-5 Pa. Der Abstand vom Ziel zum Untergrund betrug 10 cm. Die Proben werden unter einer HF-Leistung von 80, 100 und 120 W bei einem Fluss von 90 sccm N2 abgeschieden markiert als Probe LiSiON-80N9, LiSiON-100N9 bzw. LiSiON-120N9. Und Die Proben wurden unter einer HF-Leistung von 100 W bei einem Fluss von 90 sccm N2 und 10 abgeschieden sccm Ar, 90 sccm N2 und 50 sccm Ar, 50 sccm N2 und 50 sccm Ar sind als Probe LiSiON-100N9A1, LiSiON-100N9A5 und gekennzeichnet LiSiON-100N5A5 bzw..
Der MoO3-Film wurde mit einem reaktiven Gleichstrommagnetron hergestellt Sputtern (Kurt J. Lesker) mit einem Mo-Target aus reinem Metall (76,2 mm Durchmesser) gemäß unserem vorherigen Bericht[10]. Der Abstand vom Ziel zum Substrat betrug 10 cm und DC Die Sputterleistung betrug 60 W. Die Abscheidung erfolgte auf dem Substrat Temperatur von 100 °C für 4 Stunden bei einem Fluss von 40 sccm Ar und 10 sccm O2, gefolgt von einer In-situ-Glühbehandlung bei 450 °C für 1 Stunde. Anschließend wurde LiSiON-100N9A1 auf dem MoO3-Film abgeschieden Elektrolyt. Danach entstand ein metallischer Lithiumfilm von etwa 2 µm Dicke durch thermische Vakuumverdampfung auf dem LiSiON-Film abgeschieden (Kurt J. Lesker). Der letzte Herstellungsschritt umfasste die Abscheidung von Cu-Stromkollektor und Der Kapselungsprozess.
Die Kristallstrukturen von Die Proben wurden durch Röntgenbeugung (XRD, Bruker D8 Advance) charakterisiert. Die Morphologien und Mikrostrukturen der Proben wurden feldspezifisch charakterisiert Emissions-Rasterelektronenmikroskop (FESEM, FEI Quanta 250F), ausgestattet mit energiedispersive Röntgenspektroskopie (EDS). Die elementaren Zusammensetzungen der Die Proben wurden mittels Massenspektrometrie mit induktiv gekoppeltem Plasma (ICP-MS) analysiert. Agilent 7700X). Die chemische Zusammensetzung und Bindungsinformationen der Proben wurden mittels Röntgenphotoelektronenspektroskopie (XPS, Escalab 250XI, Thermo) gemessen Wissenschaftlich).
1.4 Elektrochemische Messungen
Die Ionenleitfähigkeit des LiSiON-Dünnschichtelektrolyten wurde gemessen unter Verwendung einer Sandwichstruktur aus Pt/LiSiON/Pt. Die elektrochemische Impedanz Spektroskopie (EIS) (von 1000 kHz bis 0,1 Hz mit einer möglichen Amplitude von 5 mV) und Cyclovoltammetrie (CV)-Messungen der Proben wurden am durchgeführt Biologische elektrochemische Workstation VMP3. Galvanostatisches Laden/Entladen (GCD) Die Messung des MoO3/LiSiON/Li-TFLB wurde mit einem Neware BTS4000 durchgeführt Batteriesystem in einer mit Argon gefüllten Handschuhbox bei Raumtemperatur. Ein Sartorius Zur Bestimmung wurde eine Analysenwaage (CPA225D, mit einer Auflösung von 10 μg) verwendet die Massenbeladung der Elektrode und die Massenbeladung des MoO3-Films etwa 0,4 mgâcm-2.
2 Ergebnisse und Diskussion
Wie im optischen Bild in Abb. 1(a) gezeigt, a Das Li2SiO3-Target wurde zur Herstellung eines LiSiON-Dünnfilms verwendet. Das XRD-Ergebnis in Abb. 1(a) zeigt, dass das Ziel hauptsächlich aus Li2SiO3 (JCPDS) besteht 83-1517)-Phase und Neben-SiO2-Phase. Die ICP-MS-Messung zeigt an, dass die atomare Das Verhältnis von Li : Si beträgt im Target etwa 1,79 : 1. Transparent, amorph, dünn Für die typische Probe LiSiON-100N9A1 wurde nach dem Sputtern ein Film erhalten Ziel (Abb. 1(b)). Die Dicke der typischen Probe LiSiON-100N9A1 gemessen von Das FESEM-Querschnittsbild in Abb. 1(c) ist etwa 1,2 μm, was auf eine Wachstumsrate von etwa 100 nmâh-1 unter hinweist dieser Zustand. Wie im Draufsicht-FESEM-Bild in Abb. 1(d) gezeigt, ist das Die Oberfläche des LiSiON-Dünnfilms ist sehr glatt und dicht ohne Risse oder Risse Nadellöcher, was es zu einem geeigneten Festelektrolyten für TFLB macht, um Kurzschlüsse zu vermeiden und Sicherheitsproblem.
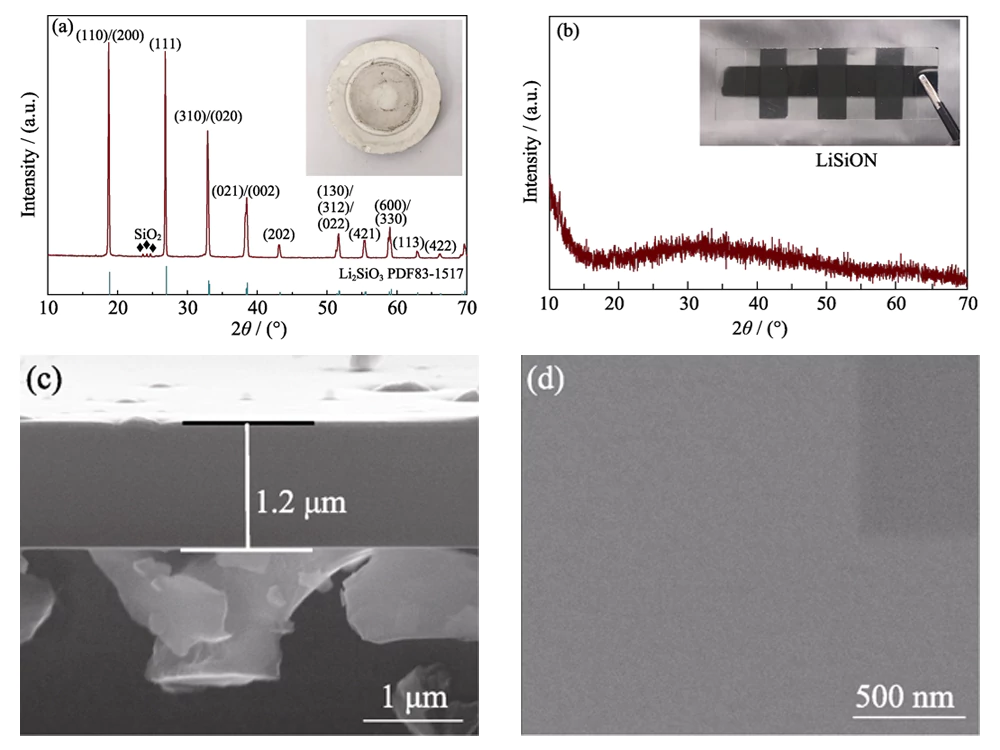
Abb. 1 (a) XRD-Muster und optisches Bild des Li2SiO3 Targets; (b) XRD-Muster und optisches Bild von typische Probe LiSiON-100N9A1; (c) Querschnitt- und (d) Draufsicht-FESEM-Bilder der typischen Probe LiSiON-100N9A1
Zur Untersuchung der chemischen Zusammensetzung wurde eine XPS-Analyse durchgeführt Bindungsinformationen des Li2SiO3-Targets und der typischen Probe LiSiON-100N9A1. Die XPS-Umfrage Scan-Spektren in Abb. 2(a) zeigen das Vorhandensein von Li-, Si- und O-Elementen im Li2SiO3-Target und die Einführung des N-Elements in den LiSiON-Dünnfilm. Das Atomverhältnis von Laut XPS-Ergebnis beträgt N : Si im LiSiON-Dünnfilm etwa 0,33 : 1. Kombiniert mit dem entsprechenden Atomverhältnis (1,51 : 1), das durch das ICP-MS erhalten wurde Messung beträgt die Stöchiometrie der typischen Probe LiSiON-100N9A1 bestimmt als Li1,51SiO2,26N0,33. Verglichen mit dem einzelnen Si-Si-Peak (103,2 eV) im Si2p-XPS-Spektrum auf Kernebene des Li2SiO3-Targets (Abb. 2(b)), Ein zusätzlicher Si-N-Peak (101,6 eV) kann im LiSiON-Dünnfilm beobachtet werden. was auf das Auftreten einer Nitridierung in LiSiON hindeutet[11,12]. Die O1 XPS-Spektrum auf Kernebene des Li2SiO3-Targets in Abb. 2(c) zeigt zwei Bindungsumgebungen: 531,5 eV stammt von SiOx und 528,8 eV Li2O zugeordnet. Nach der Abscheidung trat bei 530,2 eine zusätzliche Komponente auf eV kann bei LiSiON-Dünnfilmen beobachtet werden, was der Nichtverbrückung zugeordnet werden kann Sauerstoff (On) in Silikat[13,14]. Das N1s-Kern-XPS-Spektrum des LiSiON-Dünnfilms in Abb. 2(d) kann in drei Peaks entfaltet werden, darunter 398,2 eV für Si-N-Bindung, 396,4 eV für Li3N und 403,8 eV für die Nitritspezies NO2-, was den Einbau von N in die weiter bestätigt LiSiON-Netzwerk[14,15,16]. Wie schematisch in Abb. 2(e) dargestellt, ist die Durch den Einbau von N in das LiSiON-Netzwerk kann eine stärkere Vernetzung entstehen Struktur, die für eine schnelle Lithiumionenleitung von Vorteil ist[6,17].
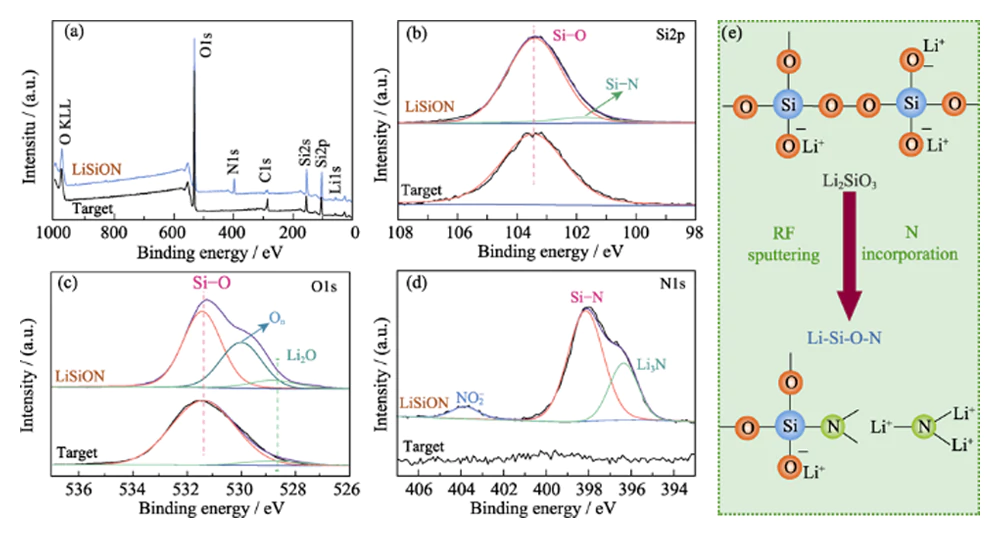
Abb. 2 (a) Survey-Scan, (b) Si2p-Kernebene, (c) O1s-Kernebene, und (d) XPS-Spektren auf N1-Kernebene des Li2SiO3-Ziels und der typischen Probe LiSiON-100N9A1; (e) Schematische Darstellung der teilweisen Strukturänderung von Li2SiO3 zu LiSiON unter Einbau von N
Zur Optimierung der Ionenleitfähigkeit und elektrochemischen Stabilität des LiSiON-Dünnfilme, verschiedene LiSiON-Dünnfilme, die durch unterschiedliche Sputterverfahren abgeschieden werden Leistungen und Arbeitsgasströme wurden hinsichtlich ihrer ionischen Eigenschaften verglichen Leitfähigkeiten und Spannungsfenster. Die Raumtemperatur-Nyquist-Diagramme des LiSiON-Dünnfilme sind in Abb. 3(a) und dargestellt die entsprechende Pt/LiSiON/Pt-Sandwichstruktur und das entsprechende Schaltbild sind dargestellt in Abb. 3(b). Als beobachtet, weisen die Nyquist-Diagramme einen einzelnen Halbkreis und ein Dielektrikum auf Kapazitätsschwanz, der für dünnschichtleitende Dielektrika charakteristisch ist mit Massenrelaxationsprozess zwischen blockierenden Kontakten[17]. Das Ionische Leitfähigkeiten (Ïi) der LiSiON-Dünnfilme können mithilfe von Gleichung berechnet werden. (1).
Ïi=d/(RA)
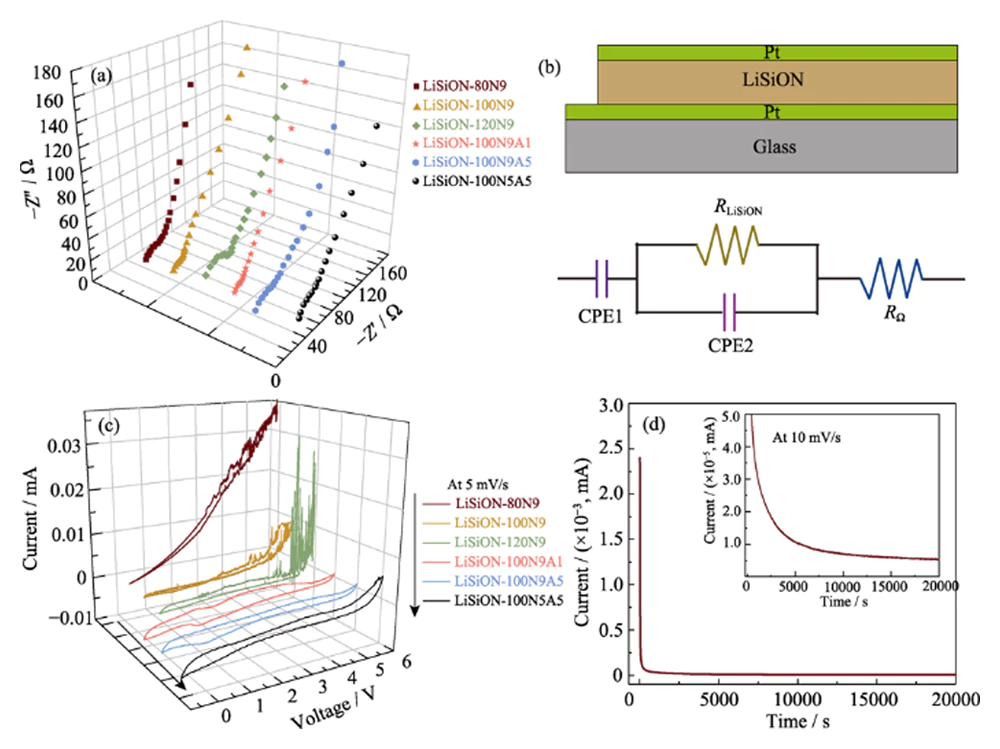
Abb. 3 (a) Spektren der elektrochemischen Impedanzspektroskopie (EIS) von die unter verschiedenen Bedingungen abgeschiedenen LiSiON-Dünnfilme; (b) Schema Darstellung der Pt/LiSiON/Pt-Sandwichstruktur und der entsprechenden Ersatzschaltbild; (c) CV-Kurven der darunter abgeschiedenen LiSiON-Dünnfilme unterschiedliche Bedingungen; (d) Chronoamperometriekurve der Probe LiSiON-100N9A1
Dabei ist d die Filmdicke, A die effektive Fläche (ca. 1 cm2) und R ist der geschätzte Filmwiderstand aus dem gemessenen Nyquist-Diagramm. Die berechneten Ionenleitfähigkeiten für diese LiSiON-Dünnfilme werden in Tabelle 1 verglichen. Wie beobachtet, ist die Ionenleitfähigkeit des abgeschiedenen LiSiON-Dünnfilms Bei einem konstanten Fluss von 90 sccm steigt N2 mit zunehmender Sputterleistung ab 80 W auf 100 W, nimmt dann ab, wenn die Sputterleistung weiter auf 120 erhöht wird W, was dem vorherigen Bericht über den LiPON-Elektrolyten ähnelt[18]. Eine Selbstverständlichkeit Ein Anstieg der Ionenleitfähigkeiten kann beobachtet werden, wenn das N2-Verhältnis in Dabei wird das Arbeitsgas mit einer konstanten Sputterleistung von 100 W gefördert Dies ist auf die erhöhte Menge an eingebautem Stickstoff zurückzuführen LiSiON mit günstigerer Umgebung für die Bewegung von Lithiumionen[5, 18]. Deutlich, Die Proben LiSiON-100N9 und LiSiON-100N9A1 zeigen die höchsten ionischen Werte Leitfähigkeiten von 7,1×10-6 bzw. 6,3×10-6 Sâcm-1, was offensichtlich höher ist als das bekannte LiPON (~2Ã10-6 Sâcm-1), zuvor berichtete amorphe LiNbO3 (~1Ã10-6 Sâcm-1)[19], LiBON (2,3Ã10- 6 Sâcm-1)[20], Li-V-Si-O (~1Ã10-6 Sâcm-1)[21], Li-La-Zr-O (4Ã10-7 Sâcm-1)[22] und Li-Si-P-O (1,6Ã10-6 Sâcm-1)[23] Elektrolytfilme, die zeigen, dass sie amorph sind LiSiON-Dünnfilm ist ein wettbewerbsfähiger Kandidat als Elektrolyt für TFLB. Das Hoch Die Ionenleitfähigkeit des LiSiON-Dünnfilms kann auf den Einbau zurückgeführt werden von N in den dünnen Film und die Bildung von Si-N-Bindungen anstelle von Si-O-Bindungen, Dies führt zu einem stärker vernetzten anionischen Netzwerk für das einfache Lithiumion Mobilität[17, 24]. Die elektrochemisch stabilen Spannungsfenster des LiSiON Dünne Filme wurden durch CV-Messung bei einer Scanrate von 5 mVâs-1 mit bewertet Spannung bis zu 5,5 V. Es ist darauf hinzuweisen, dass die Auswirkungen der Ablagerung Die Bedingung für das Spannungsfenster von LiSiON-Filmen variiert, was nicht der Fall sein kann Dies lässt sich derzeit durch einen klaren Mechanismus erklären, da keine relevanten Untersuchungen vorliegen in früheren Berichten über Dünnschichtelektrolyte[18,24-25]. Trotzdem, im Vergleich in Abb. 3(c) und Tabelle 1 zeigen die Proben LiSiON-100N9A1 und LiSiON-100N5A5 die breiteste Spannung Fenster von ~5,0 bzw. ~5,2 V, die denen von LiPON nahe kommen Elektrolyt. Daher werden sowohl die Ionenleitfähigkeit als auch das Spannungsfenster berücksichtigt In Anbetracht dessen wurde die Probe LiSiON-100N9A1 für weitere Untersuchungen ausgewählt und die Herstellung von Vollzellen. Untersuchung der Lithium-Ionen-Übertragung Zahl (Ïi) und die elektronische Leitfähigkeit (Ïe) der Probe LiSiON-100N9A1, Chronoamperometrie wurde weiterhin bei konstanter Spannung durchgeführt von 10 mV (Abb. 3(d)). Das Ïi kann nach Gl. berechnet werden. (2).
Ïi=(Ib-Ie)/Ib
wobei Ib der anfängliche Polarisationsstrom und Ie der Dauerstrom ist Zustand aktuell[18]. Der Ïi wurde mit 0,998 berechnet nahe 1, was darauf hinweist, dass die Lithiumionenleitung absolut dominant ist im Elektrolyten. Das Ïi wird durch einen gemischten Effekt der bestimmt Leitung von Ionen und Elektronen[24], die durch Gleichung ausgedrückt werden kann. (3).
Ïi=Ïi/(Ïi+Ïe)
Damit wird der Ïe der Probe LiSiON-100N9A1 berechnet 1,26Ã10-8 Sâcm-1, was im Vergleich zu seiner Ionenleitfähigkeit vernachlässigbar ist.
Tabelle 1 Vergleich der Leitfähigkeiten und Spannungen von Lithiumionen Fenster aus LiSiON-Dünnfilmen, die unter verschiedenen Bedingungen abgeschieden wurden
|
Beispiel |
Lithiumionenleitfähigkeiten |
Spannung |
|
LiSiON-80N9 |
4.6 |
~2,0 |
|
LiSiON-100N9 |
7.1 |
~3,9 |
|
LiSiON-120N9 |
2,5 |
~4.2 |
|
LiSiON-100N9A1 |
6.3 |
~5,0 |
|
LiSiON-100N9A5 |
3.0 |
~4,6 |
|
LiSiON-100N5A5 |
2.9 |
~5.2 |
Um die Machbarkeit der optimierten Probe LiSiON-100N9A1 zu überprüfen TFLB-Anwendung, MoO3/LiSiON/Li TFLB wurde weiter hergestellt. Der Querschnitt FESEM-Bild und entsprechende EDS-Kartierungsbilder des MoO3/LiSiON/Li-TFLB sind in Abb. 4(a) dargestellt. Als beobachtet, die MoO3-Kathode (ca. 1,1 µm dick) und die Li-Anode sind durch den LiSiON-Elektrolyten gut getrennt, und der LiSiON-Elektrolyt hat Enge Kontaktschnittstellen sowohl zur Kathode als auch zur Anode. Abb. 4(b) Zeigt die typische CV-Kurve des TFLB bei einer Scanrate von 0,1 mVâs-1 dazwischen an 1,5–3,5 V, was ein Paar gut definierter Redoxpeaks bei etwa 2,25 und 2,65 zeigt V, entsprechend der Insertion und Extraktion von Lithiumionen in das MoO3[10]. Abb. 4(c) zeigt die ersten drei galvanostatischen Lade-/Entladekurven des TFLB bei a Stromdichte von 50 mAâg-1 (20 μAâcm-2, basierend auf der Masse des MoO3-Films). Wie beobachtet, liefert der TFLB Die anfänglichen Lade-/Entladekapazitäten betragen 145/297 mAhâg-1 (58/118,8). μAhâcm-2). Nach dem 2. Zyklus gleichmäßiges Zyklenverhalten mit hoher Reversibilität Die TFLB erreichte eine spezifische Kapazität von 282 mAhâg-1. Die Ratenleistung von Der TFLB bei verschiedenen Stromdichten ist in Abb. 4(d) dargestellt. Der Irreversibler Kapazitätsverlust des TFLB in den ersten Zyklen bei niedrigem Strom Die Dichte kann auf einen irreversiblen Phasenübergang im abgeleiteten MoO3 zurückgeführt werden durch Lithiuminsertion[26]. Stabile Entladekapazitäten von etwa 219, 173, 107 und 50 mAhâg-1 werden bei 100, 200, 400 bzw. 800 mAâg-1 beobachtet. demonstriert eine gute Ratefähigkeit. Zur Bewertung der elektrochemischen Stabilität des TFLB wurde die Zyklusleistung weiterhin bei einer Stromdichte von durchgeführt 200 mAâg-1 (Abb. 4(e)). Der TFLB kann nach 200 Zyklen 78,1 % seiner ursprünglichen Entladekapazität beibehalten. und die Coulomb-Effizienz liegt für jeden Zyklus bei nahezu 100 %, was akzeptabel ist elektrochemische Stabilität des LiSiON-Elektrolyten. EIS-Messungen waren weiter bei Leerlaufspannung durchgeführt, um das zu untersuchen Elektrolyt/Elektroden-Grenzfläche im TFLB bei verschiedenen Zyklenzahlen und die entsprechende Nyquist-Diagramme mit Ersatzschaltbild sind in Abb. 4(f) dargestellt. Als beobachtet, zeigt der MoO3/LiSiON/Li-TFLB ein ähnliches EIS-Spektrum, das besteht von zwei Halbkreisen im Hochfrequenzbereich im Frischzustand zu dem des MoO3/LiPON/Li TFLB in unserer vorherigen Arbeit[10], was darauf hinweist dass der Li/LiSiON-Grenzflächenwiderstand im Vergleich zu dem des Li/LiSiON vernachlässigbar ist LiSiON/MoO3-Schnittstelle[20]. Der erste kleine Halbkreis in den Nyquist-Diagrammen ist wird auf die Ionenleitung von Li+-Ionen im LiSiON-Elektrolyten zurückgeführt, während die Der zweite große Halbkreis entspricht dem Ladungsübertragungsprozess am LiSiON/MoO3-Schnittstelle[27,28]. Es ist anzumerken, dass der erste kleine Halbkreis selten ist Veränderungen während der Zyklen, was auf die relativ gute Zyklenstabilität von hinweist der LiSiON-Elektrolyt. Der zweite Halbkreis dehnt sich jedoch allmählich aus Die Zykluszahl entwickelt sich und zeigt die erhöhte LiSiON/MoO3-Grenzfläche Widerstand beim Radfahren, was der Hauptgrund für die Kapazität sein könnte Verblassen des TFLB[29]. Es ist erwähnenswert, dass dies erfolgreich funktioniert verwendet den LiSiON-Elektrolyten zum Aufbau von TFLB und demonstriert das Gute Grenzflächenkontakt von LiSiON sowohl mit der MoO3-Kathode als auch mit der Lithiumanode für die Zum ersten Mal. Darüber hinaus sind die große spezifische Kapazität, die gute Ratenfähigkeit und Die akzeptable Zyklusleistung des MoO3/LiSiON/Li-TFLB zeigt, dass das LiSiON Ein dünner Film eignet sich gut als Elektrolyt für TFLB.
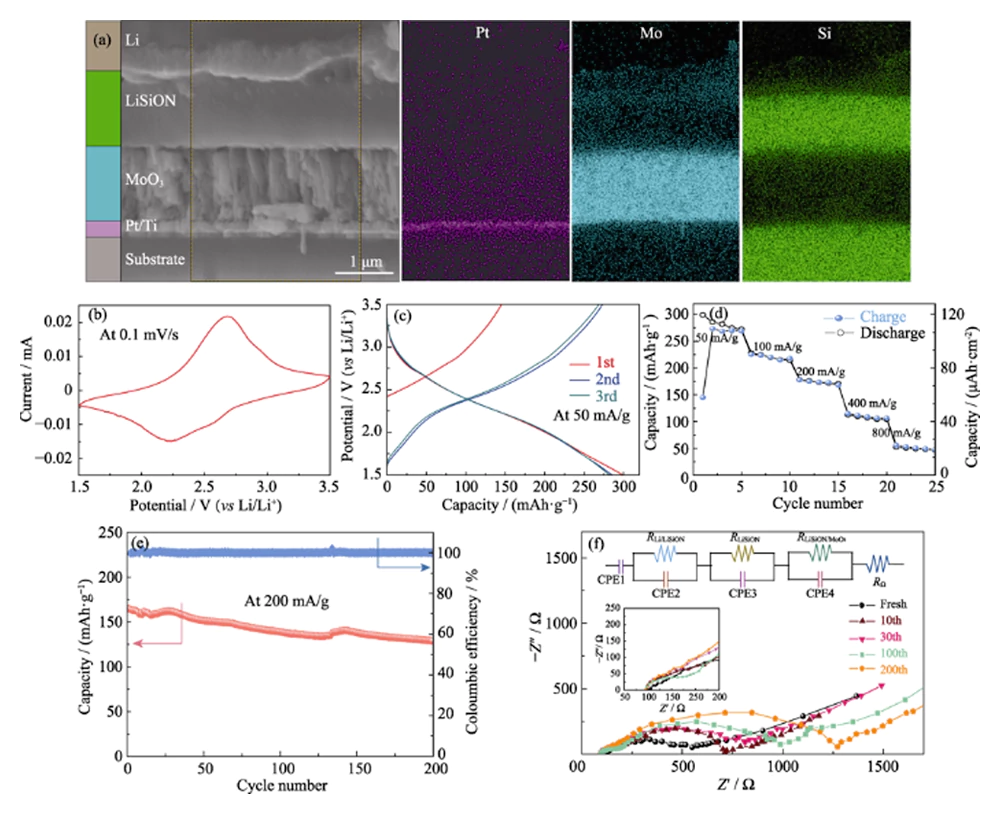
Abb. 4 (a) Querschnitts-FESEM-Bild und entsprechende EDS-Zuordnung Bilder des MoO3/LiSiON/Li TFLB; (b) Typische CV-Kurve, (c) die ersten drei Lade-/Entladekurven, (d) Rate Leistung, (e) Zyklusleistung und (f) EIS-Spektren bei verschiedenen Zyklen Zahlen des MoO3/LiSiON/Li TFLB mit Probe LiSiON-100N9A1 als Elektrolyt
3 Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass der amorphe LiSiON-Dünnschichtelektrolyt erfolgreich war hergestellt durch HF-Magnetronsputtern unter Verwendung eines Li2SiO3-Targets mit N2/Ar-Gasfluss. Der optimierte LiSiON-Dünnfilm wird unter einer HF-Leistung von 100 W beim Fluss abgeschieden 90 sccm N2 und 10 sccm Ar besitzen eine glatte Oberfläche, eine dichte Struktur und einen hohen Ionengehalt Leitfähigkeit (6,3×10-6 Sâcm-1) und ein breites Spannungsfenster (5 V), was es zu einem vielversprechenden Produkt macht Elektrolytmaterial für TFLB. Noch wichtiger ist die Verwendung von LiSiON Als Elektrolyt wurde ein MoO3/LiSiON/Li-TFLB erfolgreich demonstriert Erstmals mit hoher spezifischer Kapazität (282 mAhâg-1 bei 50 mAâg-1), guter Ratenleistung (50 mAhâg-1 bei 800 mAâg-1) und akzeptable Zyklenstabilität (78,1 % Kapazitätserhalt nach 200 Zyklen). Es wird erwartet, dass diese Arbeit neue Möglichkeiten für die Entwicklung hochentwickelter Technologien mit sich bringt. Leistung TFLB durch Verwendung eines Dünnschichtelektrolyten auf Li2O-SiO2-Basis.
Referenzen
[1] MOITZHEIM S, PUT B, VEREECKEN P M. Fortschritte bei 3D-Dünnschicht-Li-Ionen-Batterien. Advanced Materials Interfaces, 2019,6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S, et al. Tunnelverwachsung von LixMnO2-Nanoblatt-Arrays als 3D-Kathode für Hochleistungs-Festkörper-Dünnschicht-Lithium-Mikrobatterien. Fortgeschrittene Materialien, 2021,33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B, et al. Verbesserung der Lithiumionenleitfähigkeit in Festelektrolyten mit Lithium-Superionenleiter (LISICON) durch einen gemischten Polyanioneneffekt. ACS Applied Materials & Interfaces, 2017,9(8):7050-7058.
[4] BATES JB, DUDNEY N J, GRUZALSKI G R, et al. Herstellung und Charakterisierung von amorphen Lithium-Elektrolyt-Dünnfilmen und wiederaufladbaren Dünnfilmbatterien. Journal of Power Sources, 1993, 43(1/2/3):103-110.
[5] BATES J. Elektrische Eigenschaften amorpher Lithiumelektrolyt-Dünnfilme. Solid State Ionics, 1992, 53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O, et al. Zusammensetzungsabhängigkeit der Ionenleitfähigkeit in LiSiPO(N)-Dünnschichtelektrolyten für Festkörperbatterien. ACS Applied Energy Materials, 2019,2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD JN, et al. Strukturelle und mechanistische Einblicke in die schnelle Lithiumionenleitung in Li4SiO4-Li3PO4-Festelektrolyten. Journal of the American Chemical Society, 2015,137(28):9136-9145.
[8] CHEN R, SONG X. Die Ionenleitfähigkeit fester Elektrolyte für Li4+xMxSi1-xO4-yLi2O (M=Al, B)-Systeme. Journal of the Chinese Chemical Society, 2002, 49:7-10.
[9] ADNAN S, MOHAMED N S. Auswirkungen der Sn-Substitution auf die Eigenschaften des Li4SiO4-Keramikelektrolyten. Solid State Ionics, 2014,262:559-562.
[10] SUN S, XIA Q, LIU J, et al. Eigenständige sauerstoffarme α-MoO3-x-Nanoflocken-Arrays als 3D-Kathode für fortschrittliche All-Solid-State-Dünnschicht-Lithiumbatterien. Journal of Materiomics, 2019,5(2):229-236.
[11] DING W, LU W, DENG X, et al. Eine XPS-Studie zur Struktur eines SiNx-Films, der durch Mikrowellen-ECR-Magnetronsputtern abgeschieden wurde. Acta Physica Sinica, 2009,58(6):4109-4116.
[12] KIM H, KIM Y. Partielle Nitridierung von Li4SiO4 und ionische Leitfähigkeit von Li4. 1SiO3. 9N0. 1Ceramics International, 2018,44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O, et al. Analyse von SiO-Anoden für Lithium-Ionen-Batterien. Journal of The Electrochemical Society, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S, et al. Reaktion und Raumladungsschichtbildung an der LiCoO2-LiPON-Grenzfläche: Einblicke in die Defektbildung und die Ausrichtung des Ionenenergieniveaus durch einen kombinierten Ansatz aus Oberflächenwissenschaft und Simulation. Chemiematerialien, 2017,29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S, et al. Reduzierung des Ladungsübertragungswiderstands an der Grenzfläche zwischen Festelektrolyt und Elektrode durch gepulste Laserabscheidung von Filmen aus einer kristallinen Li2PO2N-Quelle. Journal of Power Sources, 2016,312:116-122.
[16] SICOLO S, FINGERLE M, HAUSBRAND R, et al. Grenzflächeninstabilität von amorphem LiPON gegenüber Lithium: eine kombinierte Dichtefunktionaltheorie und spektroskopische Studie. Journal of Power Sources, 2017,354:124-133.
[17] WU F, LIU Y, CHEN R, et al. Herstellung und Leistung eines neuartigen Li-Ti-Si-P-O-N-Dünnschichtelektrolyten für Dünnschicht-Lithiumbatterien. Journal of Power Sources, 2009,189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J, et al. Elektrische Charakterisierung ultradünner RF-gesputterter LiPON-Schichten für nanoskalige Batterien. ACS Applied Materials & Interfaces, 2016,8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Li+-Leitung in Li-Nb-O-Filmen, abgeschieden durch ein Sol-Gel-Verfahren. Solid State Ionics, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. Hochleistungsfähige flexible Festkörper-Mikrobatterien auf Basis des Festelektrolyten Lithium-Boroxynitrid. Journal of Power Sources, 2016,328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Festkörperbatterie mit Li2O-V2O5-SiO2-Festelektrolyt-Dünnfilm. Solid State Ionics, 1990, 40-41:964-966.
[22] Kalita D, Lee S, Lee K, et al. Ionenleitfähigkeitseigenschaften des amorphen Li-La-Zr-O-Festelektrolyten für Dünnschichtbatterien. Solid State Ionics, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A, et al. Herstellung amorpher Li4SiO4-Li3PO4-Dünnfilme durch gepulste Laserabscheidung für Festkörper-Lithium-Sekundärbatterien. Solid State Ionics, 2011,182:59-63.
[24] TANG, WU F, LI L, et al. Magnetron-Sputtering-Vorbereitung von stickstoffhaltigen Dünnschichtelektrolyten auf Lithium-Aluminium-Titanphosphat-Basis für Festkörper-Lithium-Ionen-Batterien. The Journal of Physical Chemistry C, 2012,116(5):3817-3826.
[25] YU X, BATES JB, JELLISON G, et al. Ein stabiler Dünnschicht-Lithiumelektrolyt: Lithiumphosphoroxynitrid. Journal of The Electrochemical Society, 1997,144(2):524.
[26] KIM H, COOK J, LIN H, et al. Sauerstofffehlstellen verbessern die pseudokapazitiven Ladungsspeichereigenschaften von MoO3-x. Naturmaterialien, 2017,16:454-460.
[27] SONG H, WANG S, SONG X, et al. Solarbetriebene Festkörper-Lithium-Luft-Batterien, die bei extrem niedrigen Temperaturen betrieben werden. Energie- und Umweltwissenschaften, 2020,13(4):1205-1211.
[28] WANG Z, LEE J, XIN H, et al. Auswirkungen der Kathoden-Elektrolyt-Grenzflächenschicht (CEI) auf die Langzeitzyklen von Festkörper-Dünnschichtbatterien. Journal of Power Sources, 2016,324:342-348.
[29] QIAO Y, DENG H, HE P, et al. Eine 500 Wh/kg Lithium-Metall-Zelle basierend auf anionischem Redox. Joule, 2020,4(6):1311-1323.



