Kategorien
neuer Blog
- Leitfaden zur Auswahl von Batterieelektrolyten: Was Einkaufsmanager wissen müssen
- Ausrüstung für Knopfzellenlabore: Die vollständige Checkliste für Batterie-Forschungs- und Entwicklungslabore
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
Tags
F-dotierte, kohlenstoffbeschichtete Nano-Si-Anode mit hoher Kapazität
F-dotierter Kohlenstoff beschichtet Nano-Si-Anode mit hoher Kapazität: Herstellung durch gasförmige Fluorierung und Leistung für Lithiumspeicher
Autor: SU Nan, QIU Jieshan, WANG Zhiyu. F-dotiert Kohlenstoffbeschichtete Nano-Si-Anode mit hoher Kapazität: Herstellung durch gasförmige Fluorierung und Leistung für die Lithiumspeicherung. Journal of Inorganic Materials, 2023, 38(8): 947-953 DOI:10.15541/jim20230009
Zusammenfassung
Si-Anoden bergen ein enormes Potenzial für die Entwicklung hochenergetischer Li-Ionen Batterien. Ein schnelles Versagen aufgrund großer Volumenänderungen bei der Li-Aufnahme behindert dies jedoch ihre Anwendung. Diese Arbeit berichtet über eine einfache, aber wenig toxische Gasfluorierung Weg zur Herstellung von F-dotierten kohlenstoffbeschichteten Nano-Si-Anodenmaterialien. Beschichtung von Nano-Si mit F-dotiertem Kohlenstoff mit hohen Defekten kann Si wirksam schützen von enormen Volumenänderungen bei der Li-Speicherung bei gleichzeitiger Erleichterung des Li+-Transports und Bildung einer stabilen LiF-reichen Festelektrolyt-Interphase (SEI). Diese Anode zeigt hohe Kapazitäten von 1540-580 mAh·g-1 bei verschiedenen aktuelle Raten von 0,2-5,0 A·g-1, unter Beibehaltung 75 % Kapazität nach 200 Zyklen. Diese Methode befasst sich auch mit den Problemen von hohe Kosten und Toxizität traditioneller Fluorierungstechniken, die Fluor verwenden Quellen wie XeF2 und F2.
Schlüsselwörterï¼ Li-Ionen-Akku; Si-Anode; F-dotierter Kohlenstoff; gasförmige Fluorierung Methode
Entwicklung effizienter Energiespeicher und Umwandlungstechnologien werden dazu beitragen, das Ziel des „Carbon Peaking“ zu erreichen CO2-Neutralitätâ. Lithium-Ionen-Batterien sind derzeit eine der am weitesten verbreiteten verwendeten hocheffiziente Energiespeichertechnologien [1]. Allerdings kommerziell Graphitanoden haben eine geringe Lithiumspeicherkapazität, was die Lithiumspeicherkapazität stark einschränkt Energiedichte von Lithium-Ionen-Batterien [2]. Silizium hat die Vorteile von niedrig potenzielle und reichlich vorhandene Reserven und ihre theoretische spezifische Kapazität (4200 mAh·g-1) ist viel höher als die der Graphitanode und wird daher als a angesehen mögliches Anodenmaterial als Ersatz für Graphit [3]. Siliziummaterialien erreichen Lithiumspeicherung basierend auf der reversiblen Legierungsreaktion mit Lithiumionen, Dieser Prozess geht jedoch mit enormen Volumenänderungen (~400 %) einher, was dazu führt schnelles Pulverisieren und Versagen der Elektrode, was zu einem wesentlichen Engpass wird Einschränkung der praktischen Anwendung von Siliziumanoden [3-4].
In den letzten Jahren haben Forscher entwickelte verschiedene Strategien zur Verbesserung der Stabilität und der Elektrochemie Leistung von Siliziumanoden. Wie zum Beispiel: Nanometerisierung [5], strukturell Verbundwerkstoff mit leitfähigem Kohlenstoff und anderen Materialien [6-7] usw. Verbessern Sie die Strukturstabilität der Siliziumanode durch Linderung der mechanischen Belastung mit der Volumenausdehnung der Lithiumspeicherung im mikroskopischen Bereich verbunden Skala. Entwickeln Sie neue Elektrolyte oder Elektrolytzusätze, um die zu verbessern Stabilität und Coulomb-Effizienz der Festelektrolyt-Grenzflächenphase (SEI) auf der Oberfläche der Siliziumanode [8]. Entwickeln Sie effiziente Polymere Bindemittel (wie Natriumcarboxymethylcellulose, Natriumalginat, Polyacryl). säurebasiertes Polyrotaxan [9] usw.). Stärken Sie die Bindungskraft zwischen den Wirkstoffen Materialien, zwischen aktiven Materialien und leitfähigem Netzwerk und dazwischen Elektrodenfilm und Stromkollektor [9-10]. Eine davon ist die Kohlenstoffbeschichtung eines der wirksamsten Mittel zur Verbesserung der strukturellen Stabilität von Siliziumanoden und modulieren Oberflächen- und Grenzflächeneigenschaften [3-4,11]. Allerdings ist das eng Die beschichtete, hochstabile Kohlenstoffschicht behindert zudem den Lithium-Ionen-Transport und begrenzt ihn die volle Leistung der Siliziumanode.
Außerdem die wiederholte Lautstärke Veränderungen der Siliziumanode während des kontinuierlichen Lade- und Entladevorgangs führen auch dazu, dass der SEI-Film kontinuierlich bricht und immer wieder wächst, was dazu führt der kontinuierliche Verlust von aktivem Lithium und Elektrolyt auf der Elektrodenoberfläche [12]. Als Reaktion auf die oben genannten Probleme schlägt diese Studie eine effiziente Lösung vor Gasphasenfluorierungsverfahren zur Beschichtung der Oberfläche des Siliziumanodenmaterials mit einer stark defekten amorphen Kohlenstoffschicht, die reich an Fluorelementen ist seine Struktur und Grenzflächenstabilität verbessern. Im Vergleich zu traditionell Fluorierungstechnologie, die kostenintensive und hochgiftige Fluorquellen nutzt wie XeF2 oder F2 [13] ist diese Strategie einfacher und weniger toxisch. Der Eine mit Fluor dotierte Kohlenstoffschicht, die die Oberfläche von Nano-Silizium-Materialien bedeckt, kann Puffern Sie effektiv die Volumenausdehnung von Lithium-eingebetteten Siliziumanoden bei gleichzeitiger Verbesserung der Lithium-Ionen-Transportfähigkeiten. Und ein äußerst stabiler SEI Ein Film, der reich an anorganischem Fluorid ist, wird vor Ort aufgebaut, um das Ziel zu erreichen Verbesserung der Zyklenstabilität der Siliziumanode.
1 Experimentelle Methode
1.1 Materialvorbereitung
Vorbereitung der Kohlenstoffbeschichtung Nanosilizium (Si@C): 0,3 g kommerzielles Nanosilizium Pulver (Partikelgröße 20–100 nm, Aladdins Reagenz) wurde mit Ultraschall behandelt dispergiert in 28 ml einer Lösungsmittelmischung aus entionisiertem Wasser und Ethanol (Vol Verhältnis 5:2). Nach Zugabe von 0,4 ml 3-Aminopropyltriethoxysilan 2 Stunden rühren um eine gleichmäßige Dispersion zu bilden. A. 0,115 g 4,4-Dihydroxydiphenyl auflösen Sulfid und 0,1 g 3-Aminophenol in 28 ml eines entionisierten Lösungsmittelgemischs Wasser und Ethanol (Volumenverhältnis 5:2), um eine homogene Lösung B zu bilden. Mischen Dispersion A und Lösung B gleichmäßig verteilen, 0,1 mL Ammoniakwasser zugeben, 30 Min. rühren, Geben Sie dann 0,14 ml Formaldehydlösung (37 % bis 40 %) hinzu und reagieren Sie mit konstanter Temperatur 12 h bei 30 °C rühren. Nach der Reaktion erfolgt die Phenolharzbeschichtung Nanosilica (Si@AF) wurde durch Zentrifugieren und Waschen mit Ethanol erhalten dreimal abwechselnd entionisiertes Wasser. Es wurde in Argongas bei 800 °C kalziniert für 3 Stunden, um kohlenstoffbeschichtetes Nanosilizium (Si@C) zu erhalten.
Herstellung von mit Fluor dotiertem Kohlenstoffbeschichtetes Nano-Silizium (Si@C-F): 100 mg Si@C und 200 mg Polyvinylidenfluorid (PVDF) wurden in einen Argon-geschützten Rohrofen gegeben. Das PVDF enthaltende Quarzschiffchen befindet sich stromaufwärts des Luftstroms Ein Si@C-haltiges Quarzschiffchen befindet sich stromabwärts des Luftstroms. Es ist geröstet bei 600 °C für 3 Stunden, um mit Fluor dotiertes, kohlenstoffbeschichtetes Nanosilizium (Si@C-F) zu erhalten.
1.2 Batteriemontage und elektrochemische Leistungsprüfung
1.2.1 Batteriebaugruppe
Bauen Sie die CR2016-Knopfbatterie zusammen zum Testen. Mischen Sie das aktive Material, den leitfähigen Ruß und Carboxymethylcellulose-Natrium-Bindemittel gleichmäßig im Massenverhältnis 7:2:1. Deionisiert Wasser wurde als Lösungsmittel und Dispergiermittel zugegeben und die erhaltene Aufschlämmung wurde hergestellt gleichmäßig auf die Kupferfolie als Arbeitselektrode aufgetragen. Das aktive Material Die Beladung betrug 0,8–1,0 mg·cm-2. Als Theke wurden Lithiumbleche verwendet Elektroden und Referenzelektroden. Der Elektrolyt ist eine DOL/DME-Lösung gelöst in 1,0 mol/L LiTFSI (Lithiumbistrifluormethansulfonatimid) und 2,0 % LiNO3(DOL ist 1,3-Dioxolan, DME ist Ethylenglykoldimethylether, Volumen Verhältnis 1:1). Bauen Sie die Zelle in einer mit Argon gefüllten Handschuhbox zusammen (Wassergehalt < 0,1 μL/L, Sauerstoffgehalt < 0,1 μL/L).
1.2.2 Batterieleistungstest
Verwenden Sie das elektrochemische IVIUM Vertex.C.EIS Arbeitsplatz zur Analyse des Reaktionsmechanismus und der Reaktionskinetik des Batterie mithilfe der Cyclic Voltammetry (CV)-Methode. Der Spannungsbereich liegt zwischen 0,01 und 1,5 V, und die Sweep-Rate beträgt 0,05~0,5 mV·s- 1. Elektrochemische Impedanz Zur Analyse der Elektrodendynamik wurde Spektroskopie (EIS) eingesetzt. Die Testfrequenz Der Bereich betrug 100 kHz bis 10 MHz und die Amplitude der Störspannung betrug 5,0 mV. Mit dem Batterietester Land CT2001A wurde die Lithiumspeicherleistung untersucht unter Verwendung der Konstantstrom-Lade- und Entlademethode. Das Spannungsfenster war 0,01–1,5 V (gegenüber Li/Li+) und die Stromdichte betrug 0,2–5,0 A·g-1.
2 Ergebnisse und Diskussion
2.1 Analyse von Aussehen, Struktur und Zusammensetzung von Materialien
Der Vorbereitungsprozess von fluordotierte, kohlenstoffbeschichtete Nano-Silizium-Materialien sind in Abbildung 1 dargestellt. Zunächst werden polymerbeschichtete Silizium-Nanopartikel (Si@AF) auf Basis hergestellt Phenol-Aldehyd-Kondensationspolymerisationsreaktion und umgewandelt in amorphe kohlenstoffbeschichtete Nano-Silizium-Nanopartikel (Si@C) bei hoher Temperatur. Dann Als Fluorquelle wird Polyvinylidenfluorid verwendet und mit Fluor dotiert über die Gasphase in die Kohlenstoffschicht außerhalb der Silizium-Nanopartikel Fluorierungsmethode bei hoher Temperatur. Abbildung 2(a) zeigt die XRD-Muster von Si@C- und Si@C-F-Materialien. Beugungspeaks liegen bei 2θ=28°, 47°, 56°, 69° und 76°. Sie entsprechen den Kristallen (111), (220), (311), (400) und (331). Ebenen aus einkristallinem Silizium (JCPDS 77-2108). Der breite Gipfel liegt bei 2θ=25°~26° wird auf die gebildete kurzreichweitig geordnete Kohlenstoffstruktur zurückgeführt durch die Carbonisierung des phenolischen Kondensationspolymerisationsprodukts. Der Kohlenstoffbeschichtungsschicht mit hoher Leitfähigkeit und ausgezeichneter struktureller Flexibilität kann den Pulverisierungsfehler von Siliziummaterialien während des Prozesses wirksam lindern den Lade- und Entladevorgang und verbessern die Leitfähigkeit der Elektrode. Abbildung 2(b) ist das Raman-Spektrum von Si@C- und Si@C-F-Materialien, mit offensichtlichem Absorptionspeaks erscheinen bei 515, 947, 1350 und 1594 cm-1. Unter ihnen sind die Absorptionspeaks bei 515 und 947 cm-1 sind die charakteristischen Peaks von kristallines Silizium, das vom Photophonon erster Ordnung abgeleitet ist Streuung und die transversale Photophononstreuung zweiter Ordnung von Silizium bzw. [14]. Die Absorptionspeaks bei 1350 und 1594 cm-1 entsprechen dem aromatische Kohlenstoffkonfigurations-Streckschwingung (G-Modus) und die Unordnung defekte Kohlenstoffstruktur (D-Modus). Im Allgemeinen ist die Das Intensitätsverhältnis von D-Modus und G-Modus (ID/IG) kann zur Messung des Grades verwendet werden von Defekten und Unordnung von Kohlenstoffmaterialien [15]. Im Vergleich zu Si@C-Material (ID/IG=0,99) erhöht sich das ID/IG von Si@C-F-Material auf 1,08. Es zeigt, dass die Der Fluorierungsprozess kann die Defekte der Kohlenstoffbeschichtungsschicht verstärken. Dies ist vorteilhaft für eine dichte Beschichtung von Nano-Silizium und verbessert gleichzeitig die Lithiumionen Transportmöglichkeiten.
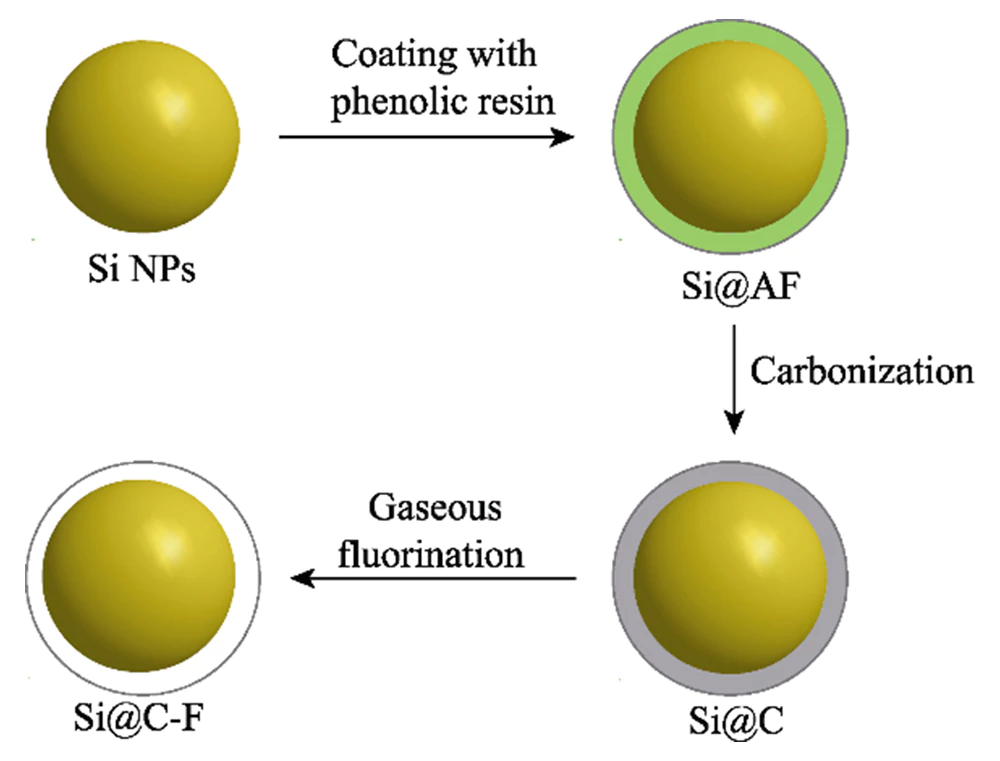
Abb. 1 Schematische Darstellung der Herstellung von Si@C-F
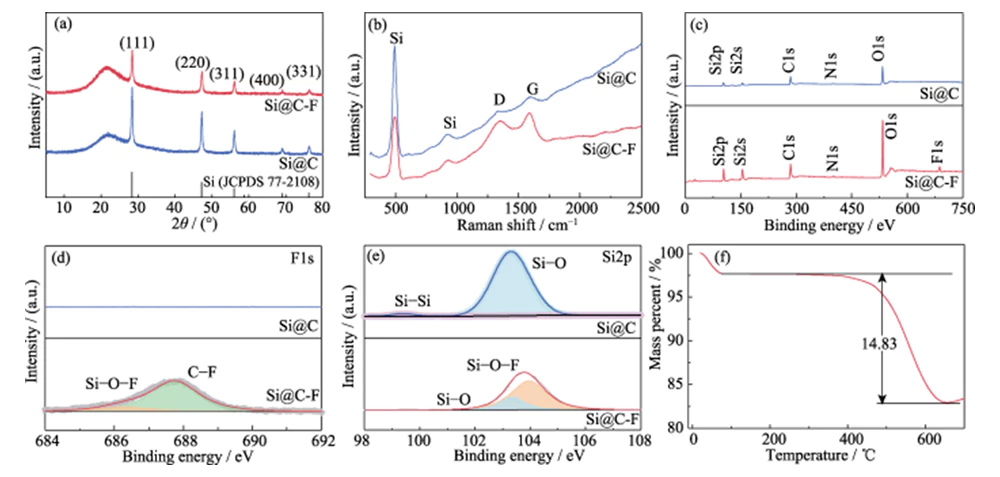
Abb. 2 (a) XRD-Muster, (b) Raman-Spektren, (c) XPS Übersichtsscan, (d) hochauflösende F1s- und (e) Si2p-XPS-Spektren von Si@C und Si@C-F, (f) TGA-Kurve von Si@C-F
Das XPS-Vollspektrum zeigt, dass die Si@C-Material enthält die Elemente O, N, C und Si (Abbildung 2(c)). Das Atom Anteil des F-Elements im Si@C-F-Material, das nach der Fluorierung erhalten wird Die Behandlung beträgt etwa 1,8 %. Im hochauflösenden F1s XPS-Spektrum (Abbildung 2(d)), die beiden charakteristischen Peaks bei der Bindungsenergie von 686,3 und 687,8 eV entsprechen C-F bzw. Si-O-F, wobei C-F dominiert eins. Es zeigt, dass die Fluorierungsbehandlung erfolgreich Fluor eingeführt hat Element in die amorphe Kohlenstoffschicht, die auf der Oberfläche von Nanosilizium aufgetragen ist. Der Hochaufgelöste Si2p- (Abbildung 2(e)) und F1s-XPS-Spektren beweisen, dass Si-Atome interagieren chemisch mit dem F-Element in der Kohlenstoffschicht, indem sie Si-O-F bilden Bindungen, was für die dichte Beschichtung der Kohlenstoffschicht auf der Oberfläche von Vorteil ist Silikonoberfläche. Die thermogravimetrische Analyse (TGA) zeigt, dass der Massenanteil Der Anteil an Si im Si@C-F-Material beträgt etwa 85,17 % (Abbildung 2(f)).
Die SEM-Analyse zeigt, dass das Si@C-F Das Material besteht aus Nanopartikeln mit einer Größe von <100 nm (Abbildung 3(a~c)). Nach der Hochtemperaturkarbonisierung und der Gasphasenfluorierungsbehandlung ist das Kohlenstoffmaterial immer noch gleichmäßig auf der Oberfläche der Silizium-Nanopartikel beschichtet.
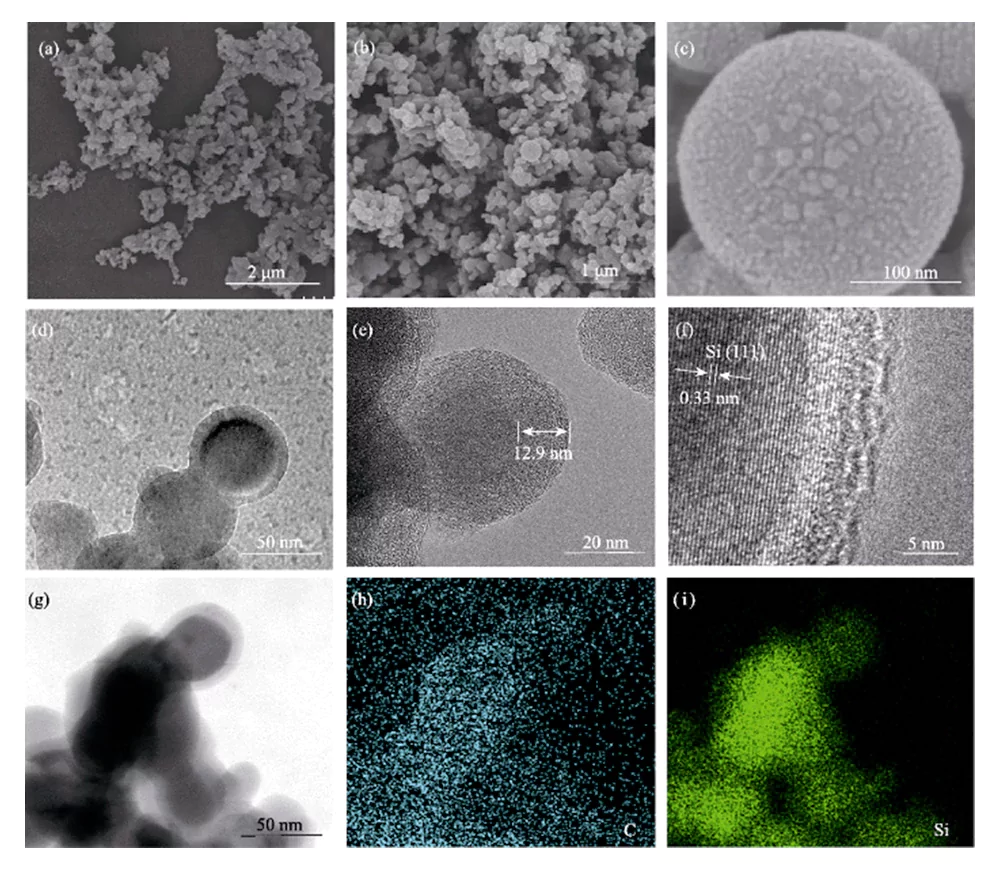
Abb. 3 (a-c) SEM-Bilder, (d-f) TEM-Bilder und (g-i) Elementkartierung von Si@C-F
TEM-Analyse zeigt, dass das Silizium Nanopartikel werden vollständig und gleichmäßig von einer Kohlenstoffschicht umhüllt Dicke von etwa zehn Nanometern, die eine Kern-Schale-Struktur bilden (Abbildung 3(d~e)). Silizium-Nanopartikel haben eine Einkristallstruktur, in der die Ein Gitterabstand von 0,328 nm entspricht der (111)-Kristallebene von Si und Die ihn bedeckende, mit Fluor dotierte Kohlenstoffschicht weist eine amorphe Struktur auf (Abbildung 3(f)). Das Elementverteilungsspektrum beweist, dass C- und Si-Elemente vorhanden sind gleichmäßig verteilt in Si@C-F (Abbildung 3(g~i)).
2.2 Elektrochemische Eigenschaften von Materialien
Abbildung 4(a, b) ist die CV-Kurve von Si@C- und Si@C-F-Anodenmaterialien. Die Wobbelgeschwindigkeit beträgt 0,1 mV·s-1 und der Spannungsbereich beträgt 0,01–1,5 V. Im ersten Zyklus entspricht der schwache breite Peak im Bereich von 0,1 bis 0,4 V dem irreversibler Prozess der Elektrolytzersetzung unter Bildung eines SEI-Films; Die Der Reduktionspeak bei 0,01 V entspricht dem Prozess von kristallinem Silizium Bildung einer Silizium-Lithium-Legierung (LixSi) durch Legierungsreaktion. Während der anschließenden Dem Ladevorgang entsprechen die beiden Oxidationsspitzen bei 0,32 und 0,49 V Prozess der Entlegierung von LixSi zur Bildung von amorphem Silizium [16]. Fluorierung Durch die Behandlung können strukturelle Dotierungs- und Ätzeffekte erzielt werden. Eine große Anzahl von Strukturdefekte werden in die darauf aufgetragene amorphe Kohlenstoffschicht eingebracht Oberfläche des Si-Materials, um einen dreidimensionalen Lithiumionentransport zu bilden Kanal, beschleunigen den Lithiumionentransport und verbessern die Elektrochemie Reaktivität des Si-Materials. Daher weist Si@C-F eine schärfere Wirkung auf Delithiierungs-Oxidationspeak bei 0,49 V als die Si@C-Anode ohne Fluor Doping. Beim anschließenden Entladevorgang liegt der neue Reduktionspeak bei 0,19 V entspricht dem Lithium-Insertionsprozess des gebildeten amorphen Siliziums beim ersten Ladevorgang [16-17]. Mit zunehmender Zyklenzahl die Positionen des Oxidationspeaks und des Reduktionspeaks in der CV-Kurve Nr längere Änderung, was darauf hindeutet, dass Si@C- und Si@C-F-Anodenmaterialien einem ähnlichen Verhalten folgen Legierungs-Lithium-Speichermechanismus nach dem ersten Laden und Entladen. Während Bei diesem Prozess nahmen der Oxidationspeak und der Reduktionspeak allmählich zu. Dies spiegelt einen typischen Elektrodenaktivierungsprozess wider.
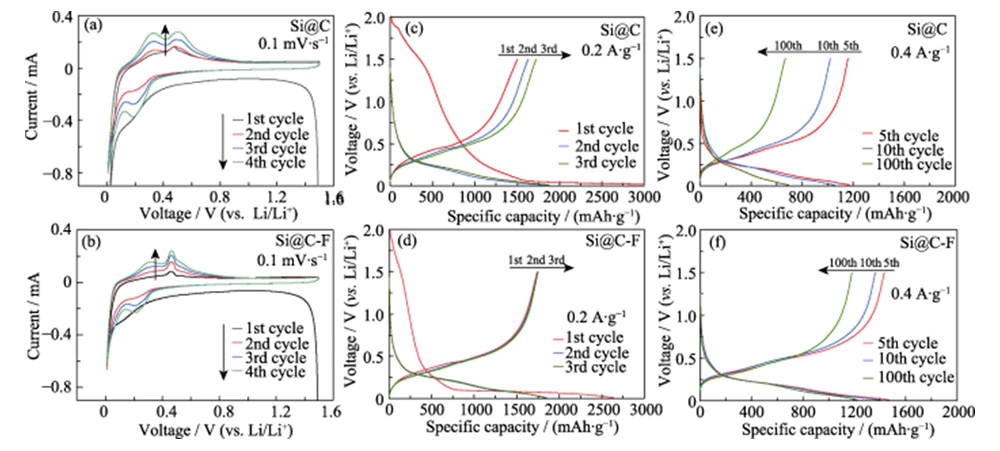
Abb. 4 (a, b) CV-Kurven bei einer Abtastrate von 0,1 mV·s-1 und Lade-Entlade-Spannungskurven bei (c, d) 0,2 und (e, f) 0,4 A·g-1 für (a, c, e) Si@C- und (b, d, f) Si@C-F-Anoden
In der Konstantstromladung und Beim Entladungstest wurde das Si-Anodenmaterial viermal hintereinander zyklisch und aktiviert niedrigere Stromdichte (0,2 A·g-1) und dann wurde seine Zyklenstabilität bei a getestet Stromdichte von 0,4 A·g-1. Abbildung 4 (c, d) zeigt die galvanostatische Ladung und Entladungskurven von Si@C- und Si@C-F-Anoden bei 0,2 A·g-1 und die Spannung Fenster beträgt 0,01~1,5 V. Während des ersten Entladevorgangs bildeten beide eine lange Plattform im Spannungsbereich < 0,1 V, entsprechend dem Lithium-Insertionsprozess der kristallinen Siliziumlegierung. Dieser Prozess geht häufig mit einer niedrigen ersten Coulomb-Effizienz einher. Während des ersten Ladevorgangs wird die Silizium-Lithium-Legierung delithiiert und in amorphes Silizium mit einer geringeren Aktivierungsenergie für die Lithium-Insertion umgewandelt [18], wodurch das Lithium-Insertionspotential nach dem ersten Laden und Entladen auf 0,1–0,3 V ansteigt. Im Vergleich zu Si@C ist die spezifische Kapazität der ersten Entladung (2640 mAh·g-1) der Si@C-F-Anode etwas niedriger. Allerdings ist die spezifische Kapazität der ersten Ladung (1739,6 mAh·g-1) höher und der erste Coulomb-Wirkungsgrad (65,9 %) ist etwa 45,8 % höher als der der Si@C-Anode. Die Lade-Entlade-Kurve des SEI-Bereichs der negativen Si@C-F-Elektrode ist kürzer als die von Si@C, was darauf hindeutet, dass sich auf der Oberfläche ein stabilerer SEI-Film bildet. Dies liegt daran, dass die mit Fluor dotierte Kohlenstoffschicht die Bildung eines SEI-Films mit anorganischen Komponenten (wie LiF) und eine höhere Stabilität auf der Oberfläche der Siliziumanode begünstigt, wodurch irreversibler Lithiumverlust und Elektrolytverbrauch reduziert werden [19].
Abbildung 4(e~f) zeigt die Lade- und Entladekurven von Si@C und Negative Si@C-F-Elektroden bei einer Stromdichte von 0,4 A·g-1 nach der Aktivierung. Nach 100 Zyklen kann die Si@C-F-Anode immer noch eine hohe spezifische Kapazität aufrechterhalten von 1223 mAh·g-1, mit einer Kapazitätserhaltungsrate von 85 % (Abbildung 5(a)). Unter die gleichen Bedingungen, die Kapazität der negativen Si@C-Elektrode ohne Die Fluorierungsbehandlung zerfiel während des Lade- und Entladevorgangs schnell. und die Kapazitätserhaltungsrate nach 100 Zyklen betrug nur 62 %. Das zeigt es Die mit Fluor dotierte Kohlenstoffbeschichtung hat einen erheblichen Einfluss auf die Verbesserung die Zyklenfestigkeit der Siliziumanode. Kommerziell Nano-Silizium-Anoden ohne Kohlenstoffbeschichtung versagen nach mehr als 10 Zyklen aufgrund der enormen Volumenausdehnung und strukturellen Pulverisierung während der Deinterkalation von Lithium. Während dieses Prozesses wird die spezifische Kapazität von Die Anzahl der negativen Si@C-F- und Si@C-Elektroden nimmt in den ersten 10 bis 20 Jahren allmählich zu Zyklen aufgrund des Aktivierungseffekts. Bei einer großen Stromdichte von 0,2 bis 5,0 A·g-1, die Si@C-F-Anode kann eine hohe spezifische Kapazität von 1540~580 aufrechterhalten mAh·g-1, was eine hervorragende Kapazitätserhaltung zeigt (Abbildung 5(b)). Bei hohem Strom Bei einer Dichte von 5,0 A·g-1 ist die Kapazitätserhaltungsrate etwa 78 % höher als das von Si@C. Wenn die Stromdichte weiter auf 0,2 A·g-1 reduziert wird, Die spezifische Kapazität kann auf 1450 mAh·g-1 wiederhergestellt werden, was darauf hinweist, dass dies der Fall ist Die Struktur ist bei der Hochgeschwindigkeitsspeicherung von Lithium äußerst stabil. Nach 200 Lade-Entlade-Zyklen bei einer Stromdichte von 0,2 A·g-1 kann die Si@C-F-Anode durchführen eine spezifische Kapazität von 75 % aufrechterhalten. Die Kapazitätserhaltungsrate der Die Si@C-Anode ohne Fluorierungsbehandlung beträgt nur 40 % (Abbildung 5(c)). Diese Anode weist außerdem eine bessere Lithium-Speicherleistung auf als das Silizium-Anodenmaterial in der Literatur berichtet (Tabelle 1).
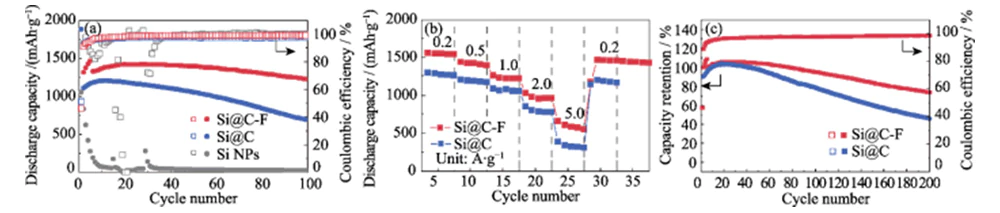
Abb. 5 (a) Zyklenstabilität bei einer Stromdichte von 0,4 A·g-1 mit von 4 aktivierten Anoden Zyklen bei 0,2 A·g-1 vor dem Zyklus und (b) Geschwindigkeitsfähigkeit bei verschiedenen Stromdichten im Bereich von 0,2 bis 5,0 A·gâ1 und (c) Kapazitätserhaltung bei einer Stromdichte von 0,2 A·g-1 für die Lithiumspeicherung in Si@C- und Si@C-F-Anoden
Tabelle 1 Vergleich der Si@C-F-Anode mit berichteten über die elektrochemische Leistung einer Anode auf Si-Basis
|
Materialien |
Ursprüngliches CE |
Anfangskapazität/(mAh·g-1) |
Kapazität rAufbewahrung |
Ref. |
|
Si@C-F |
65,9 % |
2640 |
85 % (100 Zyklen) |
Diese Arbeit |
|
Nano-Si/TiN@ |
71 % |
2716 |
59,4 % (110 Zyklen) |
[20] |
|
Si@C@RGO |
74,5 % |
1474 |
48,9 % (40 Zyklen) |
[21] |
|
Si@FA |
65 % |
1334 |
68,7 % (100 Zyklen) |
[22] |
|
p-Si@C |
58 % |
3460 |
57,5 % (100 Zyklen) |
[23] |
|
Si@void@C |
- |
900 |
70 % (100 Zyklen) |
[24] |
|
Si/C@C |
- |
1120 |
80 % (100 Zyklen) |
[25] |
Bei hohem Strom Bei einer Dichte von 5,0 A·g-1 ist die Kapazitätserhaltungsrate etwa 78 % höher als das von Si@C. Wenn die Stromdichte weiter auf 0,2 A·g-1 reduziert wird, Die spezifische Kapazität kann auf 1450 mAh·g-1 wiederhergestellt werden, was darauf hinweist, dass dies der Fall ist Die Struktur ist bei der Hochgeschwindigkeitsspeicherung von Lithium äußerst stabil. Nach 200 Lade-Entlade-Zyklen bei einer Stromdichte von 0,2 A·g-1 kann die Si@C-F-Anode durchführen eine spezifische Kapazität von 75 % aufrechterhalten. Die Kapazitätserhaltungsrate der Die Si@C-Anode ohne Fluorierungsbehandlung beträgt nur 40 % (Abbildung 5(c)). Diese Anode weist außerdem eine bessere Lithium-Speicherleistung auf als das Silizium-Anodenmaterial in der Literatur beschrieben (Tabelle 1). Die Fluordotierungsmenge in der Beschichtung Die Kohlenstoffschicht hat einen erheblichen Einfluss auf die Lithiumspeicherleistung des Si@C-F-Anode. Wenn die Fluordotierungsmenge unter 1,8 % Atomanteil liegt, Die Zyklenstabilität der Si@C-F-Anode verbessert sich erheblich Die Fluordotierungsmenge nimmt zu (Abbildung 6). Dies liegt an der verstärkten Wirkung Einfluss der Fluordotierung auf die Lithiumionentransporteigenschaften des Kohlenstoffs Beschichtungsschicht und die Stabilität des SEI-Films auf der Oberfläche des Siliziums Material. Wenn das Fluordotierungsverhältnis zu hoch ist (2,7 %), wird die kohlenstoffbeschichtet Si-Anodenmaterial behält immer noch eine gute Zyklenstabilität bei, aber die Die spezifische Kapazität sinkt erheblich. Dies ist auf den Verlust an aktivem Si zurückzuführen verursacht durch das Ätzen von Fluorspezies in der Gasphase bei hohen Temperaturen Fluorierung. Wenn die Fluordotierungsmenge 1,8 Atomprozent beträgt, ist das Si@C-F Anode weist optimale Zyklenstabilität und hohe spezifische Kapazität auf.
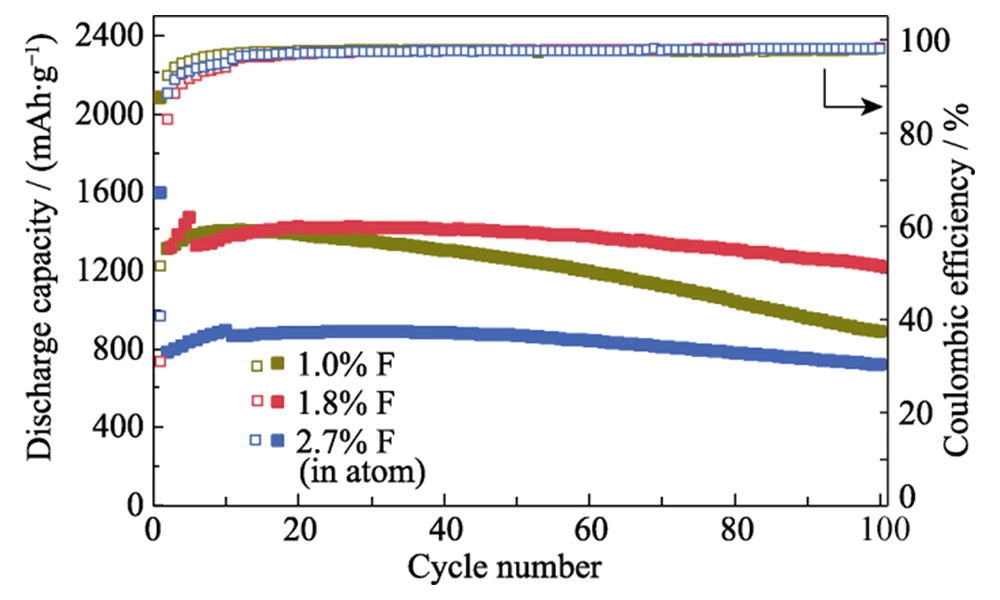
Abb. 6 Zyklenstabilität von Si@C-F-Anoden mit verschiedenen F-Verhältnisse bei einer Stromdichte von 0,4 A·g-1 mit Anoden, die vor dem Zyklus für 4–10 Zyklen bei 0,2 A·g-1 aktiviert wurden
Die EIS-Spektren von Si@C und Si@C-F Anoden bestehen aus Halbbogenkurven im Mittel- bis Hochfrequenzbereich und geneigte gerade Linien im Niederfrequenzbereich (Abbildung 7(a)). Der Halbbogen Die Kurve im Mittel- bis Hochfrequenzbereich hängt mit der Ladungsübertragung zusammen Widerstand (Rct) und die geneigte Gerade im Niederfrequenzbereich spiegelt hauptsächlich die Warburg-Impedanz (ZW) der Lithiumionendiffusion wider [26]. Vor dem Laden und Entladen wird der Rct der negativen Si@C-F- und Si@C-Elektroden gemessen sind ähnlich, erstere hat jedoch aufgrund der hohen Fehlerquote einen niedrigeren ZW Fluordotierte Kohlenstoffschicht, die die Oberfläche bedeckt. Nach dem Laden und Entladen Zyklen ist der Rct (5,51 Ω) der Si@C-F-Anode deutlich niedriger der Si@C-Anode (21,97 Ω) (Abbildung 7(b)), und der ZW ist viel niedriger als der letztere. Dies zeigt, dass der durch die fluorreiche SEI-Grenzflächenfilm induziert wird Eine mit Fluor dotierte Kohlenstoffschicht kann die Grenzflächenladung wirksam verbessern und Lithium-Ionen-Transportfähigkeiten.
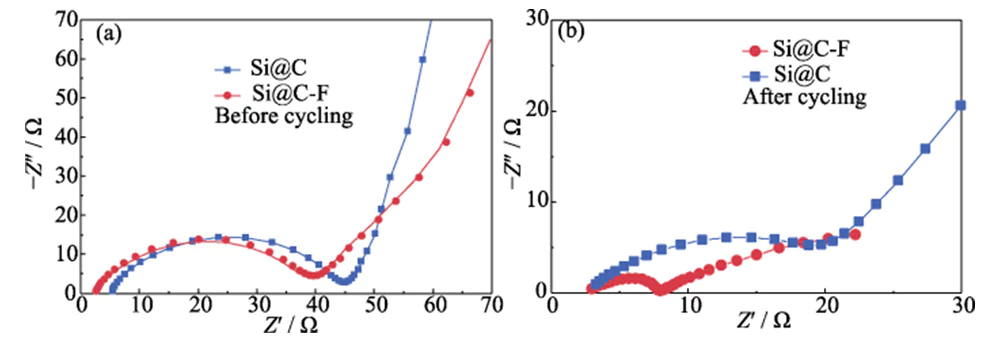
Abb. 7 Nyquist-Diagramme der Si@C- und Si@C-F-Anoden (a) vor und (b) nach dem Zyklieren bei einer Stromdichte von 0,4 A·g-1
2.3 Charakterisierung der Elektrodenstruktur nach dem Laden und Entladen
SEM-Charakterisierung nach Laden und Entladen Zyklen (Abbildung 8(a~c)) zeigt, dass dies auf die erhebliche Volumenausdehnung zurückzuführen ist Wirkung von Silizium während des Lithium-Insertionsprozesses, die Dicke des Si@C-Elektrode stieg um 132,3 %. Dies behindert nicht nur die Übertragung von Ionen und Elektronen, erhöht den Innenwiderstand und die Polarisation der Elektrode, sondern verursacht auch eine enorme mechanische Belastung, wodurch die Elektrode beschädigt wird Bruch und Trennung vom Stromkollektor, wodurch die Leistung des Si@C-Anode zerfällt schnell (Abbildung 5(c)). Im Vergleich dazu die Elektrode Die Dicke der Si@C-F-Anode erhöhte sich nach dem Laden nur um 26,6 % und Entladungszyklen und behielt eine gute strukturelle Stabilität der Elektrode bei (Abbildung 8(d~f)). Dies zeigt, dass die eingebrachte fluordotierte Kohlenstoffschicht dies kann Puffern Sie effektiv den Volumenexpansionseffekt der Lithiumeinfügung in Silizium Materialien im Mikromaßstab, wodurch die strukturelle Stabilität der erhöht wird Elektrode auf der Makroskala von unten nach oben.
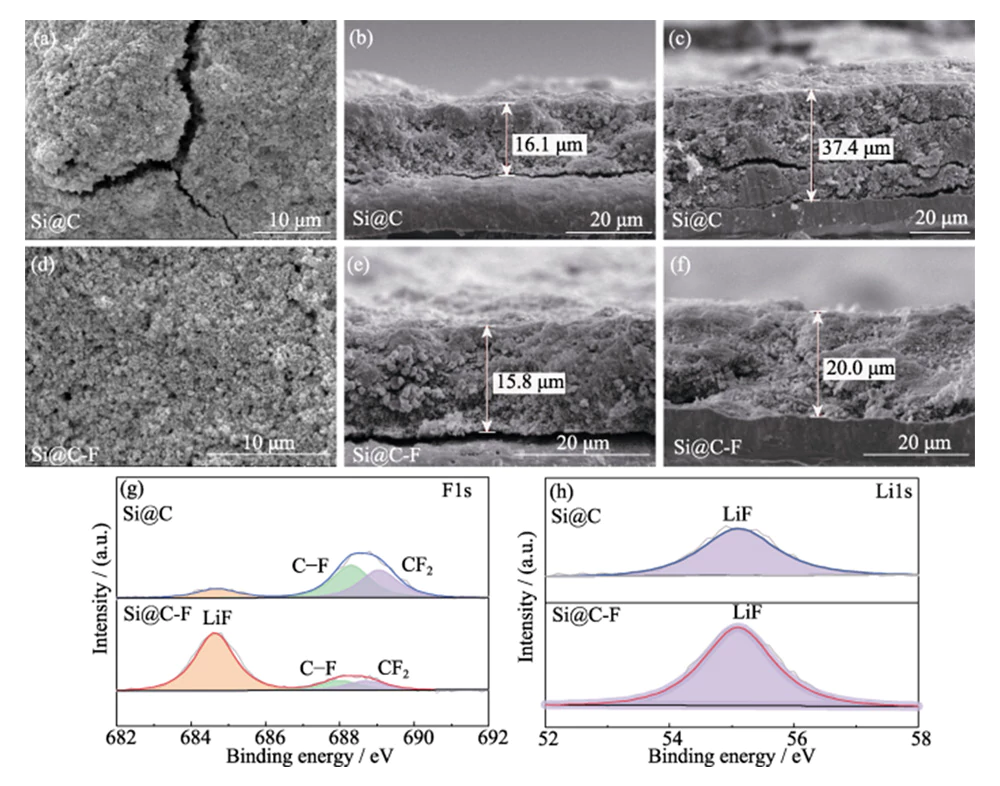
Abb. 8 Obere REM-Bilder von (a) Si@C- und (d) Si@C-F-Anoden nach dem Radfahren; Querschnitts-REM-Bilder von (b, c) Si@C- und (e, f) Si@C-F-Anoden (b, e) vor und (c, f) nach dem Radfahren; Hochauflösende (g) F1s und (h) Li1s XPS-Spektren von SEI auf Si@C- und Si@C-F-Anoden nach Zyklen
Die Zusammensetzung des SEI-Films auf der Oberfläche von Si@C und Si@C-F-Negativelektroden nach Lade- und Entladezyklen wurden analysiert durch XPS (Abbildung 8(g~h)). Im hochauflösenden F1s-XPS-Spektrum ist die Bindung erkennbar Energiespitzen bei den Bindungsenergien von 684,8, 688,3 und 689,1 eV entsprechen zu LiF, CF-Bindungen bzw. CF2. Entsprechend gibt es auch charakteristische Peaks, die LiF-Spezies in den hochauflösenden Li1s entsprechen XPS-Spektrum, das darauf hinweist, dass sich darauf ein SEI-Film gebildet hat, der LiF-Spezies enthält die Oberfläche der Siliziumanode. Verglichen mit der Si@C-Anode ist der LiF-Gehalt auf der Oberfläche der Si@C-F-Anode ist höher, was darauf hinweist, dass das LiF in der SEI-Filme entstehen nicht nur durch die Zersetzung von Lithiumsalzen Elektrolyt, sondern auch aus dem F in der fluordotierten Kohlenstoffschicht. Der Die Bildung von hochmoduligem LiF kann die strukturelle Festigkeit effektiv erhöhen des SEI-Films und hemmen die Volumenänderung der Lithiumeinfügung in Silizium Materialien. Gleichzeitig bietet LiF eine große Bandlücke und isolierende Eigenschaften kann die SEI-Dicke verringern und den anfänglichen irreversiblen Lithiumverlust verringern. Die LixSi-Legierung, das Lithiierungsprodukt von LiF und Si, weist eine hohe Grenzfläche auf Energie und kann sich besser an die plastische Verformung des lithiierten Siliziums anpassen Anode während des Zyklierens, wodurch die Zyklenstabilität des weiter verbessert wird Elektrode [19].
3 Fazit
In dieser Studie mit Fluor dotiert Kohlenstoffbeschichtete Nano-Silizium-Materialien wurden durch ein einfaches und hergestellt Gasphasenfluorierungsverfahren mit geringer Toxizität. Untersuchungen zeigen, dass Fluordotierung (1,8 % F) erhöht einerseits die Defekte der Kohlenstoffbeschichtungsschicht die Siliziumoberfläche und bietet dabei reichlich Lithium-Ionen-Transportkanäle Nano-Silizium dicht umhüllen, um dessen Volumenausdehnung zu unterdrücken. Auf der anderen Seite Andererseits wird ein hochstabiler SEI-Film, der reich an LiF ist, auf der Oberfläche induziert Nano-Silizium-Material, das die Stabilität und Coulomb-Effizienz weiter verbessert der Siliziumanode. Dadurch ist die erste Coulomb-Effizienz des Die mit Fluor dotierte, kohlenstoffbeschichtete Nano-Silizium-Anode verbesserte sich auf 65,9 %. Bei einer Strömung Mit einer Dichte von 0,2~5,0 A·g-1 weist es eine hohe spezifische Kapazität von 1540~580 auf mAh·g-1 und kann nach 200 Zyklen 75 % der ursprünglichen Kapazität beibehalten. Diese Arbeit liefert neue Ideen für die Gestaltung und Konstruktion von Siliziumanoden Materialien mit hoher Kapazität und hoher Stabilität.
Referenz
[1] NIU S S, WANG Z Y, YU ML, et al. MXen-basiert Elektrode mit verbesserter Pseudokapazität und volumetrischer Kapazität für Leistungs- Typ und extrem langlebige Lithiumspeicherung.ACS Nano, 2018, 12(4): 3928.
[2] SU X, WU Q L, LI J C, et al.Siliziumbasierte Nanomaterialien für Lithium-Ionen-Batterien: eine Rezension.Advanced Energy Materials, 2014, 4(1): 1300882.
[3] GE M Z, CAO C Y, GILL M B, et al. Aktuelle Fortschritte bei siliziumbasierten Elektroden: von der Grundlagenforschung zur Praxis Anwendungen.Advanced Materials, 2021, 33(16): 2004577.
[4] LI P, ZHAO G Q, ZHENG X B, et al. Aktuelle Fortschritte auf Siliziumbasis Anodenmaterialien für praktische Lithium-Ionen-Batterieanwendungen.Energie Speichermaterialien, 2018, 15: 422.
[5] LIU X H, ZHONG L, HUANG S, et al. Größenabhängig Bruch von Silizium-Nanopartikeln während der Lithiierung.ACS Nano, 2012, 6(2): 1522.
[6] LUO W, WANG Y X, CHOU S L, et al. Kritische Dicke von Phenol Kohlenstoff-Grenzflächenschicht auf Harzbasis zur Verbesserung der Langzeitstabilität von Silizium-Nanopartikel-Anoden.Nano Energy, 2016, 27: 255.
[7] DOU F, SHI L Y, CHEN G R,Silizium/Kohlenstoff-Verbundanodenmaterialien für Lithium-Ionen-Batterien.Electrochemical Energy Reviews, 2019, 2(1): 149.
[8] JIA H P, ZOU L F, GAO P Y, et al. Hohe Leistung Siliziumanoden durch nicht brennbare, lokalisierte hohe Konzentration Elektrolyte.Advanced Energy Materials, 2019, 9(31): 1900784.
[9] CHOI S H, KWON T W, COSKUN A, et al. Hochelastisch Bindemittel, die Polyrotaxane für Silizium-Mikropartikelanoden in Lithium integrieren Ionenbatterien.Science, 2017, 357: 279.
[10] LI Z H, ZHANG YP, LIU T F, et al.Siliziumanode mit hoher anfänglicher Coulomb-Effizienz durch moduliertes trifunktionales Bindemittel für Lithium-Ionen-Batterien mit hoher Flächenkapazität.Advanced Energy Materialien, 2020, 10(20): 1903110.
[11] XU Z L, CAO K, ABOUALI S, et al.Untersuchung der Lithiierungsmechanismen von kohlenstoffbeschichtetem Hochleistungs-Si Anoden durch In-situ-Mikroskopie.Energy Storage Materials, 2016, 3: 45.
[12] TEKI R, MONI K D, RAHUL K, et al.Nanostrukturierte Siliziumanoden für Lithium-Ionen-Akkus. Klein, 2009, 5(20): 2236.
[13] XIA S X, ZHANG X, LUO LL, et al. Sehr stabil und Ultrahochleistungs-Li-Metallanode, ermöglicht durch fluorierte Kohlenstofffasern. Small, 2021, 17: 2006002.
[14] ZHANG S L, WANG X, HO K S, et al.Raman-Spektren in a breiter Frequenzbereich von porösem Silizium vom p-Typ.Journal of Applied Physik, 1994, 76(5): 3016.
[15] HUANG W, WANG Y, LUO G H, et al. 99,9 % Reinheit mehrwandiger Kohlenstoff-Nanoröhren durch Vakuum Hochtemperaturglühen. Carbon, 2003, 41(13): 2585.
[16] MCDOWELL M T, LEE S W, NIX W D, et al.25. Jahrestag Artikel: Verständnis der Lithiierung von Silizium und anderen Legierungsanoden für Lithium-Ionen-Batterien.Advanced Materials, 2013, 25(36): 4966.
[17] KEY B, MORCRETTE M, TARASCON J M.Paarverteilungsfunktionsanalyse und Festkörper-NMR-Untersuchungen von Silizium Elektroden für Lithium-Ionen-Batterien: Verständnis der (De)Lithiierung Mechanismen. Journal of American Chemical Society, 2011, 133(3): 503.
[18] GAO H, XIAO L S, PLUMEL I, et al.Parasitische Reaktionen im Nanobereich Siliziumanoden für Lithium-Ionen-Batterien.Nano Letters, 2017, 17(3): 1512.
[19] CHEN J, FAN X L, LI Q, et al.Elektrolytdesign für LiF-reich Festelektrolyt-Schnittstellen zur Ermöglichung leistungsstarker Anoden aus Legierungen in Mikrogröße für Batterien.Nature Energy, 2020, 5(5): 386.
[20] ZHANG P, GAO Y Q, RU Q, et al.Skalierbare Herstellung von porösen Nano-Silizium/TiN@Kohlenstoff-Anode für Lithium-Ionen-Batterien. Angewandte Oberfläche Science, 2019, 498: 143829.
[21] SU M R, WAN H F, LIU Y J, et al.Mehrschichtig Kohlenstoffbeschichteter Verbundwerkstoff auf Si-Basis als Anode für Lithium-Ionen-Batterien. Pulver Technologie, 2018, 323: 294.
[22] PU J B, QIN J, WANG Y Z, et al.Synthese der Mikro-Nano-Kugelstruktur Silizium-Kohlenstoff-Verbundstoff als Anodenmaterial für Lithium-Ionen-Batterien. Chemisch Physics Letters, 2022, 806: 140006.
[23] GAO R S, TANG J, YU X L, et al.Ein sandwichartiger Silizium-Kohlenstoff Durch Oberflächenpolymerisation hergestellter Verbundwerkstoff zur schnellen Lithium-Ionen-Speicherung.
Nanoenergie, 2020, 70: 104444.
[24] GONG X H, ZHENG Y B, ZHENG J, et al.Dotterschale Silizium/Kohlenstoff-Verbundwerkstoffe, hergestellt aus einer Aluminium-Silizium-Legierung als Anode Materialien für Lithium-Ionen-Batterien.Ionics, 2021, 27: 1939.
[25] LIA Y R, WANG RY, ZHANG J W, et al.Sandwich Struktur von kohlenstoffbeschichteten Silizium-/Kohlenstoff-Nanofaser-Anoden für Lithium-Ionen Batterien.Ceramics International, 2019, 45: 16195.
[26] YANG X M UND ROGACH A L. Elektrochemische Techniken in der Batterieforschung: ein Tutorial für Nichtelektrochemiker.Advanced Energy Materials, 2019, 9(25): 1900747.



