Kategorien
neuer Blog
- Leitfaden zur Auswahl von Batterieelektrolyten: Was Einkaufsmanager wissen müssen
- Ausrüstung für Knopfzellenlabore: Die vollständige Checkliste für Batterie-Forschungs- und Entwicklungslabore
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
Tags
Na3Zr2Si2PO12 Keramikelektrolyte für Na-Ionen-Batterien
Na3Zr2Si2PO12 Keramik Elektrolyte für Na-Ionen-Batterien: Herstellung mit der Sprühtrocknungsmethode und deren Methoden Eigenschaft
Autor:LI Wenkai, ZHAO Ning, BI Zhijie, GUO Xiangxin. Na3Zr2Si2PO12 Keramische Elektrolyte für Na-Ionen-Batterien: Vorbereitung mit Sprühtrocknungsverfahren und seine Eigenschaften. Journal of Inorganic Materials, 2022, 37(2): 189-196 DOI:10.15541/jim20210486
Zusammenfassung
Na-Ionen-Batterien, die derzeit brennbare und explosive organische Stoffe verwenden Elektrolyte müssen nun dringend Hochleistungs-Natriumionen-Feststoffe entwickeln Elektrolyt, um eine sicherere und praktischere Anwendung zu realisieren. Na3Zr2Si2PO12 ist eines davon aufgrund seines breiten elektrochemischen Fensters der vielversprechendste feste Natriumelektrolyt, hohe mechanische Festigkeit, hervorragende Luftstabilität und hohe Ionenleitfähigkeit. Ursache ist jedoch die inhomogene Vermischung der Keramikpartikel mit den Bindemitteln Viel mehr Poren in den Grünkörpern machen es schwierig, eine hohe Dichte zu erreichen und hochleitfähige Keramikelektrolyte nach dem Sintern. Hier das Spray Die Trocknungsmethode wurde verwendet, um Na3Zr2Si2PO12 Partikel zu ermöglichen gleichmäßig mit Bindemitteln umhüllt und zu kugelförmigen Sekundärbindemitteln granuliert. Der Normalverteilte Partikel im vorbereiteten Zustand können effektiv miteinander in Kontakt kommen und Reduzieren Sie die Porosität des keramischen Grünkörpers. Nach dem Sintern Na3Zr2Si2PO12 Keramik Pellets durch Sprühtrocknung weisen eine relative Dichte von 97,5 % auf und eine Ionenleitfähigkeit von 6,96×10-4 Sâcm-1 bei Raum Temperatur. Im Gegensatz dazu die relative Dichte und Raumtemperatur Ionenleitfähigkeit von Na3Zr2Si2PO12-Keramikpellets ohne Sprühtrocknung hergestellte Proben haben nur 88,1 % bzw. 4,94 × 10-4 Sâcm-1.
Schlüsselwörterï¼ Festelektrolyt; Sprühtrocknungsmethode; Dichte; Ionenleitfähigkeit; Na3Zr2Si2PO12
Natriumionen und Lithiumionen gehören beide dazu die erste Hauptgruppe, haben ähnliche chemische Eigenschaften und Interkalation Mechanismen und sind reich an Ressourcenreserven. Daher Natrium-Ionen-Batterien kann Lithium-Ionen-Batterien ergänzen [1, 2, 3]. Natrium-Ionen-Batterien enthalten entflammbare, flüchtige organische Elektrolyte stellen Sicherheitsbedenken dar und sind begrenzt Energiedichte. Werden Festelektrolyte anstelle von Flüssigelektrolyten verwendet, Es wird erwartet, dass Sicherheitsprobleme gelöst werden [4,5,6,7,8]. Anorganische Festelektrolyte haben ein breites elektrochemisches Fenster und können mit einer Hochspannungskathode kombiniert werden Materialien und erhöht dadurch die Energiedichte von Batterien [9]. Jedoch, Feste Elektrolyte stehen vor Herausforderungen wie geringer Ionenleitfähigkeit und sind schwierig Ionenübertragung an der Grenzfläche zwischen Elektroden und Elektrolyten. Während Um die Grenzfläche zu optimieren, müssen zunächst Festelektrolyte gefunden werden hohe Ionenleitfähigkeit [10, 11, 12].
Derzeit ist das am besten untersuchte Natriumion Anorganische Festelektrolyte umfassen hauptsächlich Na-βâ-Al2O3, NASICON-Typ und Sulfid. Darunter sind schnelle Ionen vom Typ NASICON (Sodium Super Ion Conductors). Leiter haben großes Potenzial für Anwendungen in Festkörper-Natriumionenbatterien aufgrund ihres breiten elektrochemischen Fensters, hoher mechanischer Festigkeit und Stabilität gegenüber Luft und eine hohe Ionenleitfähigkeit [13,14] . Es wurde ursprünglich von gemeldet Goodenough und Hong et al. [15,16]. Die allgemeine Formel lautet Na1+xZr2SixP3-xO12 (0â¤xâ¤3), eine kontinuierliche feste Lösung, die aus NaZr2(PO4)3 und gebildet wird Na4Zr2(SiO4)3 und verfügt über einen offenen dreidimensionalen Na+-Übertragungskanal. Na1+xZr2SixP3-xO12 hat zwei Strukturen: Rautenstruktur (R-3c) und monoklin Struktur (C2/c, 1,8â¤xâ¤2,2). Wenn x=2, hat Na3Zr2Si2PO12 die höchste Ionenzahl Leitfähigkeit. Bei 300 â kann die Ionenleitfähigkeit von Na3Zr2Si2PO12 0,2 Sâcm-1 erreichen, was nahe an der Ionenleitfähigkeit von Na-βâ-Al2O3 (0,1~) liegt 0,3 Sâcm-1) [15]. Das aktuelle Ion bei Raumtemperatur Die in der Literatur [17,18] angegebene Leitfähigkeit von Na3Zr2Si2PO12 beträgt ca. ~10-4 Sâcm-1. Elementdotierung Zur Verbesserung der Ionenleitfähigkeit werden üblicherweise Methoden eingesetzt. Da der NASICON solide ist Elektrolyt hat eine offene Gerüststruktur und kann mit einer Vielzahl von Substanzen dotiert werden Elemente. Zu den Elementen, die Zr4+ ersetzen, gehören beispielsweise Mg2+, Zn2+, Al3+, Sc3+, Y3+, La3+, Ti4+, Hf 4+, Nb5+, Ta5+ usw. [17, 18, 19, 20, 21, 22]. Diese Als Ersatz für P5+ gelten Ge5+ und As5+ [22]. Zusätzlich zur Elementdotierung, Auch die Erhöhung der Dichte von Na3Zr2Si2PO12-Keramikplatten ist eine gängige Methode um ihre Ionenleitfähigkeit zu verbessern. Kürzlich haben Yang et al. [18] verwendetes Element Dotierung kombiniert mit Sintern in einer Sauerstoffatmosphäre, um eine hohe Synthese zu erreichen dichtes Na3,2+2xZr2-x ZnxSi2,2P0,8O12 (0â¤xâ¤0,15). Wenn x=0,1, der Raum Temperatur erreicht die Ionenleitfähigkeit den Maximalwert (5,27Ã10-3 Sâcm-1). Die Herstellungsmethoden des Na3Zr2Si2PO12-Keramikelektrolyten Dazu gehören: konventionelles Sintern (CS), Flüssigphasensintern (LPS), Funken Plasmasintern (SPS), Mikrowellensintern (MWS) und Kaltsinterverfahren (CSP) [18-21,23-29]. Unter ihnen haben Huang et al. [20] verwendeten konventionelles Sintern Methoden zur Erhöhung der Dichte von Keramik durch Dotierung mit Ga3+. Eine Keramik Es wurde ein Elektrolyt mit höherer Ionenleitfähigkeit bei Raumtemperatur (1,06 × 10-3 Sâcm-1) und niedrigerer elektronischer Leitfähigkeit (6,17 × 10-8 Sâcm-1) erhalten. ZHANG et al. [21] übernahmen das konventionelle Sintern Methode durch Einführung des Kations La3+. Es entsteht die Zwischenphase Na3La(PO4)2 an der Korngrenze und einer Na3,3Zr1,7La0,3Si2PO12-Keramikplatte mit a Es wird eine Dichte von bis zu 99,6 % erreicht. Das entsprechende Raumtemperatur-Ion Die Leitfähigkeit kann 3,4·10-3 Sâcm-1 erreichen. WANG et al. [23] verwendet Mikrowellensintern (MWS), um Na3Zr2Si2PO12-Keramik mit hoher Dichte zu erhalten von 96 % bei einer niedrigen Sintertemperatur von 850 °C und nur 0,5 Stunden gehalten, wodurch das Sintern reduziert wird Kosten. Die Werte der relativen Dichte (rrelative), der Ionenleitfähigkeit (Ït) und Aktivierungsenergie (Ea) von keramischen Elektrolyten, die mit verschiedenen Methoden hergestellt wurden sind in Tabelle 1 aufgeführt.
Tabelle 1 Schlüsselparameter des NASICON-Typs Materialien für verschiedene Sinterverfahren
|
Sintermethode |
Zusammensetzung |
Sintern |
Sintern |
Zeit/h |
rrelative/% |
st/(Sâcm-1) |
Ea/eV |
Ref. |
|
CSP |
Na3.256Mg0.128Zr1.872Si2PO12 |
140 |
Keine |
1 |
82,9 |
0,41´10-4 |
- |
[19] |
|
FH-CSP |
Na3Zr2Si2PO12 |
375 |
NaOH |
3 |
93 |
2.2´10-4 |
0,32 |
[24] |
|
LPS |
Na3Zr2Si2PO12 |
1150 |
NaF |
24 |
- |
1,7´10-3 |
0,28 |
[25] |
|
LPS |
Na3Zr2Si2PO12 |
900 |
Na3BO3 |
10 |
93 |
1,4´10-3 |
- |
[26] |
|
LPS |
Na3Zr2Si2PO12 |
1175 |
Na3SiO3 |
10 |
93 |
1,45´10-3 |
- |
[27] |
|
SPS |
Na3.4Zr1.6Sc0.4Si2PO12 |
1100 |
KOHaq |
0,1 |
95 |
9,3´10-4 |
- |
[28] |
|
SPS |
Na3Zr2Si2PO12 |
1210 |
Keine |
0,5 |
97,0 |
1,7´10-3 |
0,28 |
[29] |
|
MWS |
Na3Zr2Si2PO12 |
850 |
Keine |
0,5 |
96 |
2,5´10-4 |
0,31 |
[23] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Keine |
16 |
71,4 |
1,7´10-4 |
0,36 |
[20] |
|
CS |
Na3.1Zr1.9Ga0.1Si2PO12 |
1250 |
Keine |
16 |
86,5 |
1,06´10-3 |
0,29 |
[20] |
|
CS |
Na3Zr2Si2PO12 |
1200 |
Keine |
24 |
87,6 |
6,7´10-4 |
0,353 |
[21] |
|
CS |
Na3.3Zr1.7La0.3Si2PO12 |
1200 |
Keine |
24 |
99,6 |
3,4´10-3 |
0,291 |
[21] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Keine |
- |
84.02 |
2.17´10-4 |
0,407 |
[18] |
|
O2-CS |
Na3,4Zr1,9Zn0,1Si2,2P0,8O12 |
1250 |
Keine |
- |
99,46 |
5,27´10-3 |
0,285 |
[18] |
|
CS |
Na3Zr2Si2PO12 |
1250 |
Keine |
6 |
88,1 |
4,94´10-4 |
0,34 |
Diese Arbeit |
|
SD-CS |
Na3Zr2Si2PO12 |
1250 |
Keine |
6 |
97,5 |
6,96´10-4 |
0,32 |
Diese Arbeit |
CS: konventionelles Sintern; SD: Sprühtrocknung; O2-CS: konventionelles Sintern in Reinform Sauerstoff; CSP: Kaltsinterverfahren; FH-CSP: Kaltsinterung mit geschmolzenem Hydroxid Verfahren; MWS: Mikrowellensintern; LPS: Flüssigphasensintern; SPS: Funke Plasmasintern
Herkömmliche Methoden verwenden Pulver, das von hergestellt wird Direktes Sintern, um mit einem Bindemittel zu mischen, um Keramikkörperpulver herzustellen, und dann werden pulvergeformt und bei hoher Temperatur gesintert, um Keramik zu erhalten [30, 31, 32]. Während des Mahl- und Mischvorgangs kann es jedoch zu ungleichmäßiger Vermischung kommen des Bindemittels und der Keramikpartikel und es kommt zu einem schlechten Kontakt zwischen den Partikeln Im Grünkörper gibt es viele Poren, die die Vorbereitung der Keramik erschweren Elektrolyte mit hoher Dichte und hoher Ionenleitfähigkeit. Sprühtrocknung ist eine Schnelltrocknungsmethode, bei der die Aufschlämmung mithilfe eines Zerstäubers in Tröpfchen zerstäubt wird und trocknet die Tröpfchen mit heißer Luft, um Pulver zu erhalten. Die Teilchen der Durch Sprühtrocknung hergestellte Pulver sind kugelförmig und das Bindemittel kann gleichmäßig sein auf die Oberfläche der Partikel aufgetragen [33]. KOU et al. [34] verwendete Sprühtrocknung kombiniert mit Hochtemperatursintern zur Synthese von Festelektrolyten Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12 (LATSP) mit Ionen bei hoher Raumtemperatur Leitfähigkeit. Wenn x=0,05, erreicht die Ionenleitfähigkeit bei Raumtemperatur a maximal 1,053Ã10-4 Sâcm-1 und verdichtet Die Dichte beträgt 2,892 gâcm-3, was nahe an der theoretischen Dichte liegt von LATSP von 2,94 gâcm-3. Es ist zu erkennen, dass die Sprühtrocknung funktioniert gewisse Vorteile bei der Verbesserung der Dichte und Ionenleitfähigkeit von Keramik Elektrolyte. Angesichts der Vorteile der Sprühtrocknung ist die Wirkung von Element Eine Dotierung der Keramikdichte und der Ionenleitfähigkeit sollte berücksichtigt werden. Das Die Studie wählte Na3Zr2Si2PO12 als Forschungsobjekt und führte das Spray ein Granulierungsverfahren in die Vorbereitung von Pulvermaterialien ein Bereiten Sie einen Na3Zr2Si2PO12-Keramikelektrolyten mit hoher Dichte und hohem Ionengehalt vor Leitfähigkeit.
1 Experimentelle Methode
1.1 Materialvorbereitung
Herstellungsmethode für Na3Zr2Si2PO12-Pulver: Wiegen Sie Na2CO3 (Aladdin, 99,99 %), NH4H2PO4 (Aladdin, 99 %), ZrO2 (Aladdin, 99,99 %) und SiO2 (Aladdin, 99,99 %) entsprechend dem stöchiometrischen Verhältnis. In um die Verflüchtigung von Na und P beim Sintern auszugleichen Bei diesem Verfahren enthält das Rohmaterial einen Überschuss von 8 % Na2CO3 und einen Überschuss von 15 % NH4H2PO4 [25]. Als Kugelmahlmedium wurden Zirkonoxidkugeln verwendet Das Material/Kugel-Gewichtsverhältnis betrug 1:3, als Dispersion wurde absolutes Ethanol verwendet Medium, und die Kugelmühle wurde 12 Stunden lang zum Mahlen in der Kugelmühle verwendet. Die Kugelmühle Die Aufschlämmung wurde 12 Stunden lang in einem Ofen bei 80 °C getrocknet. Das getrocknete Pulver wurde gemahlen und Durch ein 150-Mesh-Sieb (100 µm) geleitet und dann in einen 400 °C heißen Ofen überführt Aluminiumoxidtiegel für 2 Stunden. CO32- und NH4+ aus dem Vorläufer entfernen und dann erhitzen Es wird zur Kalzinierung auf 1000–1150 °C erhitzt und nach 12 Stunden getempert, um es zu erhalten Na3Zr2Si2PO12-Pulver.
Herstellungsverfahren für Na3Zr2Si2PO12-Keramik Blätter: Um den Einfluss der Na3Zr2Si2PO12-Partikelgröße auf die zu untersuchen Um die Dichte von Keramikplatten zu ermitteln, wurden zwei Sätze von Kontrollexperimenten entworfen. Der Die erste Gruppe verwendete herkömmliche Methoden und fügte 2 % (Massenanteil) Polyvinyl hinzu Alkohol (Aladdin, Mw ~ 205.000) als Bindemittel zu Na3Zr2Si2PO12-Pulver in reiner Phase hinzufügen absolutes Ethanol und 12 Stunden Mahlen in der Kugelmühle. Das Pulver nach dem Mahlen in der Kugelmühle ist getrocknet, gemahlen und gesiebt, um ein Pulver zu erhalten, das mit einem Bindemittel auf den Partikeln beschichtet ist Oberfläche. Das Pulver wird mit einer Edelstahlpresse bei 200 MPa einachsig kaltgepresst Stahlform zur Herstellung eines Grünkörpers von Ï12 mm, aufgezeichnet als GB. . Um zu reduzieren die Verflüchtigung von Na und P beim Sinterprozess von Keramikplatten, Der Grünkörper wurde im Mutterpulver vergraben und 6 Jahre lang bei 1250 °C gesintert Stunden und dann mit einer Heizrate von 4 °C/min geglüht. Das erhaltene Der Keramikelektrolyt Na3Zr2Si2PO12 wurde als CS-NZSP bezeichnet. Die zweite Gruppe verwendeten einen Sprühtrockner (ADL311S, Yamato, Japan), um Na3Zr2Si2PO12-Pulver zu granulieren. Fügen Sie 2 % (Massenanteil) Polyvinylalkohol (Aladdin, Mw ~205.000) als Bindemittel und 2 % hinzu. Polyethylenglykol (Aladdin, Mn=1000) als Dispergiermittel für das Na3Zr2Si2PO12-Pulver, und absolutes Ethanol hinzufügen. Bereiten Sie eine Suspension mit einem Feststoffgehalt von 15 % der Masse vor fraktionieren und 12 Stunden lang in der Kugelmühle mahlen. Die in der Kugelmühle gemahlene Suspension wurde sprühgetrocknet mit einer Einlasstemperatur von 130 °C und einer Zulaufgeschwindigkeit von 5 ml/min. Der Na3Zr2Si2PO12-Pulver wurde durch einen Zyklonabscheider gesammelt. Die Tablettierung und Keramiksinterverfahren waren die gleichen wie bei der ersten Gruppe, und Der erhaltene Na3Zr2Si2PO12-Grünkörper und der Keramikelektrolyt wurden aufgezeichnet als SD-GB bzw. SD-CS-NZSP. Oberflächenpolierbehandlung von Keramik Fliesen: Verwenden Sie zunächst Schleifpapier der Maschenweite 400 (38 µm) zum Grobpolieren und anschließend Verwenden Sie Schleifpapier der Maschenweite 1200 (2,1 µm) zum Feinpolieren, bis die Keramik erreicht ist Oberfläche ist glatt. Die Durchmesser des Keramikelektrolyten CS-NZSP und SD-CS-NZSP Die Bleche sind (11,3 ± 0,1) bzw. (10,3 ± 0,1) mm und die Dicke beträgt (1,0 ± 0,1) mm.
1.2 Physikalische Charakterisierung von Materialien
Die Phasenanalyse der Proben war durchgeführt mit einem Röntgendiffraktometer (XRD, Bruker, D8 Advance). Der Die Strahlungsquelle ist CuKα, der Röhrendruck beträgt 40 kV, der Röhrenfluss beträgt 40 mA, Die Scanrate beträgt 2 (°)/min und der Scanbereich beträgt 2θ= 10°~80°. Scannen Elektronenmikroskop (REM, Hitachi, S-4800) und Transmissionselektronenmikroskop (TEM, JEOL, JEM-2100F) wurden zur Analyse der Morphologie der Proben verwendet Für die Elementaranalyse wurde das konfigurierte EDX-Zubehör verwendet.
1.3 Messung der elektrischen Leitfähigkeit aus Keramikplatten
Die elektrochemische Impedanzspektroskopie (EIS) der Probe wurde mit einer elektrochemischen Workstation getestet. Der Test Der Frequenzbereich beträgt 7 MHz ~ 0,1 Hz, die angelegte Spannung beträgt 10 mV, die Testkurve wird angepasst und die Ionenleitfähigkeit des Keramikstücks wird mit berechnet Formel (1).
Ï=L/(RÃS) (1)
In der Formel ist L die Dicke des Keramikplatte (cm), R ist der Widerstand (Ω), S ist die Sperrelektrodenfläche (cm2) und Ï ist die Ionenleitfähigkeit (Sâcm-1).
Die elektronische Leitfähigkeit der Probe wurde mit Gleichstrompolarisation (DC) und einer konstanten Spannung von 5 getestet V und einer Dauer von 5000 s. Der Ordinatenwert nach der Kurve wird stabil ist der Polarisationsstromwert. Verwenden Sie die Formeln (2, 3), um die zu berechnen elektronische Leitfähigkeit und Natriumionenwanderungszahl der Keramikplatte.
Ïe=LÃI/(VÃS) (2)
t=(Ï-Ïe)/Ï (3)
In der Formel ist L die Dicke des Keramikplatte (cm), I ist der Polarisationsstrom (A), V ist die Spannung (V), S ist die blockierende Elektrodenfläche (cm2) und Ïe ist die elektronische Leitfähigkeit (Sâcm-1). Diese Arbeit verwendet Au als Sperrelektrode. Vorbereitung von Blockierungselektrode: Bedampfungsbeschichtungsgerät mit hohem Vakuumwiderstand verwenden (VZZ-300) zur Verdampfung der Verdampfungsquelle Au durch Widerstandsheizung, und verdunstet es auf die Oberfläche der Keramikplatte. Die Keramikplatte ist befestigt in einer Ferrule mit einem Innendurchmesser von 8 mm.
2 Ergebnisse und Diskussion
2.1 Phasenstruktur und Morphologie Charakterisierung von Na3Zr2Si2PO12
Um das Sintern zu optimieren Temperatur von Na3Zr2Si2PO12, das Pulver wurde bei 1000, 1050, 1100 und gesintert 1150 â bzw. Die Röntgenbeugungsmuster der erhaltenen Proben Das Sintern bei unterschiedlichen Temperaturen ist in Abbildung 1 dargestellt Aus der Abbildung geht hervor, dass bei einer Sintertemperatur von 1000 °C die Hauptphase entsteht Es wurde eine Menge Na3Zr2Si2PO12 erzeugt, es gibt jedoch Na2ZrSi2O7- und ZrO2-Verunreinigungen Phasen und die Beugungspeakintensität der Hauptphase ist schwach und die Die Halbwertsbreite ist groß, was darauf hindeutet, dass das Sinterprodukt schlecht ist Kristallinität. Wenn die Sintertemperatur 1100 °C beträgt, entsteht die ZrO2-Verunreinigung Phase verschwindet und die Beugungspeakintensität der Na2ZrSi2O7-Verunreinigung verschwindet Die Phase wird schwächer, was auf eine Erhöhung der Sintertemperatur hinweist vorteilhaft für die Eliminierung der Verunreinigungsphase. Die Beugungspeaks der Produkte, die bei 1100 und 1150 °C gesintert wurden, haben kleinere Halbwertsbreiten als die Beugungspeaks der bei 1000 °C gesinterten Produkte zeigen, dass die Je höher die Sintertemperatur, desto besser ist die Kristallinität des Produkts. Verglichen mit dem 1000 â gesinterten Produkt sind die Beugungspeaks des 1150 â Das gesinterte Produkt wird bei 2θ = 19,2°, 27,5° und 30,5° gespalten. Dies zeigt, dass die Material geht von einer rhombischen Phase mit geringer Ionenleitfähigkeit in eine über monokline Phase mit hoher Ionenleitfähigkeit [25,35]. Und der Beugungspeak stimmt mit dem Standard-PDF-84-1200-Beugungspeak überein, was darauf hinweist 1150 °C ist die Phasenbildungstemperatur des Na3Zr2Si2PO12-Festelektrolyten mit einer monoklinen Struktur mit hoher Ionenleitfähigkeit.
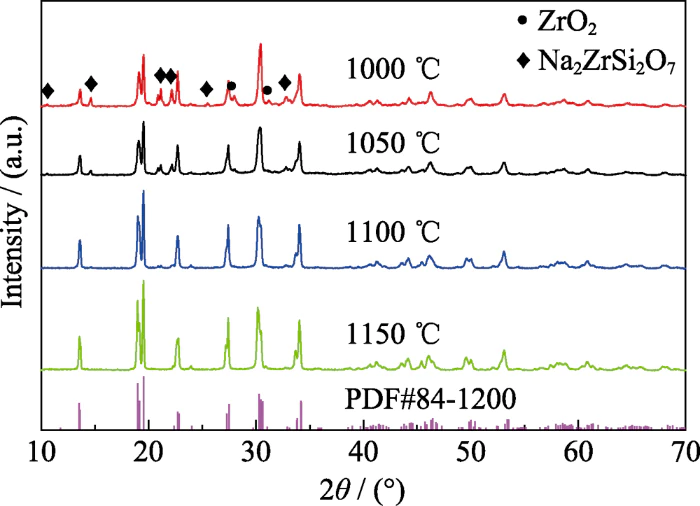
Abb. 1 XRD Muster aus gesintertem Na3Zr2Si2PO12-Pulver bei unterschiedlichen Temperaturen
Abbildung 2 zeigt SEM-Fotos und TEM-Fotos von Na3Zr2Si2PO12-Partikel, erhalten durch konventionelles Mischen und Sprühtrocknen Methoden. Abbildung 2(a) ist ein SEM-Foto von Na3Zr2Si2PO12-Partikeln danach konventionelles Mischen. Auf dem Bild ist zu erkennen, dass die Form des Die Partikel sind unregelmäßig und der Durchmesser einiger Partikel erreicht 20 µm. was darauf hinweist, dass die Partikel nach dem herkömmlichen Mischen groß sind und ungleichmäßig geformt. Abbildung 2(b~c) zeigt SEM-Fotos von Na3Zr2Si2PO12-Partikeln nach der Sprühtrocknung. Die Partikel sind kugelförmig und der Partikeldurchmesser beträgt kleiner als 5 µm, was darauf hinweist, dass die Partikelform regelmäßig ist und der Partikel Die Größenverteilung ist nach der Sprühtrocknung konzentrierter. Abbildung 2(d) ist ein TEM Foto der Oberfläche von Na3Zr2Si2PO12-Partikeln nach der Sprühtrocknung. Der Die Partikeloberfläche wird gleichmäßig mit einer Bindemittelschicht mit einer Dicke von beschichtet ca. 5 nm, was zu einem engeren Kontakt zwischen Keramikpartikeln führt.

Abb. 2 REM-Bilder von Na3Zr2Si2PO12 Partikeln nach konventioneller Untersuchung Mischen (a) und Sprühtrocknen (b-c) und TEM-Bild (d) der Na3Zr2Si2PO12-Partikeloberfläche nach dem Sprühen Trocknen
Abbildung 3 zeigt die Partikelgröße Verteilungsdiagramm des mit Polyvinylalkohol beschichteten Na3Zr2Si2PO12 (NZSP) erhalten durch herkömmliches Mischen und das mit Polyvinylalkohol beschichtete Na3Zr2Si2PO12 (SD-NZSP), erhalten durch die Sprühtrocknungsmethode. Es ist zu erkennen, dass die Die Halbwertsbreite der SD-NZSP-Partikelgrößenverteilungskurve ist schmaler als die der NZSP-Partikelgrößenkurve, was darauf hinweist, dass die Partikelgröße Die Verteilung nach der Sprühtrocknung ist konzentrierter. Das ist grundsätzlich so im Einklang mit den in den REM-Fotos in Abbildung 2(a,b) gezeigten Ergebnissen. In Darüber hinaus liegt die Partikelgrößenverteilungskurve nach der Sprühtrocknung nahe bei a Normalverteilung. Durch diese Partikelgrößenabstufung kann die Partikelgröße effektiv erhöht werden Kontakt zwischen Partikeln und verringern die Porosität des Grünkörpers. Wie gezeigt In Tabelle 2 ist die Dichte des von der hergestellten Na3Zr2Si2PO12-Grünkörpers angegeben Die herkömmliche Mischmethode beträgt 83,01 % und die Dichte ist Na3Zr2Si2PO12 Der Anteil des im Sprühtrocknungsverfahren hergestellten Grünkörpers wird auf 89,12 % erhöht. In Ordnung um den Einfluss der Na3Zr2Si2PO12-Partikelgröße auf die Keramikdichte weiter zu untersuchen und Leitfähigkeit, Querschnittsabtastung, Dichtemessung und Leitfähigkeitstests wurden an Na3Zr2Si2PO12-Keramikplatten durchgeführt, die von erhalten wurden konventionelle Misch- und Sprühtrocknungsmethoden.
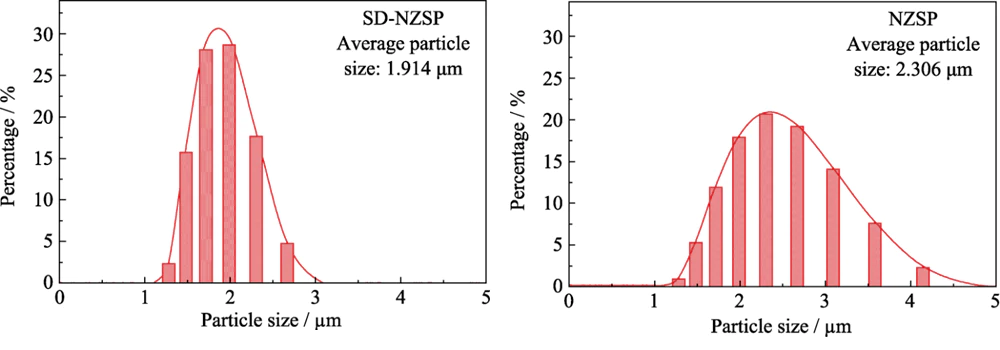
Abb. 3 Na3Zr2Si2PO12 Partikelgröße Profile des konventionellen Mischens (NZSP) und der Sprühtrocknung (SD-NZSP) gemessen durch Laser-Partikelanalysator
Tabelle 2 Sinterparameter und Dichtemessparameter und Messergebnisse des Festelektrolyten Na3Zr2Si2PO12 Grünkörper und Keramikplatten
|
Beispiel |
Prozesstemp./â |
Zeit/h |
m/g |
Rethanol/(g·cm-3) |
muntergetaucht/g |
rreal/(g·cm-3) |
rtheoretisch/(g·cm-3) |
rrelative/% |
|
GB |
- |
- |
0,2902 |
0,785 |
0,2056 |
2,693 |
3.244 |
83.01 |
|
SD-GB |
- |
- |
0,2880 |
0.785 |
0,2098 |
2.891 |
3.244 |
89,12 |
|
CS-NZSP |
1250 |
6 |
0,2672 |
0,785 |
0,1938 |
2.858 |
3.244 |
88,10 |
|
SD-CS-NZSP |
1250 |
6 |
0,2644 |
0,785 |
0,1988 |
3.164 |
3.244 |
97,53 |
Abbildung 4 zeigt das physikalische Bild des Na3Zr2Si2PO12-Keramikplatte, ihre Querschnittsmorphologie und Elementarstruktur Analysediagramm. Abbildung 4(a) zeigt die Querschnittsmorphologie des Keramikstück, das durch herkömmliche Sintermethode hergestellt wird. Es wurde beobachtet dass es im Querschnitt der Keramikplatte viele unregelmäßige Poren gab, und der lokale Porendurchmesser überstieg 5 µm. Der Grund liegt in der Partikelgröße Nach dem Mahlen ist es ungleichmäßig, es gibt größere Partikel und es gibt keine Naht Der Kontakt zwischen den Partikeln führt zu unregelmäßigeren Poren in der Keramik Blech während des sekundären Sinterprozesses. Abbildung 4(b) zeigt die Querschnittsmorphologie des durch Sprühtrocknung erhaltenen Keramikstücks Verfahren. Die Kristallkörner stehen in engem Kontakt miteinander und das ist der Fall keine offensichtlichen Poren. Dies zeigt, dass Na3Zr2Si2PO12-Partikel eine regelmäßige Form haben und eine konzentrierte Partikelgrößenverteilung kann leicht eine hohe Dichte erreichen Keramikplatten während des sekundären Sinterprozesses. Die Zunahme der Dichte spiegelt sich auch in der zunehmenden Schrumpfung des Keramikkörpers wider Sintern, wie in Abbildung 4(c) dargestellt. Auf der linken Seite ist ein Keramikstück zu sehen, das von erhalten wurde das herkömmliche Sinterverfahren, mit einem Durchmesser von 11,34 mm und einer Schrumpfung Rate von nur 5,5 %; Auf der rechten Seite ist ein durch Sprühtrocknung erhaltenes Keramikstück zu sehen Methode, mit einem Durchmesser von 10,36 mm und einer Schrumpfrate von 13,7 %. Um zu Um die Zusammensetzung jedes Elements in der Probe zu untersuchen, wurde eine Elementaranalyse durchgeführt durchgeführt am Querschnitt des Keramikstücks (Abbildung 4(b)) und Abbildung 4(d~g) wurde erhalten. Der Inhalt jedes Elements ist in Tabelle 3 aufgeführt Element ist gleichmäßig über den Querschnitt des Keramikstücks verteilt und Es gibt keine Aggregation von Elementen. Gemäß Tabelle 3 wird festgestellt, dass die Der Atomprozentsatz von Na und P beträgt 2,98:1, was im Wesentlichen mit dem übereinstimmt Chemische Standardformel von Na:P=3:1, was darauf hinweist, dass überschüssiges Na und P im Rohstoffe können die Verflüchtigung von Na und P während der Produktion kompensieren Sinterprozess.

Abb. 4 REM-Bilder von Schichtabschnitten für CS-NZSP (a) und SD-CS-NZSP (b), entsprechende Fotos (c) und Elementekartierungsbilder (d-g) von SD-CS-NZSP
Tabelle 3 Elementaranalyse des Na3Zr2Si2PO12 Keramikscheibenschnitts durch Sprühen Trocknen/%
|
Element |
O K |
Na K |
Si K |
P K |
Zr L |
|
Atomprozentsatz |
60,10 |
15.09 |
9,94 |
5.06 |
9,81 |
|
Gewichtsprozentsatz |
36,43 |
13.13 |
10,59 |
5,94 |
33,91 |
2.2 Dichte von Na3Zr2Si2PO12-Keramikplatten
Das Experiment maß die Dichte von Na3Zr2Si2PO12-Keramikplatten nach der Methode von Archimedes [30]. Um zu studieren die Auswirkung der Granulationsmethode auf die Dichte von Na3Zr2Si2PO12-Keramik Platten, in den experimentellen Parametern der Keramikplattenherstellung, die experimentelle Parameter (Sintertemperatur, Haltezeit usw.) der Die Kontrollversuchsgruppe blieb mit Ausnahme der Granulationsmethode gleich. In um den Einfluss experimenteller Messfehler auf die Dichte zu reduzieren Um die Ergebnisse zu ermitteln, wurden die Dichtemessungen an den Keramikplattenproben wiederholt erhalten durch jede Zubereitungsmethode im Experiment. Aus dem Experimentellen Die in Tabelle 4 gezeigten Daten zeigen, dass die Dichte der CS-NZSP-Keramik Die durch herkömmliche Sinterverfahren erhaltenen Bleche betragen grundsätzlich 88,1 % im Einklang mit den in der Literatur berichteten Ergebnissen [21]. Die Dichte von SD-CS-NZSP-Keramikplatten, die durch Sprühtrocknung erhalten werden, können 97,5 % erreichen der höchste Wert, der derzeit mit konventionellen Sinterverfahren ohne erreicht wird Elementdotierung. Sie ist sogar höher als die Dichte von Na3Zr2Si2PO12-Keramik Platten, die durch andere in der Literatur beschriebene Sintermethoden erhalten wurden. Wie zum Beispiel Mikrowellen-Sinterverfahren (96 %) [23], Kaltsinterverfahren (93 %) [24], flüssig Phasensinterverfahren (93 %) [26] und Entladungsplasmasinterverfahren (97,0 %) [29].
Tabelle 4 Ionenleitfähigkeit von CS-NZSP und SD-CS-NZSP bei Raumtemperatur
|
Beispiel |
sb/(S·cm-1) |
sgb/(S·cm-1) |
st/(S·cm-1) |
Ea/eV |
|
CS-NZSP |
1,28Ã10-3 |
8.03Ã10-4 |
4.94Ã10-4 |
0,34 |
|
SD-CS-NZSP |
1,64Ã10-3 |
1.21Ã10-3 |
6,96Ã10-4 |
0,32 |
2,3 Na3Zr2Si2PO12 elektrische Leistung test
Abbildung 5(a) zeigt die Raumtemperatur Elektrochemisches Impedanzspektrum (EIS) des Keramikwafers, erhalten durch konventionelles Sinterverfahren und Sprühtrocknungsverfahren. Der Halbkreis im Die Abbildung spiegelt die parallelen Impedanzeigenschaften der Korngrenze wider Impedanz und kapazitive Reaktanz. Der Schnittpunkt zwischen der linken Seite von Der Halbkreis und die Abszisse stellen den Widerstand des Korns dar. Der Die Spannweite des Halbkreises auf der Abszisse spiegelt den Widerstand des Korns wider Grenze, und die schräge Linie nach dem Halbkreis spiegelt die Impedanz wider Eigenschaften der Sperrelektrode/Elektrolyt-Grenzfläche [36]. Von Passend zum EIS in Abbildung 4, der Ionenleitfähigkeit von CS-NZSP und SD-CS-NZSP erhalten werden kann. Die experimentellen Daten sind in Tabelle 4 aufgeführt. Der Raum Temperatur-Ionenleitfähigkeit von SD-CS-NZSP, erhalten durch Sprühtrocknung Methode beträgt 6,96×10-4 Sâcm-1, was höher ist als das von CS-NZSP (4.94Ã10-4 Sâcm-1), erhalten durch die konventionelle Sintermethode. Durch die Bei der Datenanalyse der EIS-Anpassung ist ersichtlich, dass SD-CS-NZSP höher ist Die Dichte hat einen geringeren Korngrenzenwiderstand und eine höhere ionische Raumtemperatur Leitfähigkeit.
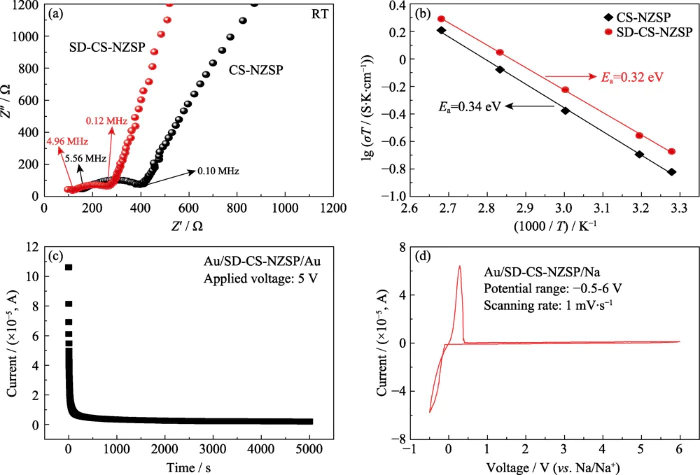
Abb. 5 (a) EIS-Spektren bei Raumtemperatur und (b) Arrhenius-Diagramme von CS-NZSP und SD-CS-NZSP; (c) DC-potentiostatische Polarisation Strom und (d) elektrochemisches Fenster für SD-CS-NZSP
Abbildung 5(b) zeigt die Arrhenius-Kurven von Raumtemperatur bis 100 °C für Keramikplatten, die durch unterschiedliche Herstellung erhalten wurden Methoden. Aus der Abbildung ist ersichtlich, dass ihre Leitfähigkeit mit zunimmt steigende Temperatur. Wenn die Temperatur 100 °C erreicht, sinkt die Leitfähigkeit von SD-CS-NZSP kann 5,24×10-3 Sâcm-1 erreichen, was einer Größenordnung von entspricht Größe höher als die Leitfähigkeit bei Raumtemperatur. Seine Aktivierungsenergie wird gemäß der Arrhenius-Gleichung angepasstÏ=Aexp(-Ea/kT)[7]. Die Aktivierungsenergien von CS-NZSP und SD-CS-NZSP wurden mit 0,34 bzw. 0,32 eV ermittelt ähneln dem Bericht von YANG et al. [18].
Feste Elektrolytmaterialien sollten vorhanden sein sowohl eine hohe Ionenleitfähigkeit als auch eine niedrige elektronische Leitfähigkeit. Daher ist die Die elektronische Leitfähigkeit von SD-CS-NZSP wurde mit Gleichstrom gemessen Polarisation (DC), und die entsprechende Polarisationskurve ist in Abbildung dargestellt 5(c). Aus der Abbildung ist ersichtlich, dass mit zunehmender Testzeit die Der Polarisationsstrom nimmt allmählich ab. wenn die Testzeit 5000 s erreicht, Der Polarisationsstrom (I=3,1 μA) ändert sich mit der Testzeit nicht mehr verlängert. Berechnet durch die Formeln (2, 3), die elektronische Leitfähigkeit von SD-CS-NZSP beträgt 1,23×10-7 Sâcm-1 und das Natriumion Die Migrationsnummer ist 0,9998. In der Studie wurde auch das elektrochemische Fenster gemessen von SD-CS-NZSP durch Cyclovoltammetrie (CV) [18]. Wie in Abbildung 5(d) gezeigt, zwei Bei etwa 0 V treten Oxidations- und Reduktionspeaks auf, die das Strippen darstellen bzw. Ablagerung von Natrium [20]. Abgesehen davon kein anderes Redox Innerhalb des gescannten Spannungsbereichs wurden Spitzen beobachtet. Das bedeutet, dass es sie gibt keine Stromänderung durch Zersetzung des Elektrolyten in der Spannung Bereich von 0 bis 6 V, was darauf hinweist, dass SD-CS-NZSP eine gute elektrochemische Stabilität aufweist. Das breite elektrochemische Fenster (6 V (gegenüber Na/Na+)) kann dem Natriumion entsprechen Festelektrolyt bis hin zu Hochspannungskathodenmaterialien, wie z Kathodenmaterialien auf Nickel-Mangan-Basis, was sich positiv auf die Verbesserung auswirkt Energiedichte von Natrium-Ionen-Batterien.
3 Fazit
Eine Hochtemperatur-Festphasenmethode war Wird zur Synthese von phasenreinem Na3Zr2Si2PO12-Pulver bei Sintertemperatur verwendet von 1150 °C durch Einbringen von überschüssigem Na und P in den Vorläufer. Mit Sprühtrocknung Um das Pulver kugelförmig zu granulieren, wird das Polyvinylalkohol-Bindemittel gleichmäßig verteilt auf der Oberfläche von Na3Zr2Si2PO12-Partikeln beschichtet und die Partikelgröße Die Verteilung liegt nahe an der Normalverteilung. Die Dichte des vorbereiteten Na3Zr2Si2PO12-Keramik erreicht 97,5 %. Eine erhöhte Dichte kann effektiv reduzieren Korngrenzenwiderstand und die Ionenleitfähigkeit erreicht 6,96 × 10-4 Sâcm-1 bei Raumtemperatur, was höher ist als bei Keramikplatten hergestellt durch herkömmliche Sintermethoden (4,94×10-4 Sâcm-1). Darüber hinaus ist die Durch die Sprühtrocknungsmethode hergestellte Keramik weist ein breites elektrochemisches Fenster auf (6 V (vs. Na/Na+)) und kann mit Hochspannungskathodenmaterialien kombiniert werden Erhöhen Sie die Energiedichte der Batterie. Es ist zu erkennen, dass das Spray Die Trocknungsmethode ist eine wirksame Methode zur Herstellung von Na3Zr2Si2PO12-Keramikelektrolyten mit hoher Dichte und hoher Ionenleitfähigkeit und ist für andere Typen geeignet von keramischen Festelektrolyten.
Referenzen
[1] JIAN Z L, ZHAO L, PAN H L, et al. Kohlenstoffbeschichtetes Na3V2(PO4)3 als neuartiges Elektrodenmaterial für Natriumionenbatterien. Electrochemistry Communications, 2012,14(1):86-89.
[2] ZHAO L, ZHAO JM, HU Y S, et al. Dinatriumterephthalat (Na2C8H4O4) als Hochleistungsanodenmaterial für kostengünstige Raumtemperatur-Natrium-Ionen-Batterie. Fortschrittliche Energiematerialien, 2012,2(8):962-965.
[3] RUAN Y L, GUO F, LIU J J, et al. Optimierung des Na3Zr2Si2PO12-Keramikelektrolyten und der Schnittstelle für hohe Hochleistungs-Festkörper-Natriumbatterie. Keramik International, 2019,45(2):1770-1776.
[4] VETTER J, NOVAK P, WAGNER M R, et al. Alterungsmechanismen in Lithium-Ionen-Batterien. Zeitschrift für Energiequellen, 2005,147(1/2):269-281.
[5] KAMAYA N, HOMMA K, YAMAKAWA Y, et al. A Lithium-Superionenleiter. Nature Materials, 2011,10(9):682-686.
[6] TARASCON J M, ARMAND M. Probleme und Herausforderungen für wiederaufladbare Lithiumbatterien. Natur, 2001,414(6861):359-367.
[7] KHOKHAR W A, ZHAO N, HUANG W L, et al. Unterschiedliches Verhalten der Metallpenetration in Na- und Li-Festelektrolyten. ACS Applied Materials & Interfaces, 12(48):53781-53787.
[8] OUDENHOVEN J F M, BAGGETTO L, NOTTEN P H L. All-Solid-State-Lithium-Ionen-Mikrobatterien: eine Übersicht über verschiedene drei- dimensionale Konzepte. Advanced Energy Materials, 2011,1(1):10-33.
[9] ZHAO C L, LIU L L, QI X G, et al. Festkörper-Natriumbatterien. Advanced Energy Materials, 2017,8(17):1703012.
[10] HAYASHI A, NOI K, SAKUDA A, et al. Superionische Glaskeramik-Elektrolyte für bei Raumtemperatur wiederaufladbares Natrium Batterien. Nature Communications, 2012,3:856.
[11] LOU SF, ZHANG F, FU C K, et al. Schnittstellenprobleme und Herausforderungen bei Festkörperbatterien: Lithium, Natrium, und darüber hinaus. Advanced Materials, 2020,33(6):2000721.
[12] HUANG W L, ZHAO N, BI Z J, et al. Kann Finden wir eine Lösung, um das Eindringen von Li durch feste Granatelektrolyte zu verhindern? Materialien heute Nano, 2020,10:100075.
[13] JIAN ZL, HU YS, JI XL, et al. NASICON-strukturierte Materialien zur Energiespeicherung. Fortschrittliche Materialien, 2016,29(20):1601925.
[14] HOU W R, GUO X W, SHEN X Y, et al. Festelektrolyte und Grenzflächen in Festkörper-Natriumbatterien: Fortschritte und Perspektive. Nanoenergie, 2018,52:279-291.
[15] GOODENOUGH J B, HONG H Y P, KAFALAS J A. Schneller Na+-Ionentransport in Skelettstrukturen. Materialforschungsbulletin, 1976,11(2):203-220.
[16] HONG H Y P. Kristallstrukturen und Kristallchemie im System Na1+xZr2SixP3-xO12. Materialforschung Bulletin, 1976,11(2):173-182.
[17] RAN L B, BAKTASH A, LIM, et al. Sc, Ge-Co-Dotierung mit NASICON steigert die Leistung von Festkörper-Natriumionenbatterien. Energiespeichermaterialien, 2021,40:282-291.
[18] YANG J, LIU GZ, AVDEEV M, et al. Ultrastabile wiederaufladbare Festkörper-Natriumbatterien. ACS-Energiebriefe, 2020,5(9):2835-2841.
[19] LENG H Y, HUANG J J, NIE J Y, et al. Kaltsinterung und Ionenleitfähigkeiten des Feststoffs Na3,256Mg0,128Zr1,872Si2PO12 Elektrolyte. Journal of Power Sources, 2018,391:170-179.
[20] HUANG C C, YANG G M, YU W H, et al. Galliumsubstituierte Nasicon Na3Zr2Si2PO12-Festelektrolyte. Zeitschrift für Legierungen Und Verbindungen, 2021,855:157501.
[21] ZHANG Z Z, ZHANG Q H, SHI J N, et al. Ein selbstbildender Verbundelektrolyt für Festkörper-Natriumbatterien mit Ultralange Lebensdauer. Advanced Energy Materials, 2017,7(4):1601196.
[22] ANANTHARAMULU N, RAO K K, RAMBABU G, et al. Eine umfassende Übersicht über Materialien vom Typ Nasicon. Zeitschrift für Materialien Wissenschaft, 2011,46(9):2821-2837.
[23] WANG X X, LIU Z H, TANG Y H, et al. Niedrigtemperatur- und schnelles Mikrowellensintern des Feststoffs Na3Zr2Si2PO12 Elektrolyte für Na-Ionen-Batterien. Journal of Power Sources, 2021,481:228924.
[24] GRADY Z M, TSUJI K, NDAYISHIMIYE A, et al. Verdichtung eines NASICON-Natriumionen-Festkörperelektrolyten unter 400 °C durch Kaltsintern mit einem geschmolzenen Hydroxidlösungsmittel. ACS Angewandte Energiematerialien, 2020,3(5):4356-4366.
[25] SHAO YJ, ZHONG G M, LU YX, et al. A neuartiger Glaskeramik-Verbundelektrolyt auf NASICON-Basis mit verstärktem Na-Ion Leitfähigkeit. Energiespeichermaterialien, 2019,23:514-521.
[26] LENG H Y, NIE J Y, LUO J. Kombinieren Kaltsintern und Bi2O3-aktiviertes Flüssigphasensintern zur Herstellung Mg-dotiertes NASICON mit hoher Leitfähigkeit bei reduzierten Temperaturen. Zeitschrift für Materiomics, 2019,5(2):237-246.
[27] OH J A S, HE L C, PLEWA A, et al. Zusammengesetzter NASICON (Na3Zr2Si2PO12)-Festkörperelektrolyt mit erhöhtem Na+ Ionenleitfähigkeit: Wirkung des Flüssigphasensinterns. ACS Angewandte Materialien & Interfaces, 2019,11(43):40125-40133.
[28] DA SILVA J G P, BRAM M, LAPTEV A M, et al. Sintern eines natriumbasierten NASICON-Elektrolyten: eine Vergleichsstudie zwischen kalten, feldunterstützten und konventionellen Sintermethoden. Zeitschrift der Europäische Keramikgesellschaft, 2019,39(8):2697-2702.
[29] WANG H, OKUBO K, INADA M, et al. Niedrig temperaturverdichtete Keramik auf NASICON-Basis, gefördert durch Na2O-Nb2O5-P2O5-Glas Additiv- und Funkenplasmasintern. Solid State Ionics, 2018,322:54-60.
[30] HUO H Y, GAO J, ZHAO N, et al. A flexible elektronenblockierende Grenzflächenabschirmung für dendritenfreies festes Lithium Metallbatterien. Nature Communications, 2021,12(1):176.
[31] JIA M Y, ZHAO N, HUO H Y, et al. Umfassende Untersuchung von Granatelektrolyten in Richtung anwendungsorientierte Feststoff-Lithium-Batterien. Bewertungen zu elektrochemischer Energie, 2020,3(4):656-689.
[32] ZHAO N, KHOKHAR W, BI Z J, et al. Solide Granatbatterien. Joule, 2019,3(5):1190-1199.
[33] VERTRUYEN B, ESHRAGHI N, PIFFET C, et al. Sprühtrocknung von Elektrodenmaterialien für Lithium- und Natrium-Ionen-Batterien. Materialien, 2018,11(7):1076.
[34] KOU Z Y, MIAO C, WANG Z Y, et al. Neuartiger struktureller Li1.3Al0.3Ti1.7SixP5(3-0.8x)O12-Festkörper vom NASICON-Typ Elektrolyte mit verbesserter Ionenleitfähigkeit für Lithium-Ionen-Batterien. Solide State Ionics, 2019,343:115090.
[35] SHEN L, YANG J, LIU GZ, et al. Hoch Ionenleitfähigkeit und dendritbeständiger NASICON-Festelektrolyt für Festkörper-Natriumbatterien. Materials Today Energy, 2021,20:100691.
[36] LI Y Q, WANG Z, LI C L, et al. Verdichtung und Verbesserung der Ionenleitung von Lithium-Granat-Feststoff Elektrolyte durch fließendes Sauerstoffsintern. Zeitschrift für Energiequellen, 2014,248:642-646.



