Kategorien
neuer Blog
- Leitfaden zur Auswahl von Batterieelektrolyten: Was Einkaufsmanager wissen müssen
- Ausrüstung für Knopfzellenlabore: Die vollständige Checkliste für Batterie-Forschungs- und Entwicklungslabore
- Vergleich der Kathodenmaterialien für Batterien: NMC vs. LFP vs. NCA
- Trends in der Lithium-Ionen-Batterieherstellung 2026: Ein Leitfaden für B2B-Käufer
- Schritt-für-Schritt-Anleitung zum Herstellungsprozess von Lithium-Ionen-Batterien
Tags
Sb-dotiertes O3-Kathodenmaterial vom Typ Na0,9Ni0,5Mn0,3Ti0,2O2 für Na-Ionen-Batterien
Sb-dotiertes O3-Kathodenmaterial vom Typ Na0,9Ni0,5Mn0,3Ti0,2O2 für Na-Ionen-Batterien
KONG Guoqiang, LENG Mingzhe, ZHOU Zhanrong, XIA Chi, SHEN Xiaofang. Sb-dotierte O3-Kathode vom Typ Na0,9Ni0,5Mn0,3Ti0,2O2 Material für Na-Ionen-Batterie[J]. Journal of Inorganic Materials, 2023, 38(6): 656-662.
Zusammenfassung
Zyklenstabilität und spezifische Kapazität von Kathodenmaterialien für Natriumionenbatterien spielen dabei eine wichtige Rolle ihre breite Anwendung. Basierend auf der Strategie der Einführung spezifischer Heteroelemente zur Optimierung der strukturellen Stabilität und der spezifischen Kapazität von Kathodenmaterialien, O3-Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) wurde durch eine einfache Festkörperreaktionsmethode und die Wirkung von Sb hergestellt Dotierungsmenge auf die Natriumspeichereigenschaften von Na0,9Ni0,5Mn0,3Ti0,2O2 Kathodenmaterialien wurden untersucht. Die Charakterisierungsergebnisse zeigen, dass die elektrostatische Abstoßungskraft zwischen Sauerstoffatomen im Übergangsmetall Die Schicht wird nach der Sb-Dotierung verkleinert, während der Gitterabstand erweitert wird fördert die Deinterkalation von Na+. Inzwischen das starke Elektron Die durch Sb-Dotierung verursachte Delokalisierung verringert die Energie des gesamten Systems. Dies führt zu einer stabilen Struktur, die das zyklische Laden erleichtert und entladen. Der elektrochemische Test zeigt, dass die anfängliche Entladung spezifisch ist Die Kapazität von undotiertem NMTSb0 beträgt 122,8 mAh·gâ1 bei 1C (240 mA·gâ1), und die Kapazitätserhaltungsrate beträgt nach 200 Zyklen nur 41,5 %. Die spezifische Anfangsentladungskapazität von dotiertem NMTSb0,04 beträgt jedoch 135,2 mAh·gâ1 bei 1 °C, und die Kapazitätserhaltungsrate beträgt bis zu 70 % nach 200 Zyklen. Diese Studie zeigt, dass die Sb-dotierte O3-Kathode vom Typ Na0,9Ni0,5Mn0,3Ti0,2O2 ist Das Material kann die spezifische Kapazität der anfänglichen Entladung erheblich verbessern Kapazitätserhaltungsrate von Natriumionenbatterien. Unsere Ergebnisse legen nahe, dass Sb Eine Dopingstrategie könnte ein nützlicher Ansatz für die Vorbereitung eines hohen Stalls sein Natriumionenbatterien.
Schlüsselwörterï¼ Sb Doping; O3-Typ; Kathodenmaterial; Festphasenmethode; breite Spannung; Na-Ion Batterieherstellung
Seit der Kommerzialisierung von Lithium-Ionen Batterien werden häufig in tragbaren elektronischen Geräten und Elektrogeräten verwendet Fahrzeuge und elektrochemische Energiespeicher usw. Allerdings sind die begrenzten Ressourcen und die ungleichmäßige Verteilung von Lithium sind ein wichtiger einschränkender Faktor die Entwicklung von Lithium-Ionen-Batterien. Gleichzeitig sind Natriumreserven vorhanden reichlich vorhanden und weit verbreitet, und was noch wichtiger ist, aufgrund der Ähnlichkeit von die chemischen Eigenschaften von Lithium und Natrium, das Wirkprinzip von Natrium-Ionen-Batterien ähneln denen von Lithium-Ionen-Batterien. Daher ist die Anwendung von Natrium-Ionen-Batterien im Bereich der Energiespeicherung im großen Maßstab hat große Beachtung gefunden.
Kathodenmaterialien für Natrium-Ionen-Batterien
Dazu gehören hauptsächlich Übergangsmetallschichtoxide, polyanionische Verbindungen und
Preußischblaue Analoga. Darunter ist das Schichtoxid NaxTMO2 (TM).
Übergangsmetall, 0
Unter den verschiedenen NaxTMO2-Materialien vom O3-Typ berichteten, hat NaxTMO2, das Ni und Mn enthält, viel angezogen Aufmerksamkeit wegen seiner reichlichen Ni/Mn-Ressourcen und seiner hohen Speicherkapazität. NaNi0,5Mn0,5O2 vom O3-Typ hat beispielsweise eine hohe reversible Kapazität (133 mAh gâ1). Gute Ladeleistung (30 °C, 40 mAh gâ1) und lange Zyklenlebensdauer (70 % spezifische Kapazitätserhaltung nach 500 Zyklen bei 3,75 °C). Es gibt jedoch immer noch einige Probleme, die eine weitere Einschränkung darstellen Entwicklung, wie unbefriedigende Ratenleistung, komplexer Phasenübergang beim Laden und Entladen und schneller Kapazitätsabfall, insbesondere bei hohen Temperaturen Spannungen von 4,1–4,5 V. Neuere Studien haben gezeigt, dass eine teilweise Dotierung anderer Elemente können die Reversibilität des Phasenübergangs effektiv verbessern. Für Beispielsweise weist Ti-dotiertes Na0,9Ni0,4Mn0,4Ti0,2O2 eine reversiblere O3-P3-Phase auf Übergang zwischen 2,5 und 4,2 V, höhere spezifische Kapazität (197 mAh g-1) und stabilere Zyklusleistung. Fe-dotiertes NaFe0,2Mn0,4Ni0,4O2 hat eine hohe reversible Kapazität (165 mAh g-1) und einen stabilen Phasenübergang (87 % Kapazität). Retention nach 200 Zyklen) im Bereich von 4,0-4,3 V.
Darüber hinaus kann auch eine Sb5+-Dotierung eine Verbesserung bewirken die Zyklenstabilität und Arbeitsspannung von Kathodenmaterialien. Um zu Erhalten Sie eine stabilere Materialstruktur und eine überlegene Geschwindigkeitsleistung breiterer Spannungsbereich für Schichtoxide vom Typ O3. In dieser Studie war Sb5+ Ni2+ in Na0,9Ni0,5Mn0,3Ti0,2O2 (NMT) teilweise durch ein einfaches ersetzt Festkörpermethode zur Untersuchung der Auswirkung der Sb-Dotierung auf die Elektrochemie Leistung von Schichtoxiden und die Reversibilitätsänderung der O3-P3-Phase Übergang in einem weiten Spannungsbereich.
1 Experimentelle Methode
1.1 Materialvorbereitung
Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) Materialien wurden durch die Festphasenmethode hergestellt. Das Spezifische Die Schritte sind wie folgt: Mischen Sie Na2CO3, NiO, Sb2O5, MnO2 und TiO2 im entsprechendes stöchiometrisches Verhältnis und fügen Sie einen zusätzlichen Molenanteil von 5 % hinzu Na2CO3 unter Berücksichtigung der Flüchtigkeit von Na bei hohen Temperaturen. Mahlen Sie es Mit einem Achatmörser gleichmäßig verteilen und mit einer Tablettiermaschine eine dünne Scheibe von Ï16 mm formen. Je zweimal Wärmebehandlung bei 950 °C in Luftatmosphäre für 12 Std. Das gleiche Verfahren wurde zur Herstellung von NMTSb0 ohne Start von Sb2O5 verwendet Material, und alle Proben wurden zur späteren Verwendung in einer Handschuhbox aufbewahrt.
1.2 Batteriebaugruppe
Das aktive Material NMTSbx, Acetylenruß und Polyvinylidenfluorid (PVDF) wurden im Massenverhältnis 7:2:1 eingewogen und Zum Erhalt wurde eine geeignete Menge N-Methylpyrrolidon (NMP) zugegeben eine gleichmäßig gemischte Aufschlämmung. Die Aufschlämmung wurde auf die Oberfläche von Aluminium aufgetragen Folie und die Oberflächenbeladung des Aktivmaterials in der Elektrode betrug ca 2,5 mg cm-2. 12 Stunden lang bei 80 °C vakuumgetrocknet und dann mit einem Mikrotom als positiver Elektrode in kleine Scheiben von Ï12 mm geschnitten. CR2032-Taste Die Zellen wurden in einer mit Ar-Gas gefüllten Handschuhbox zusammengebaut (die Volumenanteile von Wasser und Sauerstoff lagen beide unter 1Ã10-6). Darunter die Gegenelektrode ist ein Natriumblech, der Separator besteht aus Glasfaser und der Elektrolyt ist 1 mol L-1 NaClO4 Dibutylcarbonat + Fluorethylencarbonatlösung (Vol Verhältnis 1 : 1).
1.3 Materialcharakterisierung und -prüfung
Das Röntgenbeugungsspektrum (XRD) des Die Probe wurde mit MiniFlex 600 (Rigaku, Japan, Cu Kα) und dem Kristall getestet Die Struktur wurde von Rietveld durch die Strukturanalyse weiter verfeinert System (GSAS + EXPGUI). Die mikroskopische Morphologie und Partikelgröße der Die Proben wurden mit dem Rasterelektronenmikroskop JSM-7610F (JEOL, Japan) beobachtet (REM) und hochauflösendes Transmissionselektronenmikroskop JEOL JEM-2100F (HRTEM). Die Röntgenphotoelektronenspektroskopie (XPS) des Valenzzustands des Elemente wurden auf einem Escalab250xi-Spektrometer mit achromatischer AlKα-Röntgenstrahlung getestet Quelle. Das Molverhältnis jedes Elements in der Probe wurde analysiert Optisches Emissionsspektrometer mit induktiv gekoppeltem Plasma (ICP-AES, iCAP 6300). Lade- und Entlademessungen wurden bei Raumtemperatur unter Verwendung von a durchgeführt Land CT2001A Batterietestsystem zwischen 2,0 und 4,2 V und der elektrochemischen Die Impedanzspektroskopie (EIS) der Elektroden wurde mit einem CHI660E gemessen Elektrochemischer Arbeitsplatz (CH Instruments).
2 Ergebnisse und Diskussion
2.1 Strukturmerkmale von NMTSbx
Die elementare Zusammensetzung aller Proben wurde durch ICP-AES bestimmt und die Ergebnisse sind in Tabelle S1 aufgeführt. Innerhalb der Bereich des Messfehlers, der tatsächliche Gehalt jedes Metallions ist grundsätzlich im Einklang mit der Designkomposition. Im XRD-Spektrum von Abb. 1(a) alle Proben haben eine hexagonale α-NaFeO2-Struktur vom O3-Typ (Raumgruppe R-3m), im Einklang mit NaNi0,5Mn0,5O2 (JCPDS 54-0887). Es zeigt sich, dass die Die Einführung von Sb in das NMT-Gitter verändert die intrinsische Struktur nicht des Materials. Das Verfahren zur Herstellung von Schichtoxidkathoden mit hohem Nickelgehalt durch Bei der Festkörpermethode wird zwangsläufig eine kleine Menge an Rückständen entstehen inaktive NiO-Komponenten, und die Literatur zeigt, dass die Auswirkungen von Spuren Die Auswirkungen von NiO auf die Batterieleistung sind vernachlässigbar. In Abb. 1(b) ist die Beugungspeaks von NMTSb0.02, NMTSb0.04 und NMTSb0.06 zu groß verschoben Winkel und verschiedene Peaks begannen in NMTSb0.06 aufzutreten. Laut der Bragg-Gleichung (nλ=2dsinθ), die durchschnittliche Korngröße des Pulvers ist qualitativ analysiert. wobei n die Beugungsordnung und d die durchschnittliche Dicke (nm) ist. der Körner der Probe senkrecht zur Kristallrichtung Ebene ist θ der Beugungswinkel, der der stärksten Beugung entspricht Peak und λ ist die Röntgenwellenlänge (nm). Die Ergebnisse der Kristallebenenberechnung zeigen, dass die Korngröße der Probe nach der Sb-Dotierung abnimmt hängt mit dem Unterschied im Ionenradius von Sb (0,06 nm) und Ni (0,069) zusammen nm). Nach dem Satz von Vegard bedeutet dies auch, dass es sich um eine solide Lösung handelt Die Reaktion erfolgte während der Bildung von NMTSbx.
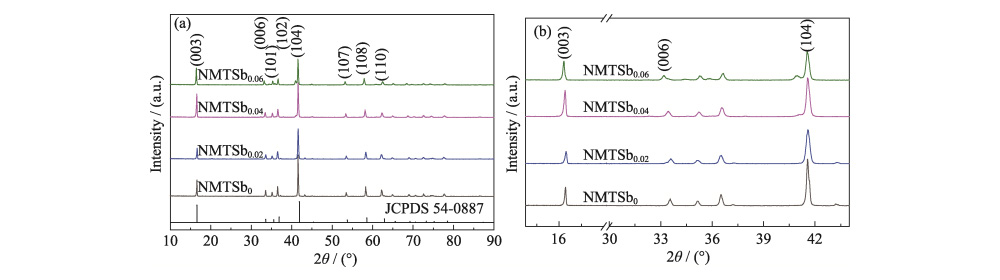
Abb. 1 Umfrage (a) und vergrößerte (b) XRD-Muster von NMTSbx (x=0, 0,02, 0,04, 0,06)
Abbildung 2(a, b) zeigt die verfeinerte XRD Rietveld-Muster von NMTSb0 und NMTSb0.04 und die detaillierten Gitterparameter sind in Tabelle S2 aufgeführt. Es ist ersichtlich, dass die Gitterparameter von NMTSb0.04 (a=b=0,29790 nm) sind im Vergleich zum ursprünglichen NMTSb0 leicht reduziert (a=b=0,29812 nm). Dies wird auch auf die Tatsache zurückgeführt, dass der Ionenradius von Sb (0,06 nm) ist kleiner als der von Ni (0,069 nm), was mit dem übereinstimmt XRD-Analyse. Der c (c=1,608391 nm) von NMTSb0,04 war im Vergleich zu erhöht das von NMTSb0 (c=1,600487 nm). Der Hauptgrund ist der Gitterparameter a/b reagiert empfindlich auf die Änderung der (Ni/Mn/Ti/Sb)-O-Bindungslänge des Schichtstruktur auf der Basisebene, und der Einbau von Sb verkürzt die Bindung Länge. Dies verursacht die elektrostatische Abstoßung zwischen Sauerstoffatomen im Die kontinuierliche Übergangsmetallschicht (Ni/Mn/Ti/Sb) wird größer, was zu einer Anstieg in c. Darüber hinaus ergab sich nach der Berechnung das c/a von NMTSb0 und NMTSb0,04 Es änderte sich nicht viel, sie lagen bei 5,36 bzw. 5,39, beide waren größer als 4,99, was darauf hinweist, dass die dotierten Proben eine gute Schichtstruktur beibehielten.
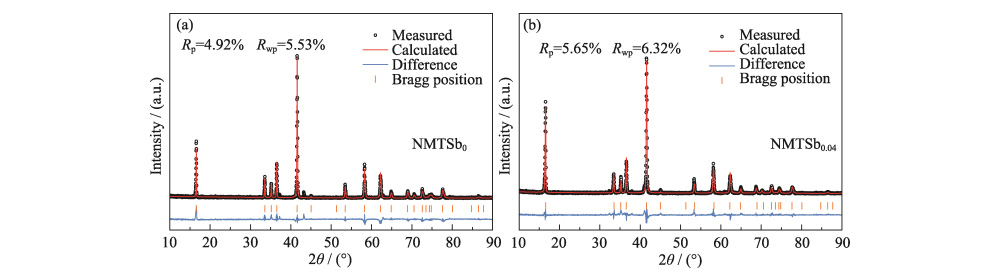
Abb. 2 Rietveld Verfeinerung der XRD-Muster von NMTSb0 (a) und NMTSb0.04(b)
Abbildung 3 zeigt die SEM-Bilder von NMTSb0 und NMTSb0.04. Beide Produkte bestehen aus einer Vielzahl von Mikro-Nano-Maßstäben dünne Scheiben mit gleichmäßiger Dicke und klaren Kanten. Besonders nach SB-Doping, Die Flockenoberfläche ist glatter und es mangelt nicht an sechseckigen Flocken Struktur mit scharfen Kanten und Ecken. EDS-Elementaranalyse ausgewählter Bereiche von NMTSb0.04 zeigt, dass die Elemente Na, O, Ni, Ti, Mn und Sb gleichmäßig verteilt sind in der Probe, was auch beweist, dass Sb-Elemente erfolgreich dotiert wurden die intrinsische Struktur von NMTSb0.

Abb. 3 SEM Bilder und EDS-Zuordnungen von NMTSb0 (a, b) und NMTSb0.04 (c, d)
Die Mikrostrukturen von NMTSb0 und NMTSb0.04 wurden weiter mit HRTEM beobachtet und die Ergebnisse sind in Abbildung S1 dargestellt. In Abbildung S1(a, c), die Partikel vor und nach der Sb-Dotierung sind verbunden oder überlagert und makroskopisch als blattartiges oder annähernd erscheinen kreisförmige oder vieleckige Struktur. Die HRTEM-Bilder von Abbildung S1(b, d) zeigen das Gitterränder des Materials und die Gitterabstände von NMTSb0 und NMTSb0,04 sind 0,238 bzw. 0,237 nm. Beide entsprechen der (101) Kristallebene, und die Auswirkung der Dotierung von Sb auf den Gitterabstand ist konsistent mit den Ergebnissen der XRD-Analyse. Die Einschübe in Abbildung S1(b, d) sind die Punkte von das ausgewählte Flächenelektronenbeugungsmuster (SEAD) von NMTSb0 und NMTSb0.04, was beweist, dass die erhaltenen NMTSb0 und NMTSb0,04 eine gute Kristallinität aufweisen.
Die Röntgenphotoelektronenspektroskopie (XPS) Abbildung S2 zeigt die Oxidationszustandsergebnisse der Elemente Mn, Ni, Ti und Sb in NMTSb0 und NMTSb0.04. In Abbildung S2(a) sind die beiden Hauptpeaks von NMTSb0 bei 877 zu sehen und 850 eV entsprechen Ni2p1/2 bzw. Ni2p3/2 und beide gehören zu Ni2+ in der Probe. Der Bindungsenergiepeak bei 858,2 eV ist ein häufiger Begleiter Peak im Ni-Element. Das Ni2p1/2 von NMTSb0.04 spaltet sich in zwei Peaks auf, was darauf hinweist dass die Einführung von Sb in das NMTSb0-Gitter die Anzahl reduzieren kann äußere Elektronen um Ni herum, was zu einer starken Elektronendelokalisierung führt Wirkung. Übergangsmetalle haben stärker delokalisierte d-Orbitale, was zu einer Verstärkung führen kann die Metall-Metall-Wechselwirkung von seitenverknüpften MO6-Oktaedern in der Schicht Struktur, wodurch der Kollaps von MO6-Oktaedern gehemmt und gemildert wird die Nebenreaktionen von Gittersauerstoff und Elektrolyt. Während der Durch den Lade-Entlade-Prozess wird die Struktur des schichtförmigen Oxidmaterials verändert stabiler, was darauf hindeutet, dass eine starke Elektronendelokalisierung vorteilhaft ist die strukturelle Stabilität von NMTSb0.04. Für das Mn-Element liegt der Mn2p3/2-Peak bei 642 eV und der Mn2p1/2-Peak bei 652 eV in Abbildung S2(b) weisen auf das Vorhandensein von hin Mn im Valenzzustand +4 sowohl in NMTSb0 als auch in NMTSb0.04. Der Mn2p3/2-Peak liegt bei 643 eV können mit dem Mn3+-Peak übereinstimmen. Die oktaedrische Konfiguration von Mn3+ wird deformiert, was durch die Ingwer-Taylor-Verzerrung verursacht wird. Die Auflösung Das Mn-Element führt zu einem schnellen Kapazitätsabfall, während Ti in NMTSb0,04 ersetzt einen Teil von Mn, und die Reduzierung des Mn-Gehalts kann auch stabilisieren Strukturgerüst des Materials und hemmt so den schnellen Verfall Batteriekapazität durch den Ginger-Taylor-Effekt. Die typische Bindungsenergie Peaks von Ti2p1/2 und Ti2p3/2 bei 457,3 und 453,1 eV für NMTSb0 in Abbildung S2(c) entsprechen dem stabilen +4-Valenzzustand von Ti. Während Ti2p1/2 und Ti2p3/2 Peaks bei 454,1 und 463,9 eV von NMTSb0,04 entsprechen Ti in der Wertigkeit +3 Zustand. Aus Sicht der Gebührenentschädigung ist dies vor allem darauf zurückzuführen Reduktionsreaktion von Ti nach Einführung von hochvalentem Sb5+. Während Während der Lade-Entlade-Reaktion existierte Ti4+ weiterhin in stabiler Form wurde in der Cyclovoltammetrie (CV)-Kurve von NMTSb0,04 verifiziert, wie in gezeigt Abbildung 4. Dies zeigt auch, dass die Quelle der Batteriekapazität keine Rolle spielt mit dem Redoxpaar Ti4+/Ti3+. Darüber hinaus sind die Bindungsenergiespitzen von NMTSb0,04 bei 529â536 eV in Abbildung S2(d) bestätigen das Vorhandensein von Sb.
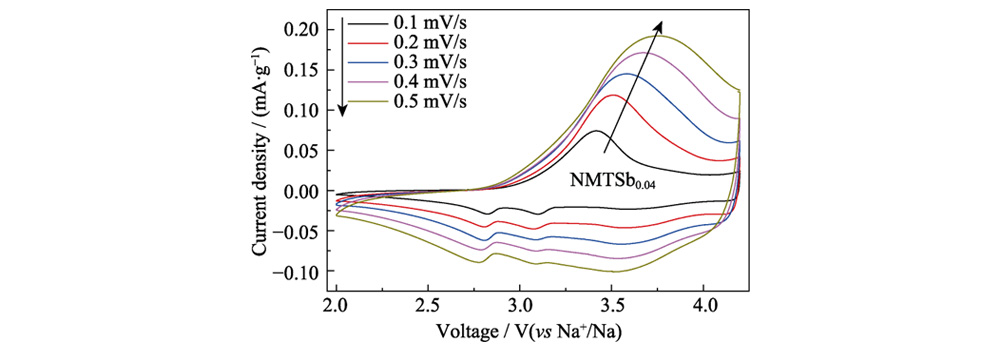
Abb. 4 Lebenslauf Kurven des Kathodenmaterials NMTSb0,04
2.2 Elektrochemische Leistung
Abbildung 5 zeigt die Elektrochemie Impedanz-Nyquist-Diagramm von NMTSbx. Darunter der Halbkreis in der Mitte und Der Hochfrequenzbereich repräsentiert den Ladungsübertragungswiderstand (Rct) zwischen dem Elektrolyten und der Elektrode und der schrägen Linie im Niederfrequenzbereich Der Bereich stellt den Warburg-Widerstand dar, der durch die Diffusion von Natrium verursacht wird Ionen. Die Anpassung des Ersatzschaltbildes zeigt, dass der Rct von NMTSb0 und NMTSb0.04 betragen 1185,4 bzw. 761 Ω. Mit zunehmendem Sb-Dotierungsgehalt steigt der Auch die Impedanz der Probe nimmt ab. Wenn x=0,04, ist die Impedanz des Probe erreicht den Minimalwert. Weitere Erhöhung des Sb-Dotiergehalts führt zu einer Impedanzerhöhung. Wenn x=0,06, übersteigt die Impedanz die von das NMTSb0-Beispiel. Durch einen geeigneten Dotierungsgehalt kann das optimale Metall erhalten werden Zwischenschichtabstände der Schichtstruktur sorgen für einen reibungslosen Elektronentransport Kanäle tragen dazu bei, die dynamischen Eigenschaften von NMTSb0.04 zu verbessern Gleichzeitig ist die Stabilität der Gesamtkonstruktion zu berücksichtigen.
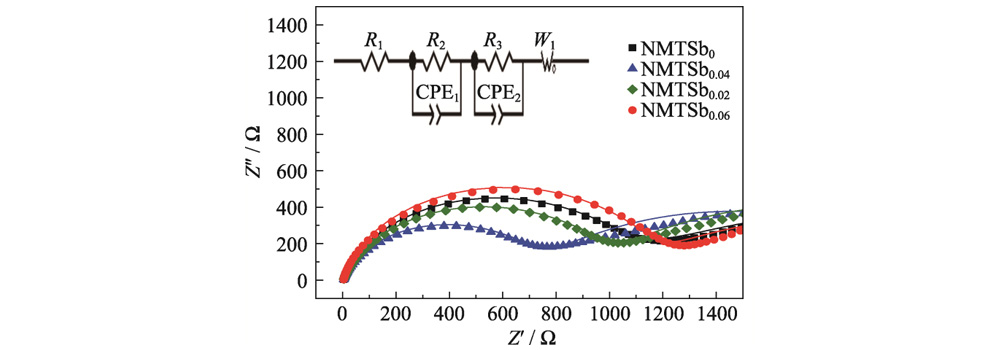
Abb. 5 Elektrochemisch Impedanzspektren von NMTSbx
Unter der Bedingung der Stromdichte von 1C (240 mA·gâ1) und Spannungsbereich von 2,0–4,2 V, das Natrium Speicherleistung der Na-Ionen-Batterie mit NMTSbx als Elektrode getestet. Wie in Abbildung 6(a) dargestellt, sind die reversiblen Kapazitäten von NMTSbx (x=0, 0,02, 0,04, 0,06) Proben sind 122,8, 128,0, 135,2 bzw. 103,9 mAh gâ1. Der Unterschied in der spezifischen Kapazität ist darauf zurückzuführen unterschiedliche Dopinginhalte. Die Strategie der Substitution chemischer Elemente kann unterdrücken den irreversiblen Phasenübergang und verbessern den Natriumionentransport Kinetik. Die Vorteile lassen sich wie folgt zusammenfassen: Hochaktiv ersetzen Elemente mit elektrochemisch inaktiven und strukturstabilen Elementen, wie z als Verhinderung der Kationenvermischung durch Erhöhung der Energiebarriere der Ni2+-Migration, und Reduzieren des während des elektrochemischen Kreislaufs freigesetzten Sauerstoffs durch Stärkung der Metall-Sauerstoff-Bindungen. Dotieren oder Ersetzen von Übergangsmetallstellen kann den Phasenübergang erheblich hemmen und Übergangsmetallionen hemmen Migration und verbessern die chemische und elektrochemische Stabilität von desodiumisierte Materialien. Der konkrete Dopinggehalt sollte erforscht werden abhängig von der Art des Dotierungselements und der intrinsischen Struktur. . Auf der Einerseits kann die Dotierung mit hochvalenten Metallionen die Gesamtleitfähigkeit verbessern des Materials, nachdem die Metallionen in das Innere des Gitters gelangt sind. Wann der Molenanteil der Dotierung ist größer als 1 % (stöchiometrisches Verhältnis). x0,01) nimmt der spezifische Widerstand schnell ab, was große Auswirkungen hat Einfluss auf die Leitfähigkeit. Andererseits führt eine zu hohe Dopingmenge dazu zwangsläufig den Gehalt an Redoxpaaren im System verringern und die beeinflussen Energiedichte des Systems, während eine zu geringe Dotierungsmenge nicht ausreicht zur Stabilisierung der Struktur schichtförmiger Oxidmaterialien. In dieser Studie NMTSbx(x=0, 0,02, 0,04, 0,06), x ist das stöchiometrische Verhältnis und das tatsächliche Der Dotierungsgehalt beträgt 2 %, 4 % bzw. 6 % nach Molanteil.
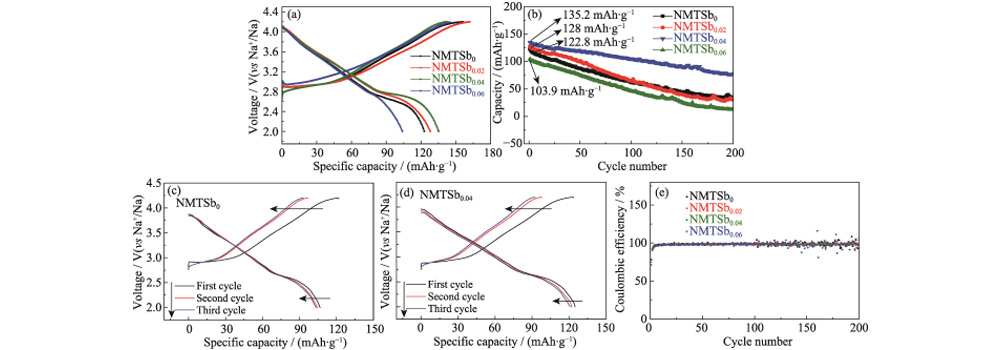
Abb. 6 Leistung von Na-Ionen-Batterien mit NMTSbx als Elektroden
(a) Aufladen und Entladekurven von Na-Ionen-Batterien mit Proben als Elektroden für den ersten Zyklus bei 1 °C; (b) Zyklenleistung von Na-Ionen-Batterien mit Proben wie Elektroden bei 1 C für 200 Zyklen; (c, d) Laden und Entladen Kurven von Na-Ionen-Batterien mit Proben als Elektroden für die ersten drei Zyklen bei 5 °C; (e) Coulomb-Effizienz von Na-Ionen-Batterien mit NMTSbx as Elektroden für 200 Zyklen bei 1C Farbige Abbildungen finden Sie auf Website
In Abb. 6(a) ist die Lade-Entlade-Kurve von Die undotierte Probe NMTSb0 enthält offensichtlich mehrere Spannungsplateaus und Schritte, was darauf hinweist, dass es mehrere Phasenübergänge von hexagonal zu monoklin gibt können im Schichtaufbau auftreten. Während jedoch der Zwischenschichtschlupf der Wenn eine Übergangsmetallschicht auftritt, ist die gesamte Lade-Entlade-Kurve relativ glatt. Die drei Spannungsplattformen über 3,00 V neigen dazu, unscharf zu sein. Für NMTSb0, die Ladekurve ist hauptsächlich in zwei Teile unterteilt: den Steigungsabschnitt etwa 3,00–3,80 V und der lange Plateauabschnitt über 3,80 V. Wenn jedoch Sb eingeführt wurde, stieg die Anfangsspannung des Plattformsegments auf über 4,00 V. Bei der Entladekurve tritt üblicherweise das lange Plateau in der Spannung auf Bereich von 2,50–2,75 V. Das Auftreten des Spannungsplateaus kann darauf zurückgeführt werden zur Umwandlung der O3-Phase in die P3-Phase, während die Steigung Segment, wenn die Spannung ansteigt, wird durch die Reaktion der festen Lösung verursacht mit der P3-Struktur. Abbildung 6(b) ist ein Vergleich der Zyklusleistung von NMTSbx (x=0, 0,02, 0,04, 0,06) Elektroden bei einer Stromdichte von 1C. Es ist Erwähnenswert ist, dass die Zyklenstabilität des Kathodenmaterials NMTSb0,04 ist am besten, und etwa 70 % der reversiblen Kapazität können nach 200 beibehalten werden Zyklen. Im Gegensatz dazu nimmt die spezifische Kapazität der NMTSb0-Elektrode stark ab schnell, mit einem Anfangswert von 122,8 mAh g-1, der auf 51 mAh g-1 sinkt nach 200 Zyklen sind nur noch 41,5 % der spezifischen Kapazität übrig. In Abb. 6(c, d), selbst bei einer sehr hohen Rate von 5C (1200 mA gâ1), die Die spezifische Kapazitätserhaltung der NMTSb0,04-Elektrode beträgt immer noch 92,6 % (125,3). mAh gâ1). Die spezifische Kapazität des NMTSb0 Elektrode ist nur 106,7 mAh·gâ1, was überlegen ist andere berichtete Schichtoxide vom O3-Typ. Die anfängliche spezifische Entladungskapazität von O3-Na(Ni1/3Mn1/3Fe1/3)0,95Al0,05O2, hergestellt von Yans Gruppe mit einer Geschwindigkeit von 0,1C beträgt 145,4 mAh·gâ1. Und nach 80 Zyklen bei einer Rate von 0,2 °C ist das reversible Spezifische Die Kapazität beträgt 128,4 mAh·gâ1. Das O3-NaNi0,5Mn0,5O2 Die von Guos Forschungsgruppe hergestellte Batterie hat eine spezifische Kapazität von 80 mAh·g-1 im Spannungsbereich von 2-4 V bei einer Rate von 2C. Abbildung 6(e) zeigt die Coulomb-Effizienz des Na-Ionen-Batterie während des kontinuierlichen Radfahrens bei 1 °C. Unter ihnen die Coulomb-Methode Die Effizienzverteilung der NMTSb0,04-Elektrode ist stabil und tendiert zu a gerade Linie, die im Wesentlichen bei 98 % bleibt, was ebenfalls anzeigt, dass es so ist Die Schichtstruktur ist stabiler. Allerdings ist die Coulomb-Effizienz des Die NMTSb0-Elektrode schwankte nach 140 Zyklen erheblich, und es gab eine großer Sprung, als es fast 200 Zyklen waren. Die Batterie zusammengebaut mit NMTSb0,04 wurde nach 200 Zyklen zerlegt und verarbeitet, und das XRD-Spektrum wurde erstellt des Elektrodenblatts getestet wurde, sind die Ergebnisse in Abbildung S3 dargestellt. Das XRD Beugungspeaks des NMTSb0.04-Polstücks verschoben sich danach nicht wesentlich Radfahren, was darauf hinweist, dass die NMTSb0,04-Kathode irreversible Phasenänderungen aufweist Material wurde nach der Dotierung unterdrückt.
3 Fazit
In dieser Studie Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06), ein geschichtetes Oxid-Kathodenmaterial für Natrium-Ionen-Batterien, wurde durch eine praktische Festkörpermethode hergestellt. Es ist Partikel bestehen aus Mikro-Nano-Flocken mit gleichmäßiger Dicke und klare Kanten und die Korngröße nimmt ab, nachdem Sb einen Teil von Ni ersetzt hat. Am Gleichzeitig führt die Dotierung von Sb zu einer starken Elektronendelokalisierung, die reduziert die Energie des gesamten Systems und erhält eine stabile Struktur geeigneter für langfristige Lade-Entlade-Zyklen. In der Elektrochemie Test im Bereich von 2,00–4,20 V unterdrückte die Dotierung mit Sb die irreversible Phase Übergang des Kathodenmaterials und Verbesserung der Arbeitsspannungsplattform. Beim Laden und Entladen mit einer Rate von 1 °C ist dies die spezifische Anfangsentladungskapazität von NMTSb0,04 beträgt 135,2 mAh·g-1 und die Kapazitätserhaltungsrate nach 200 Zyklen beträgt 70 %. Die spezifische Kapazitätserhaltung kann 92,6 % (125,3 mAh·gâ1) bei einer Temperatur von 5 °C erreichen.
Ergänzende Informationen

Abb. S1 HRTEM Bilder von NMT (a, b) und NMTSb0.04 (c, d) mit Einschub in (b, d) mit entsprechenden SEAD-Bildern
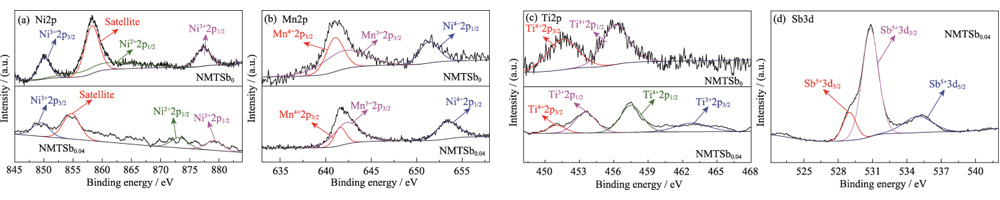
Abb. S2 (a) Ni2p-, (b) Mn2p-, (c) Ti2p- und (d) Sb3d-XPS-Spektren von NMTSb0 und NMTSb0.04
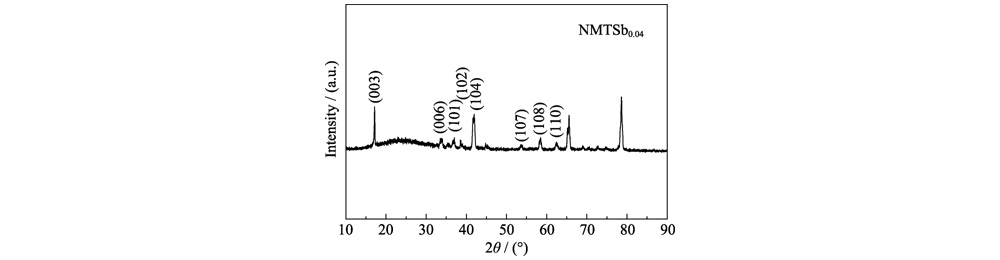
Abb. S3 XRD Muster von NMTSb0.04 als Kathodenmaterial von Na-Ionen-Akku nach 200 Zyklen
Tabelle S1 ICP-AES-Ergebnisse von O3-NMTSbx (x=0, 0,02, 0,04, 0,06) (stöchiometrisches Verhältnis)
|
Na |
Ni |
Mn |
Ti |
Sb |
|
|
NMTSb0 |
0,913 |
0,486 |
0,288 |
0,181 |
0 |
|
NMTSb0.02 |
0,924 |
0,471 |
0,284 |
0,186 |
0,023 |
|
NMTSb0.04 |
0,920 |
0,452 |
0,287 |
0,184 |
0,039 |
|
NMTSb0.06 |
0,929 |
0,435 |
0,279 |
0,184 |
0,061 |
Tabelle S2 Gitterparameter von Materialien mit NMTSb0 und NMTSb0.04
|
a/nm |
b/nm |
c/nm |
V/nm3 |
Rwp/% |
Rp/% |
|
|
NMTSb0 |
0,29812 |
0,29812 |
1.600487 |
0,1232 |
4,92 |
5,53 |
|
NMTSb0.04 |
0,29790 |
0,29790 |
1.608391 |
0,1236 |
5,65 |
6.32 |



